Clear Sky Science · ru
ГликоРНК, в комплексе с гепарансульфатом, регулирует сигналы VEGF-A
Как клетки точно настраивают сигналы для кровеносных сосудов
Сосуды не возникают повсюду, где появляются сигналы роста — их нужно точно контролировать, чтобы питать ткани, но не способствовать опухолям или слепоте. В этой статье раскрыт неожиданный «тормоз» для важного сигнала роста сосудов VEGF-A. Авторы показывают, что небольшие фрагменты РНК, расположенные на внешней стороне клеток в связке с углеводами и белками, могут ослаблять сигнал VEGF-A, меняя наше представление о языке, которым клетки обмениваются на своей поверхности.
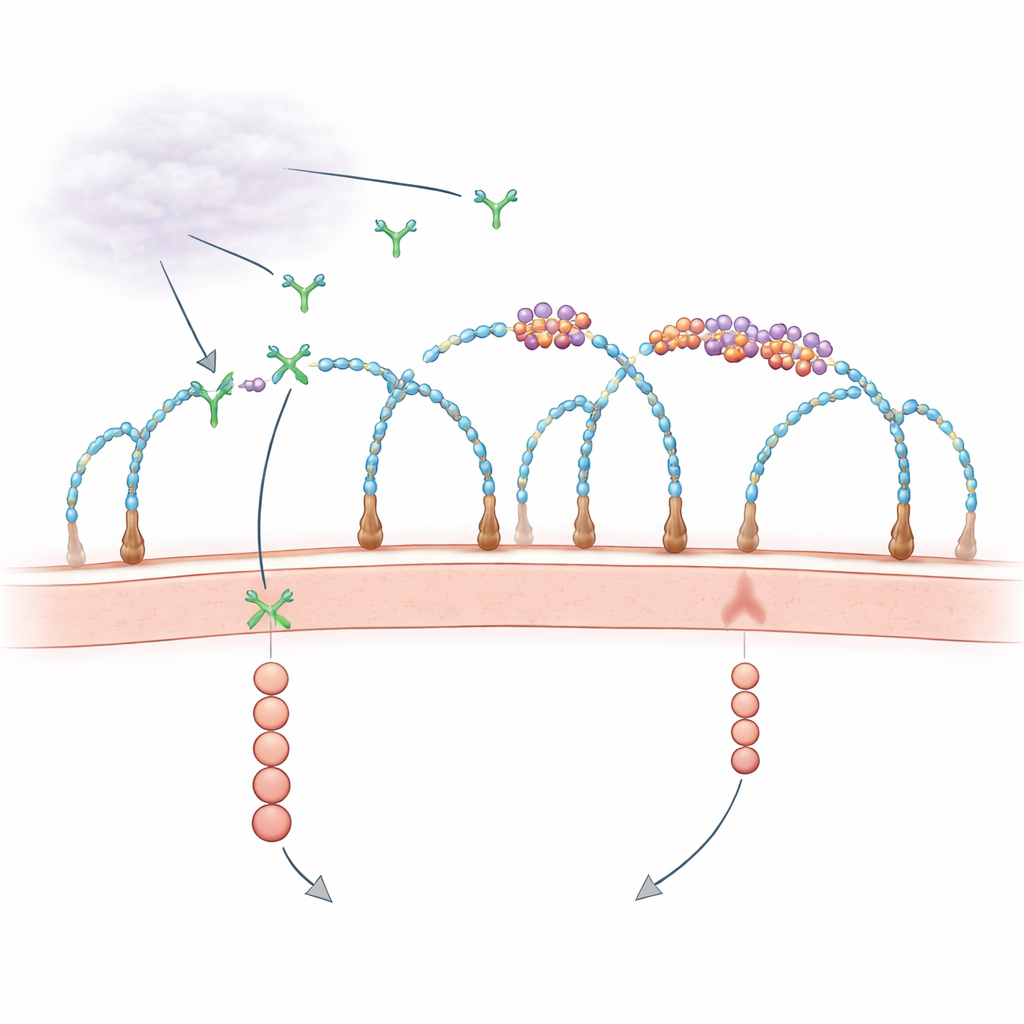
Неожиданный функционал РНК на поверхности клетки
Долгое время биологи знали, что наружный покров клетки, богатый белками, украшенными углеводными цепями — протеогликанами гепарансульфата — помогает захватывать факторы роста и представлять их рецепторам. Одновременно отдельные наблюдения намекали, что фрагменты РНК снаружи клеток могут влиять на рост сосудов, но участники и механизмы были неясны. Недавние работы показали, что некоторые маленькие РНК химически связаны со сложными углеводами, формируя «гликоРНК», и что некоторые РНК-связывающие белки тоже встречаются на поверхности клетки, образуя кластеры вместе с этими РНК. Новое исследование задаёт прямой вопрос: контролируют ли эти крошечные островки РНК–белок на мембране приём сигналов роста, таких как VEGF-A?
Сборка кластеров РНК–белок на углеводных цепях
С помощью широгеномных CRISPR-скринов и высокоразрешающей микроскопии исследователи обнаружили, что специфические углеводные цепи — гепарансульфат с определёнными сульфатными модификациями — служат необходимым каркасом для сборки этих РНК–белковых кластеров, которые они называют рибонуклеопротеинами на поверхности клетки (csRNPs). Когда удаляли ключевые ферменты, ответственные за синтез или сульфирование гепарансульфата, кластеры гликоРНК и их партнёрских белков исчезали с поверхности клетки, хотя сами РНК и белки оставались внутри клетки. Ферменты, отрезающие цепи гепарансульфата от поверхности, или химические блокаторы сульфирования давали тот же эффект. Эти результаты показывают, что целые, правильно сульфатированные цепи гепарансульфата организуют csRNPs в наноразмерные «островки» на мембране.
Кластеры РНК работают как тормоз для мощного сигнала роста сосудов
Дальше команда обратилась к человеческим эндотелиальным клеткам, выстилающим сосуды и реагирующим на VEGF-A. Они обнаружили, что и эти клетки демонстрируют анкеровнные гепарансульфатом csRNP-кластеры. Обработка живых клеток РНКазами, ферментами, разрушающими РНК, удаляла РНК-компонент, не повреждая лежащие в основе углеводные цепи. В таких условиях наиболее распространённая форма VEGF-A, связывающаяся с гепараном (VEGF-A165), вызывала гораздо более сильную активацию нисходящего пути сигнализации ERK, тогда как укороченная форма, лишённая гепаран-связывающего хвоста (VEGF-A121), не претерпевала изменений. После удаления РНК на поверхности клетки связывалось больше молекул VEGF-A165, хотя уровни рецепторов оставались неизменными. В 3D микрофлюидных устройствах эндотелиальные клетки, обработанные РНКазой, глубже прорастали в коллагеновые гели и более активно формировали трубчатые структуры, что указывает на то, что разрушение поверхностной РНК высвобождает проангиогенное поведение.
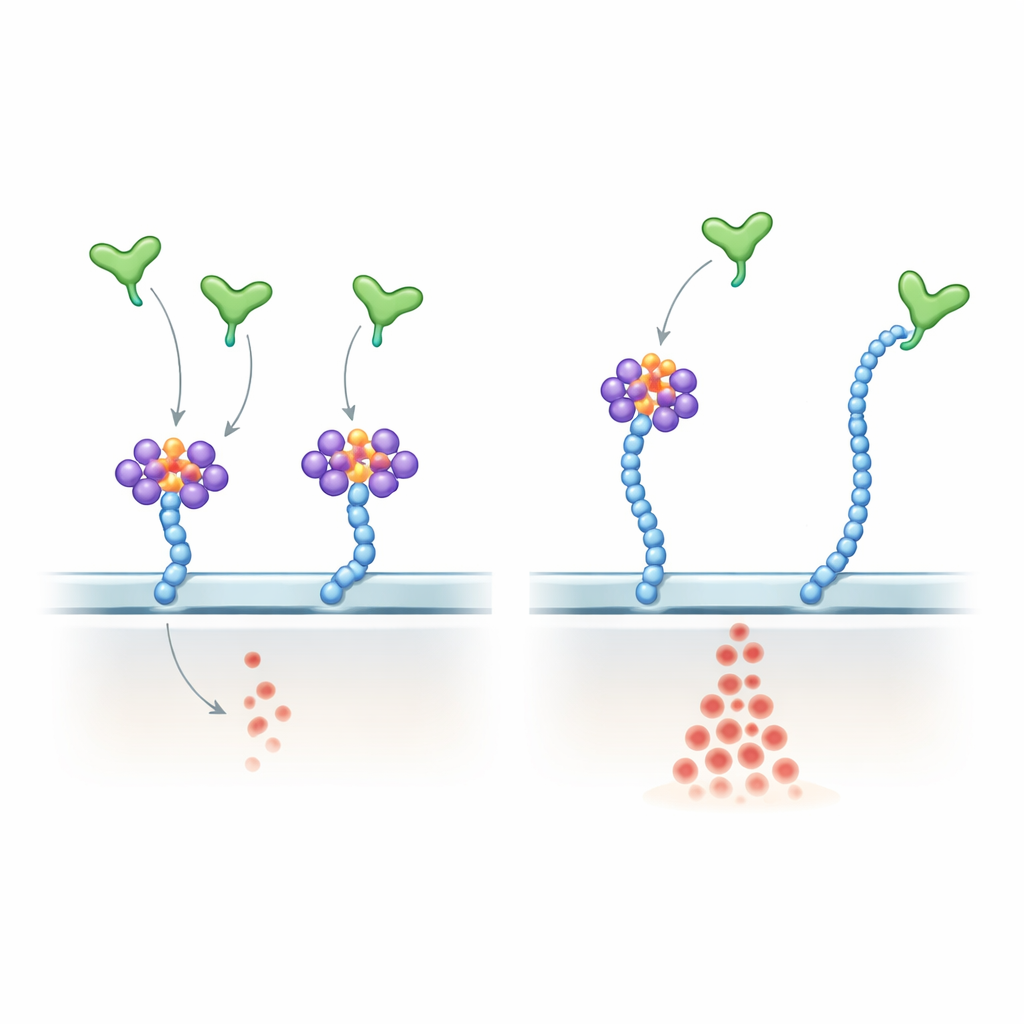
Разбор того, как VEGF-A чувствует РНК и углеводы
Чтобы исследовать механизм, авторы показали, что VEGF-A165 непосредственно связывается с отобранными малыми РНК, включая многие известные гликоРНК, через свою положительно заряженную С-концевую область — ту же область, которая связывает гепарансульфат. Они создали тонкую версию VEGF-A165, в которой ключевые аргининовые остатки в этом хвосте были заменены на лизины. Этот мутант сохранил общий положительный заряд и всё ещё захватывал цепи гепарансульфата, но слабо связывался с гликоРНК и в значительной степени стал нечувствителен к обработке РНКазой. В эндотелиальных клетках мутант вызывал более сильную и более устойчиваю к РНКазе активацию ERK, чем нормальный VEGF-A165, что очень напоминало эффект удаления РНК с поверхности. В живых мышах инъекция мутанта в глаз вызывала более пышный рост сосудов сетчатки, чем нормальный белок. У эмбрионов цыплят/рыбок (зебрафиш) сверхэкспрессия мутантной версии Vegfa нарушала нормальную схему сосудов и увеличивала число эндотелиальных клеток.
От базового механизма к более широким последствиям
Наконец, авторы показали, что присоединение гепаран-связывающего хвоста VEGF-A к несвязанному с ним сигнальному белку Wnt3a может перенаправить активность Wnt: прицепление нормального хвоста ослабляло вызываемые Wnt развитие изменения, тогда как прикрепление RNA-нечувствительного хвоста усиливало их. Вместе эти эксперименты поддерживают модель, в которой csRNP-кластеры, анкерованные специфически сульфатированным гепарансульфатом, связывают VEGF-A и родственные факторы, чтобы умерять их активность. Когда РНК-компонент удалён или когда факторы роста теряют способность чувствовать РНК, равновесие смещается в сторону усиленной сигнализации и изменённого сосудистого развития у нескольких видов.
Почему это важно для здоровья и будущих терапий
Для неспециалиста ключевая мысль такова: клетки используют не только белки и углеводы, но и маленькие РНК на своей поверхности, чтобы тонко настраивать мощные сигналы роста, такие как VEGF-A. Эти углеводные анкеры с РНК–белковыми кластерами действуют как регулируемые тормоза для образования сосудов, помогая новообразованиям появляться тогда и там, где это необходимо. Нарушение этого баланса — путем деградации поверхностной РНК или изменения свойств факторов роста по связыванию РНК — может либо усиливать, либо искажать рост сосудов. Понимание этого недавно выявленного уровня контроля может открыть путь к терапии, которая точнее регулирует ангиогенез в раке, заболеваниях глаза, заживлении ран и регенеративной медицине путем нацеливания на поверхностные РНК, их углеводные каркасы или РНК-чувствительные участки факторов роста.
Цитирование: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Ключевые слова: ангиогенез, сосудистый эндотелиальный фактор роста, гепарансульфат, РНК на поверхности клетки, гликоРНК