Clear Sky Science · ru
Взаимодействие опухоли и мозга сдерживает противоопухолевый иммунитет через сенсорно-симпатическую ось
Как нервы помогают опухолям прятаться
Рак обычно представляют как противостояние между дефектными клетками и иммунной системой, но это исследование выявляет неожиданного третьего участника — нервную систему. Учёные показали, что опухоли лёгких могут подключаться к сенсорно‑симпатическому нервному контуру, связывающему лёгкие с мозгом, и использовать этот путь, чтобы ослабить естественные противораковые защиты организма. Понимание этого скрытого «провода» между опухолью и мозгом может открыть новые подходы к лечению рака лёгкого, нацеливаясь не только на сами раковые клетки, но и на нервы и их сигналы. 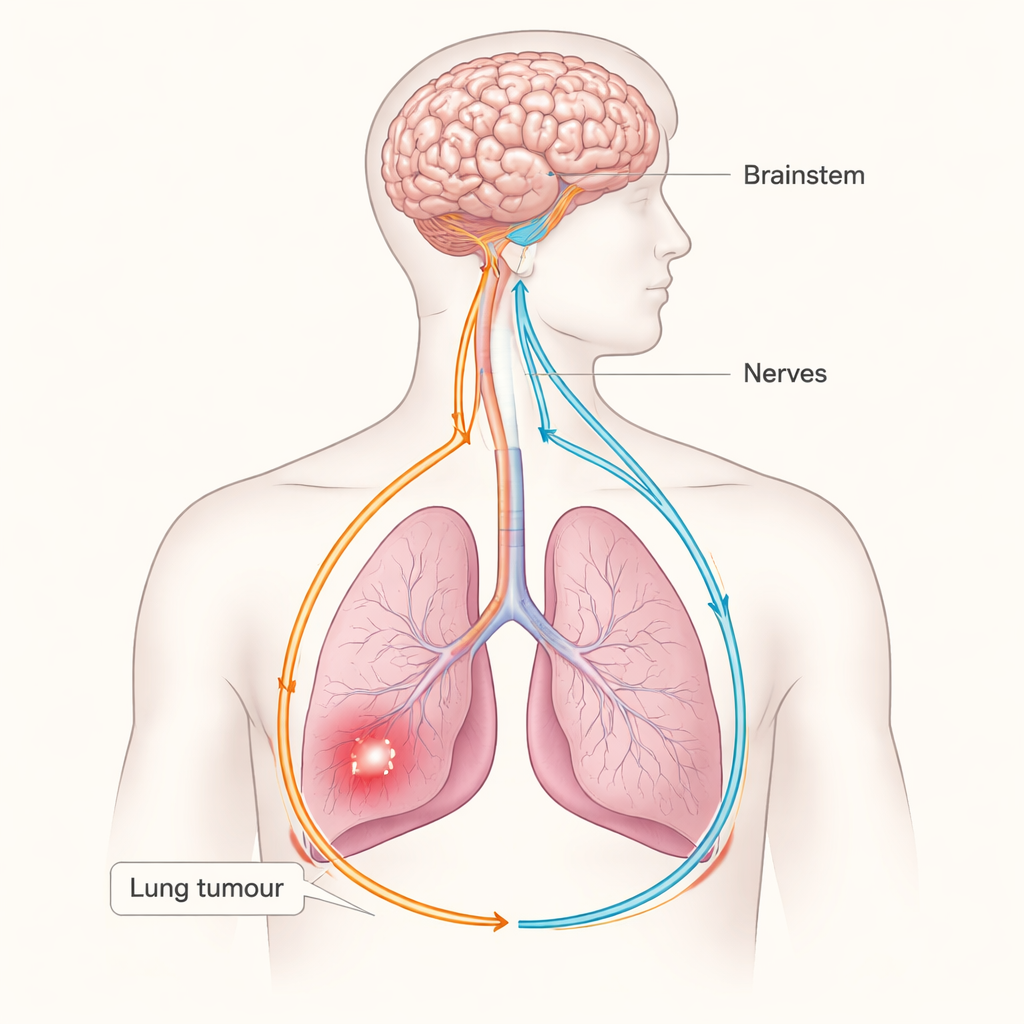
Нервы, прорастающие в опухоль
Команда изучала аденокарциному лёгкого, распространённую форму рака лёгких, в продвинутых модельных мышах, которые хорошо имитируют человеческое заболевание. С помощью 3D‑визуализации целого органа и генетической маркировки они обнаружили, что опухоли в лёгких интенсивно иннервированы нервными волокнами. Эти нервы не случайны: многие исходят от определённой группы сенсорных клеток в блуждающем нерве, который обычно передаёт в мозг информацию о состоянии органов. Наблюдалось, что опухолевые клетки выделяют факторы роста, такие как фактор роста нервов, стимулирующие отростки вагальных сенсорных волокон и их прорастание в опухоль. Одновременно сами сенсорные нейроны изменяли свою генную активность, что указывает на перепрограммирование их реакции по сравнению со здоровой тканью лёгкого.
Одностороннее усиление сигналов, благоприятных для опухоли
Не все сенсорные нейроны, связанные с блуждающим нервом, были вовлечены. Исследователи выделили подтип, отмеченный двумя молекулами — NPY2R и TRPV1 — как ключевой. Эти нейроны были многочисленны внутри участков опухоли и почти отсутствовали в соседних здоровых тканях лёгкого. Когда учёные выборочно удаляли или заглушали эту группу NPY2R/TRPV1 — с помощью генетических методов, направленных токсинов или дизайнерских рецепторов, которые можно было выключить лекарством — опухоли лёгкого значительно уменьшались, а мыши жили дольше с лучшим весом и поведением. Напротив, удаление другой сенсорной подгруппы, иннервирующей иные структуры лёгкого, не замедляло рост опухоли, что подчёркивает: именно специфический сенсорный «канал» встроен в систему контроля опухоли. 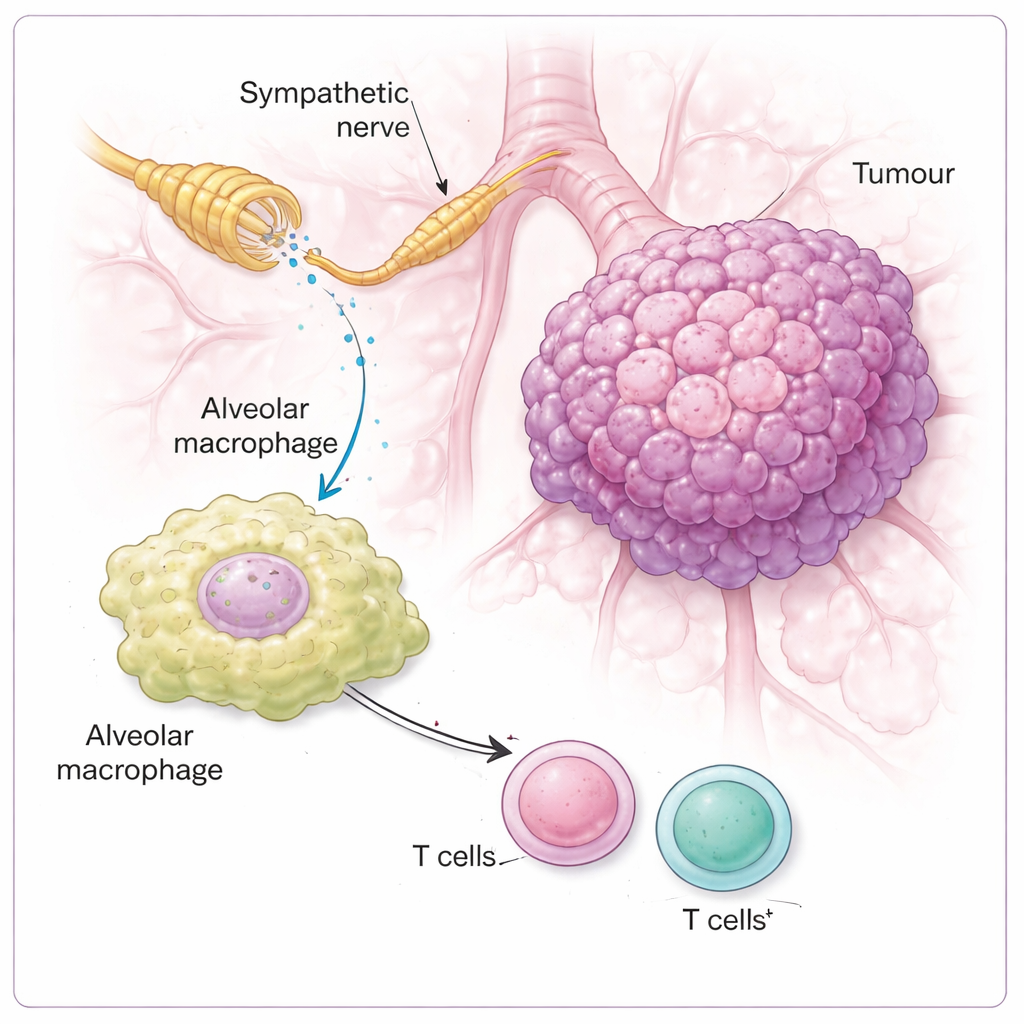
От ствола мозга к стрессоподобным сигналам в лёгком
Чтобы выяснить, как мозг обрабатывает эти сенсорные сигналы, команда проследила контур вверх по направлению к мозгу. Маркеры активности показали, что при наличии опухолей лёгких активируются участки ствола мозга, получающие вагальную информацию, особенно область, называемая ростральной вентролатеральной медуллой — ключевой узел, усиливающий симпатический «бей‑или‑беги» выход. Выключение сенсорных нейронов NPY2R/TRPV1 снижало эту активность ствола мозга и уменьшало количество симпатических волокон и уровень стрессового медиатора норадреналина в области опухоли. Подавление самого узла ствола мозга также замедляло рост опухоли. В сумме эти результаты описывают замкнутую петлю: опухоль стимулирует вагальные сенсорные нервы, ствол мозга отвечает усилением симпатического выхода, а симпатические нервы возвращают влияние на лёгочное окружение так, что это содействует росту рака.
Отключение иммунных клеток через местных посредников
Далее исследование попыталось выяснить, какие клетки в окрестности опухоли «слышат» симпатические сигналы. Удивительно, но норадреналин мало влиял напрямую на рост опухолевых клеток в культуре. Вместо этого ключевыми реагентами оказались иммунные клетки, особенно альвеолярные макрофаги — сторожевые клетки, находящиеся в альвеолах лёгкого. Эти макрофаги экспрессировали высокий уровень рецептора β2‑адренорецептора, который чувствует норадреналин. Когда этот рецептор отсутствовал, или когда норадреналин‑сигналирование блокировали, опухоли росли меньше, а Т‑клеточная атака усиливалась. При интактной нервной петле норадреналин переводил макрофагов в более иммуносупрессивное состояние, отмеченное повышением уровня фермента ARG1, известного подавлять Т‑клетки. После такой перепрограммировки макрофагов близлежащие CD4 и CD8 Т‑клетки — обычно основные киллеры опухолевых клеток — теряли способность развить мощный ответ.
Почему это важно для лечения рака
Проще говоря, авторы показывают, что опухоли лёгких могут «разговаривать» с мозгом через блуждающий нерв и получать вредный ответ через симпатические нервы, которые приказывают местным макрофагам утихомирить Т‑клетки. Разрыв любого из ключевых звеньев этой петли — сенсорного ввода, релейной станции в стволе мозга, симпатического выхода или β2‑адренорецепторного сигнала в макрофагах — был достаточен, чтобы восстановить более эффективный противоопухолевый иммунитет и замедлить развитие рака у мышей. Данные по человеку также указывают, что пациенты с опухолями, демонстрирующими повышенные сигнатуры этих нервных путей, как правило, имеют худший прогноз и меньше киллерных Т‑клеток в опухоли. Работа открывает перспективу, что уже существующие препараты, применяемые при сердечных заболеваниях и тревоге, например бета‑блокаторы, или будущие терапии, нацеленные на специфические нервные контуры, могут быть переориентированы или доработаны, чтобы «перерезать провода», которыми опухоли пользуются, чтобы ускользнуть от иммунной атаки.
Цитирование: Wei, H.K., Yu, C.D., Hu, B. et al. Tumour–brain crosstalk restrains cancer immunity via a sensory–sympathetic axis. Nature 650, 1007–1016 (2026). https://doi.org/10.1038/s41586-025-10028-8
Ключевые слова: нейроонкология, иммунитет при раке лёгкого, блуждающий нерв, симпатическая нервная система, микроокружение опухоли