Clear Sky Science · ru
Индивидуализированные мРНК-вакцины вызывают долговременный Т‑клеточный иммунитет при адъювантной терапии ТНБК
Новая надежда после лечения рака молочной железы
Для многих женщин с агрессивной формой рака молочной железы, называемой тройным негативным раком, страх не исчезает с окончанием химиотерапии и операции. У этого типа опухоли высокий риск рецидива и метастазирования, часто в первые несколько лет. Исследование, описанное здесь, проверяет высокоиндивидуализированную вакцину, созданную на основе мутаций конкретной пациентки, чтобы выяснить, сможет ли она «обучить» иммунную систему охранять организм годами и снизить вероятность рецидива после завершения стандартного лечения.
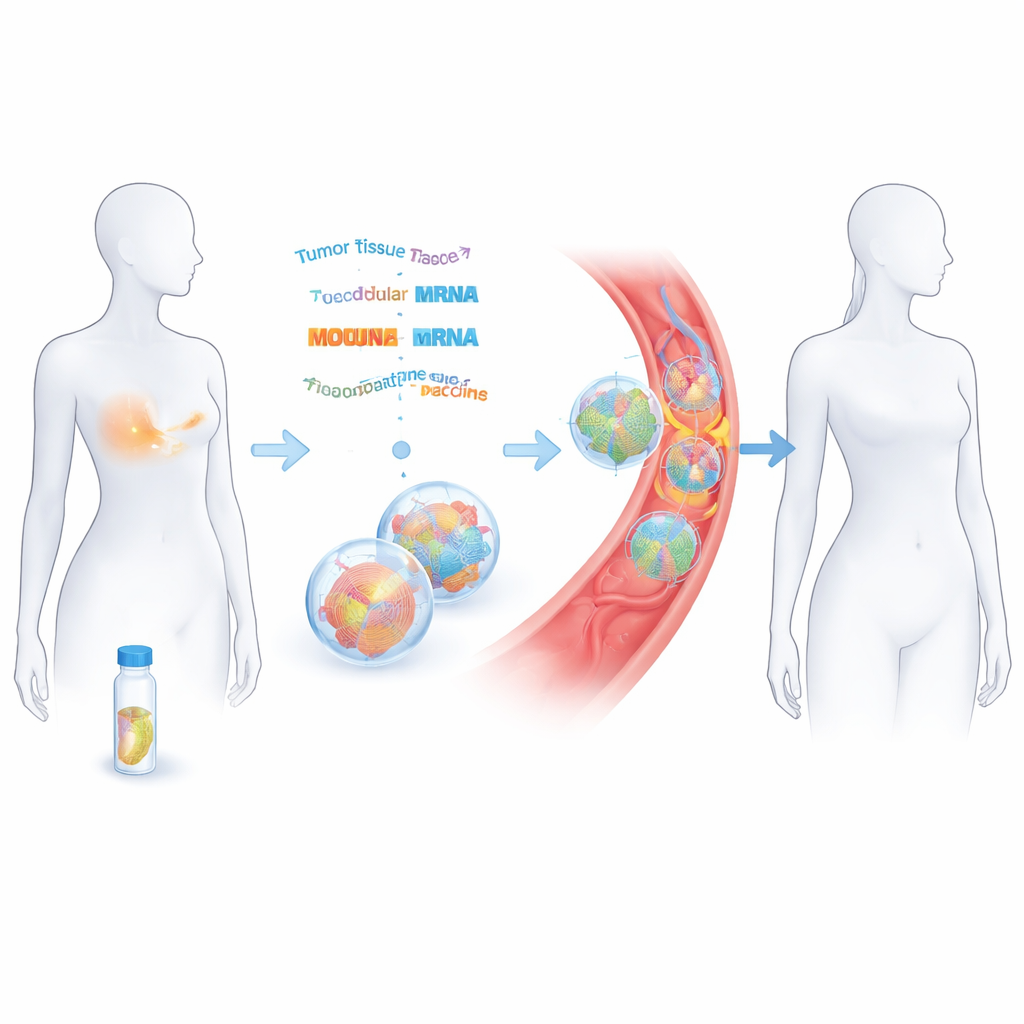
Как удалённую опухоль превращают в индивидуальную вакцину
Исследователи работали с 14 женщинами с ранней стадией тройного негативного рака молочной железы, которые уже прошли операцию и химиотерапию с целью излечения. Из удалённой ткани опухоли они считали ДНК и РНК, чтобы каталогизировать уникальные мутации рака. С помощью компьютерных инструментов предсказывали, какие из этих изменений могут быть восприняты иммунной системой как чужеродные. До 20 таких «неоантигенов» затем связывали вместе и кодировали в двух цепях матричной РНК (мРНК), по принципу схожих с вакцин против COVID‑19, но адаптированных под каждую пациентку. Эти мРНК-цепочки помещали в крошечные липидные пузырьки и вводили внутривенно восемью дозами в течение примерно двух месяцев.
Как вакцина пробуждает иммунных защитников
Попав в организм, мРНК инструктирует дендритные клетки — иммунных стражей — кратковременно синтезировать белки неоантигенов и выставлять их фрагменты на своей поверхности. Это работает как ориентировка для Т‑клеток, основной силы иммунной системы по уничтожению рака. Команда брала кровь до вакцинации и в несколько контрольных точек после, чтобы проверить, появились ли неоантиген‑специфические Т‑клетки и насколько сильными они были. С помощью чувствительных лабораторных тестов было обнаружено, что каждая пациентка развила новые или усилила существующие Т‑клеточные ответы хотя бы на одну из выбранных мутаций, а большинство отвечало на несколько. Во многих случаях значительные доли циркулирующих Т‑клеток — уровни, обычно наблюдаемые лишь при мощных клеточных терапиях — были теперь настроены на распознавание опухолево‑специфических мишеней.
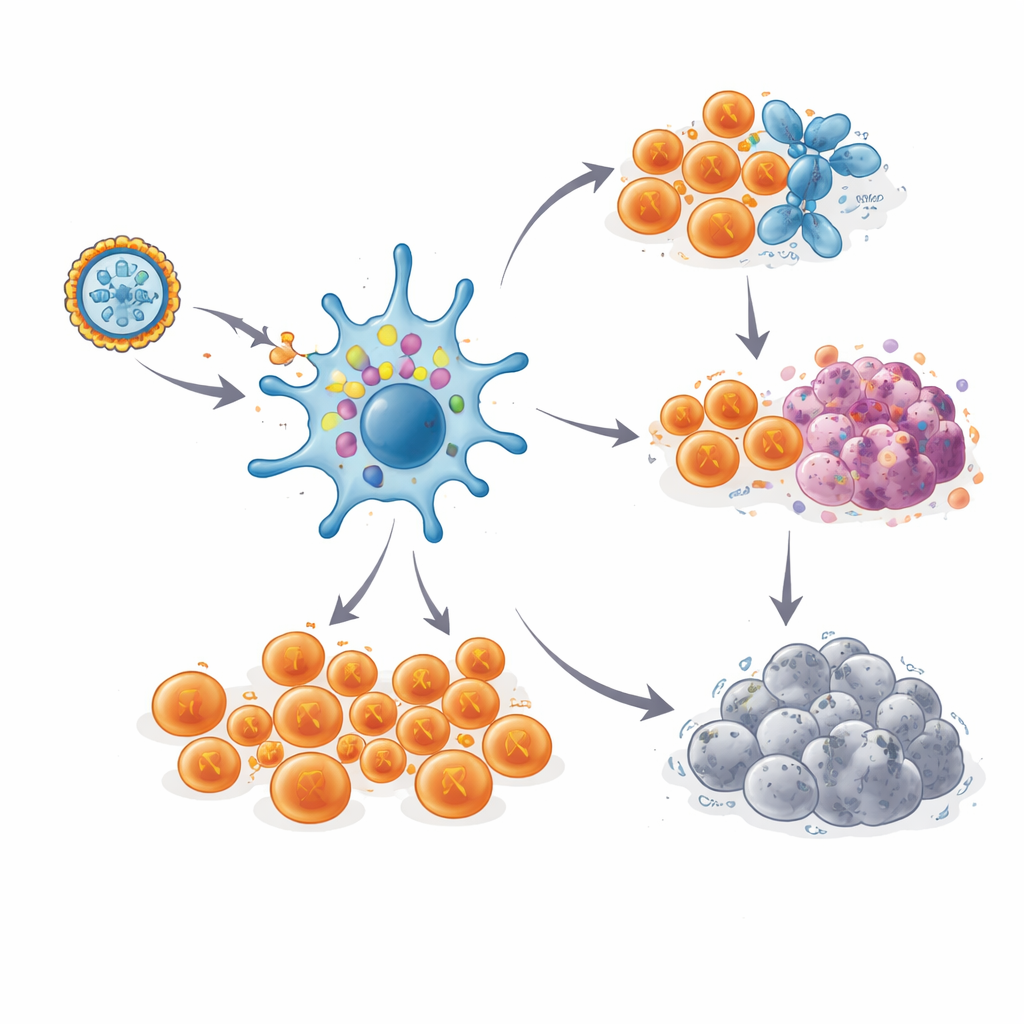
Долговременная иммунная память
Важно, что эти Т‑клеточные ответы не угасали быстро. У большинства пациенток сильные ответы достигали пика в период вакцинации, незначительно снижались, а затем сохранялись на высоком уровне от одного до трёх с половиной лет, даже без бустерных прививок. Отслеживая уникальные «штрихкоды» рецепторов отдельных Т‑клеточных клонов, учёные могли наблюдать конкретные неоантиген‑реактивные клетки до шести лет у одной пациентки, которая оставалась без рецидива. Детальные анализы на уровне одиночных клеток показали два основных пути судьбы этих клеток. Многие превратились в сильно вооружённые киллер‑Т‑клетки, готовые уничтожить любую клетку с соответствующим неоантигеном. Другие развились в более редкий стволоподобный пул памяти с маркёрами самовоспроизведения, что указывает на резервуар, способный генерировать новые волны защитников при повторном появлении раковых клеток.
Что произошло с пациентками
После медианы наблюдения чуть более пяти лет от первой дозы вакцины у одиннадцати из четырнадцати женщин не было зарегистрировано возврата рака; одна из этих пациенток умерла от причин, не связанных с онкологией, оставаясь в ремиссии. У трёх женщин имелся рецидив, и их случаи дают подсказки, почему индивидуальная вакцина иногда может не сработать. Одна пациентка сформировала только слабый Т‑клеточный ответ и позже получила пользу от другой иммунотерапии — антитела против PD‑1, прежде чем в конечном итоге погибла от распространённого заболевания. У второй была наследственная предрасположенность и опухоли в обеих молочных железах; для разработки вакцины использовали только одну опухоль, и вскоре стало ясно, что рецидив произошёл из генетически отличной, невакцинированной опухоли. Третья пациентка имела сильные вакцина‑индуцированные Т‑клетки, которые инфильтрировали рецидивную опухоль, но раковые клетки во многом утратили ключевые молекулы, необходимые для показа неоантигенов на своей поверхности, фактически скрывшись от иммунной атаки.
Почему эта работа важна для будущего
Это пилотное исследование было небольшим и не имело контрольной группы, поэтому оно не может доказать, что только вакцина предотвратила рецидивы. Тем не менее оно демонстрирует, что создание сложной индивидуальной мРНК‑вакцины на основе опухоли пациентки осуществимо в обычных больничных условиях, в целом переносится хорошо и может вызвать мощные, длительно сохраняющиеся Т‑клеточные армии против множества опухолево‑специфических мишеней. Результаты также выявляют пути побега, которые могут использовать опухоли — например утрату механизма представления антигенов или возникновение из невключённых в дизайн очагов — указывая на необходимость комбинаций с другими иммунными методами и более широкого секвенирования опухолей. Для пациентов с тройным негативным раком молочной железы эта работа подразумевает, что индивидуальная вакцина, применённая после стандартного лечения, однажды может помочь предотвратить возвращение болезни, превратив собственную иммунную систему в долговременную, высокоспецифичную линию защиты.
Цитирование: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Ключевые слова: тройной негативный рак молочной железы, мРНК‑вакцины против рака, неоантигенная иммунотерапия, Т‑клеточный иммунитет, рецидив опухоли