Clear Sky Science · ru
Лиганда‑специфические траектории активации определяют сигнальную активность GPCR в клетках
Как один рецептор может вести себя как множество переключателей
Многие современные лекарства действуют на обширное семейство белков на поверхности клеток, называемых G‑белок‑связанными рецепторами, или GPCR. Эти рецепторы влияют на частоту сердцебиения, настроение, дыхание и множество других функций организма. Долгое время их рассматривали как простые выключатели: препарат связывается — выключатель включается — и сигнал проходит внутрь клетки. В этой работе показано, что реальность гораздо богаче. С помощью нового типа флуоресцентного «шпиона», встроенного непосредственно в рецептор, авторы в живых клетках наблюдали, как разные препараты направляют один и тот же рецептор по разным путям активации — словно выбирая разные маршруты по городу — приводя к различным схемам сигнализации. Понимание этих скрытых маршрутов может помочь в разработке лекарств, дающих желаемый эффект и уменьшающих побочные действия.
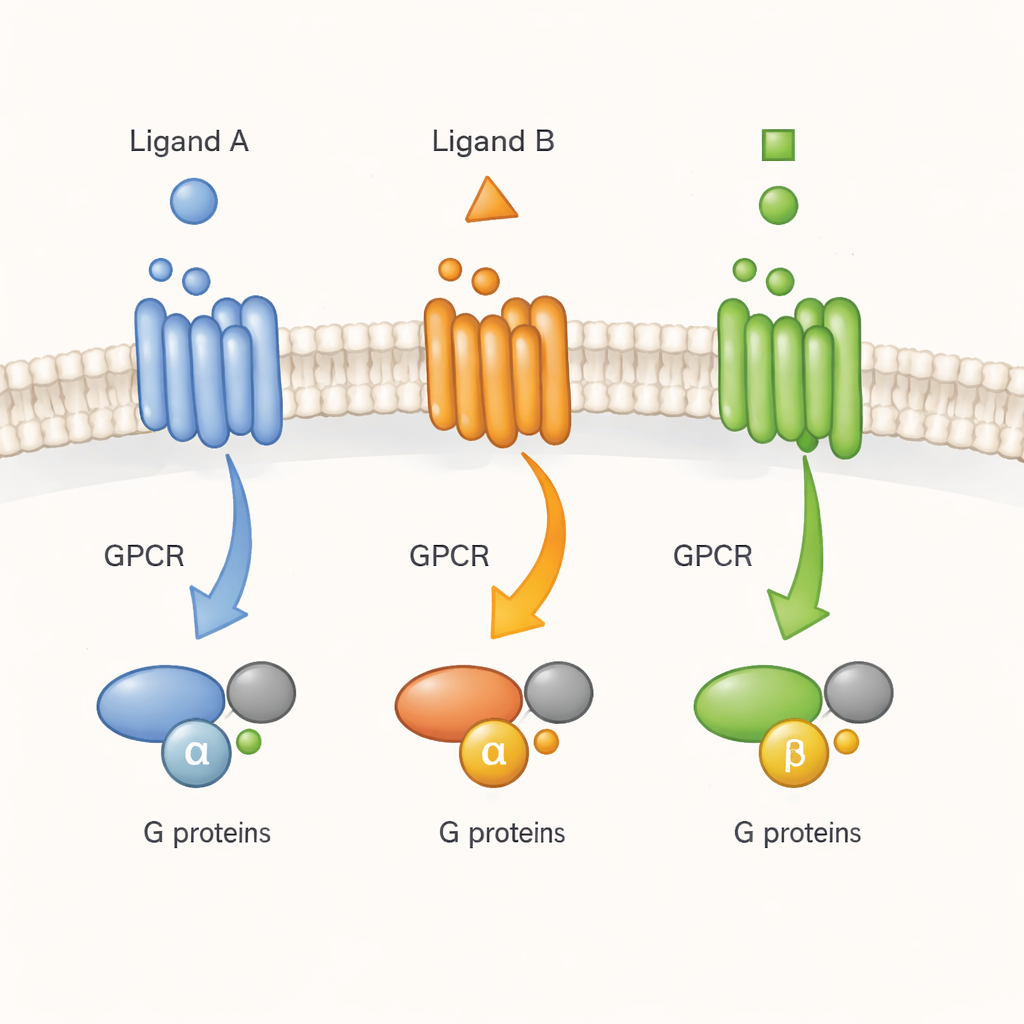
Наблюдая «дверной звонок» клетки в реальном времени
GPCR часто сравнивают с молекулярными дверными звонками: сигнальная молекула (лиганд) звонит снаружи, а рецептор передаёт сообщение G‑белкам внутри клетки. Ранние исследования очищенных рецепторов в детергентах предполагали, что GPCR не просто переключаются между одной неактивной и одной активной формой. Вместо этого они перебирают множество конформаций, которые лекарства стабилизируют в разной степени. Но оставалось неясным, сохраняется ли такая сложность в плотной и динамичной среде живой клетки. Здесь авторы сосредоточились на одном представительном рецепторе — M2 мускариновом ацетилхолиновом рецепторе, важном регуляторе сердечной и нервной активности — и проверили, приводят ли разные лиганды к возникновению различных активных форм, которые имеют значение для реальной клеточной сигнализации.
Создание крошечных световых индикаторов на поверхности рецептора
Чтобы отслеживать движения рецептора, не нарушая его нормальной функции, команда использовала расширение генетического кода — технологию, позволяющую встраивать специально разработанную аминокислоту в выбранные позиции на внешней поверхности рецептора. Этот химический «якорь» можно «пришпинить» к малому флуоресцентному красителю в живых клетках. Просканировав 72 позиции и оставив только те, которые по‑прежнему вели себя как нормальные рецепторы, они создали панель из семи вариантов M2‑рецептора, каждый с одним красителем в разной наружной петле. При добавлении естественного медиатора ацетилхолина яркость красителя в этих точках повышалась или снижалась по характерным схемам, раскрывая, как каждая часть внешней поверхности рецептора смещалась в начале сигнализации. Важно, что эти меченные рецепторы всё ещё могли активировать G‑белки и подвергаться обычной внутреклеточной эндоцитозной переработке, что показывает: индикаторы были достоверными, а не разрушительными.
Препараты оставляют характерные «конформационные отпечатки»
Затем исследователи сравнили несколько веществ, которые всё включают M2‑рецептор, но с разной силой: собственный ацетилхолин, сверхмощный синтетический агонист ипероксo и два более слабых частичных агониста — ареколин и пилокарпин. Каждый препарат вызывал уникальную картину изменений флуоресценции по семи репортёрным позициям — конформационный отпечаток. В большинстве позиций размер смещения коррелировал с тем, насколько сильно препарат активировал рецептор. Однако в двух позициях связь была инверсной: слабые препараты вызывали наибольшие изменения, тогда как сильнейший препарат почти не давал ответа. Такое поведение невозможно объяснить наличием единственной активной состояния. Скорее, это указывает на то, что один и тот же рецептор в живых клетках может принимать несколько разных активных форм, одни из которых предпочитают мощные препараты, другие — слабые.
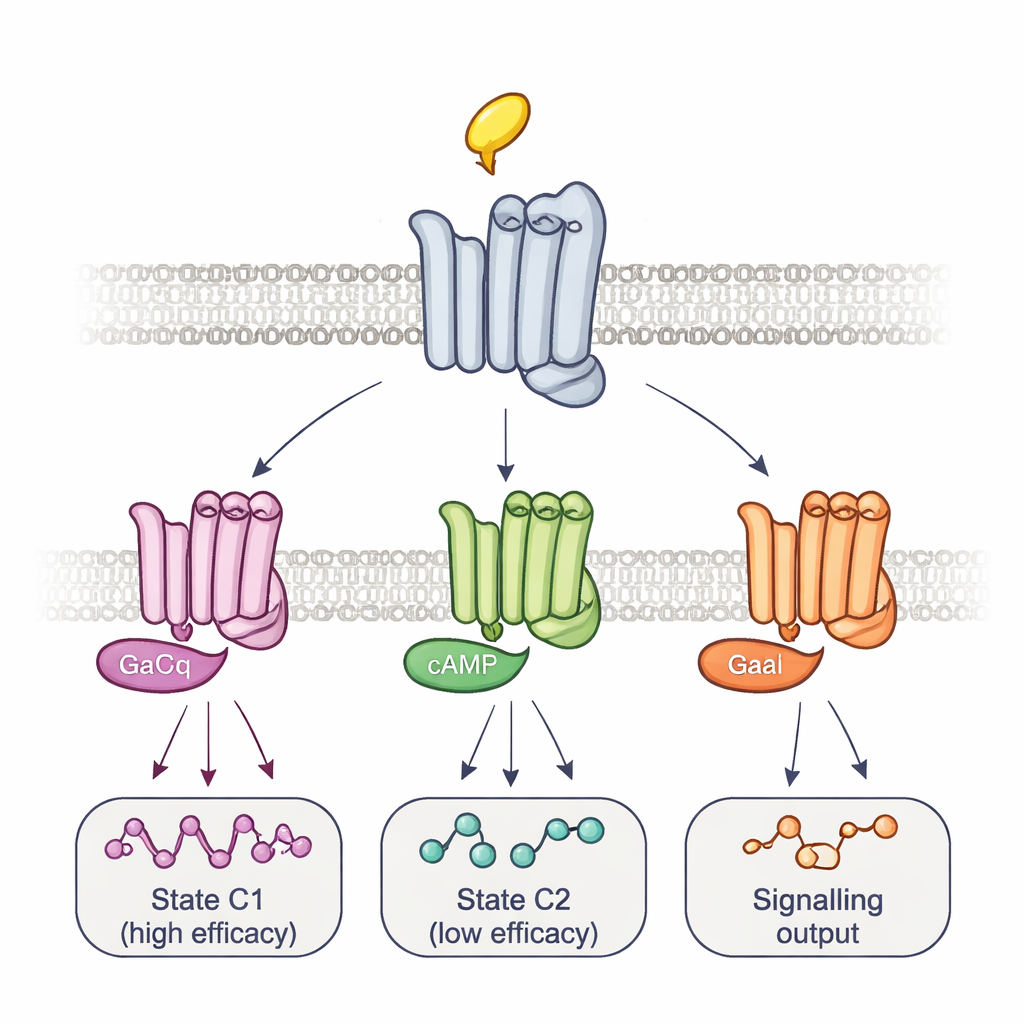
Множественные комплексы и временные маршруты к сигнализации
Чтобы связать эти конформации с реальной сигнализацией, команда изменила сами G‑белки. Переэкспрессия мутантного G‑белка, который формирует очень прочные и долгоживущие комплексы с рецепторами, избирательно стирала сигнал с некоторых репортёрных позиций и усиливала другой. Эта картина в сочетании с временными характеристиками изменений флуоресценции выявила по крайней мере два основных комплекса рецептор–G‑белок: быстро формирующийся высокоэффективный комплекс и более медленный низкоэффективный. Различные препараты смещали баланс между этими комплексами и даже использовали разные промежуточные шаги, прокладывая лиганда‑специфические траектории активации. С помощью отдельного биолюминесцентного анализа, отслеживающего панель из 14 подтипов G‑белков, авторы показали, что эти равновесия определяют не только силу общей активации сигнализации препаратом, но и то, какие именно G‑белки включаются. Например, ареколин преимущественно активировал определённые белки Go, тогда как пилокарпин сильно смещал предпочтение в сторону низкоэффективного комплекса.
Почему это важно для лучших лекарств
Для неспециалистов главный вывод в том, что один рецептор — это не просто один переключатель, а совокупность родственных переключателей, каждый из которых достижим разными путями и связан с чуть различными последующими эффектами. Это исследование даёт прямое представление о таких путях и состояниях в целых клетках, а не в упрощённых пробирочных системах. Картируя, как конкретные препараты смещают рецептор в сторону определённых комплексов и партнёров по G‑белкам, исследователи получают чертёж для создания «умных» лекарств — соединений, которые подталкивают рецепторы в состояния, запускающие полезные сигналы и избегают тех, что связаны с побочными эффектами. Разработанная здесь стратегия флуоресцентных биосенсоров должна быть адаптируема к многим другим рецепторам, открывая окно в хореографию действия лекарств в живых клетках в реальном времени.
Цитирование: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Ключевые слова: GPCR-сигналы, эффективность лиганда, G‑белки, конформационные биосенсоры, поиск лекарств