Clear Sky Science · ru
Индукция пластичности Т‑клеток микробиотой обеспечивает иммунный контроль опухоли
Как дружелюбные кишечные микробы могут помочь в борьбе с раком
Имунотерапия рака революционизировала лечение многих пациентов, но лишь у части опухоли уменьшаются и не возвращаются. В этом исследовании поставлен на первый взгляд простой вопрос с большими последствиями: могут ли конкретные кишечные бактерии «наставлять» иммунные клетки так, чтобы препараты, блокирующие контрольные точки, например анти–PD‑1‑терапия, работали лучше? Проследив путь иммунных клеток от тонкой кишки до опухолей у мышей, авторы обнаружили прямую, проверяемую связь между одним кишечным микробом и успешным контролем опухоли.
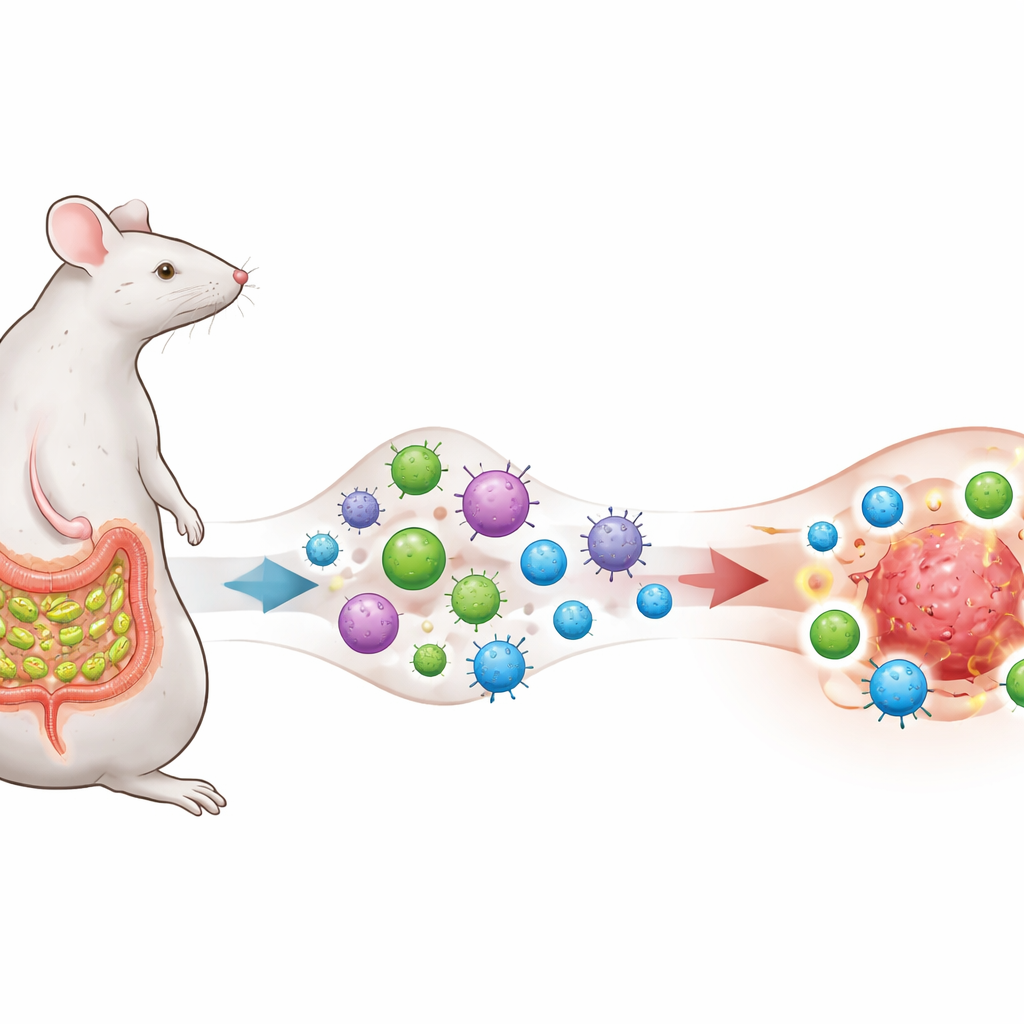
Микроб, который обучает иммунную систему
Исследователи сосредоточились на бактерии кишечника, называемой сегментированной филаментарной бактерией (SFB), известной тем, что живёт близко к эпителию тонкой кишки у мышей и вызывает сильный, но обычно гомеостатический ответ Т‑хелперов 17 (TH17). Они модифицировали клетки меланомы, лёгких и кишки так, чтобы они экспонировали фрагмент белка, также встречающийся в SFB, создав намеренное «совпадение антигена» между микробом и опухолями. Мышей либо оставляли лишёнными SFB, либо колонизировали ею, и всем вводили анти–PD‑1 — широко используемое антитело, блокирующее контрольные точки и нацеленное на «снятие тормозов» с Т‑клеток.
Кишечные обученные клетки превращают опухоли из холодных в горячие
Одна только терапия анти–PD‑1 или одна только колонизация SFB мало влияют на рост опухоли. Но когда опухоли несут антиген, происходящий от SFB, и мыши колонизованы SFB, анти–PD‑1 внезапно становится очень эффективным: опухоли уменьшаются, выживаемость улучшается, а выжившие животные отказываются от повторно введённой опухоли без дополнительной терапии, что свидетельствует о стойкой иммунной памяти. У этих успешных мышей опухоли наполняются агрессивными CD8 «киллерными» Т‑клетками, продуцирующими интерферон‑γ и другие цитотоксические молекулы, тогда как доля супрессивных регуляторных Т‑клеток снижается. Иными словами, локальная среда вокруг рака перестраивается из относительно «холодной» и неответной в «горячую» и воспалённую.
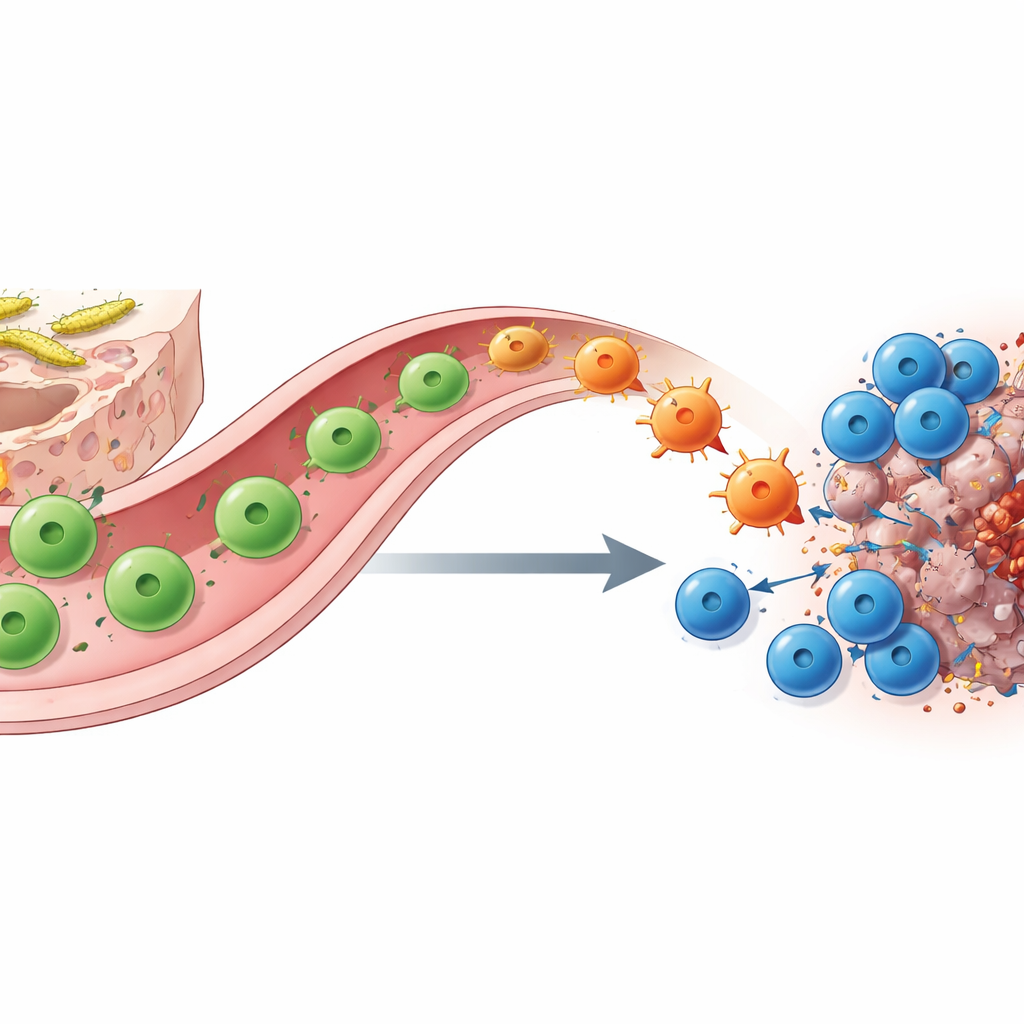
Помогающие Т‑клетки‑трансформеры связывают кишечник и опухоль
Как колонизация SFB вызывает эту перестройку? С помощью молекулярного штрихкода, секвенирования одиночных клеток и хитрого генетического трайсинга авторы показывают, что ключевыми действующими лицами являются SFB‑специфичные CD4‑хелперы. В тонкой кишке эти клетки изначально представлены как TH17, которые поддерживают барьерную функцию и обычно вырабатывают молекулу IL‑17A. Когда при блокаде контрольных точек они встречают совпадающий антиген в опухоли, они мигрируют из кишечника в опухолевую нишу и «переспециализируются» в клетки типа TH1, которые вместо этого секретируют большие количества интерферона‑γ и TNF. Эти преобразованные «бывшие TH17» усиливают представление антигенов и выделяют хемокины, привлекая и активируя CD8‑киллеры. Удаление либо хелперных, либо киллерных Т‑клеток, либо генетическое удаление клеток происхождения линии IL‑17A, служащих предшественниками, в значительной мере лишает анти–PD‑1 пользы, подчёркивая их партнёрство.
Не все микробы дают полезные инструкции
Чтобы проверить, подойдёт ли любой кишечный микроб с совпадающими антигенами, команда повторила эксперимент с другим комменсалом, Helicobacter hepaticus. Этот организм тоже вызывает сильные Т‑клеточные ответы, но преимущественно расширяет регуляторные клетки, которые подавляют воспаление. Когда опухоли модифицировали для экспрессии антигена H. hepaticus и мышей колонизировали этой бактерией, анти–PD‑1 терапия не дала улучшения. Хотя многие H. hepaticus‑специфичные хелперы мигрировали в опухоль, они сохраняли регуляторный характер и мало продуцировали интерферон‑γ, не сумев активировать киллерные Т‑клетки. Это противопоставление показывает, что качество и пластичность индуцированных микробиотой Т‑клеточных программ — а не только совпадение антигена — определяют, будет ли микробиота помогать или мешать раковой иммунотерапии.
Что это может значить для будущей онкологической помощи
В целом работа даёт прямое доказательство на животных, что определённая кишечная бактерия может заранее натренировать хелперные Т‑клетки в кишечнике, послать их в опухоли с общими антигенами и, при условии блокады контрольных точек, заставить их сменить роль и стать мощными антиопухолевыми клетками. Прояснив этот путь «кишечник‑→‑опухоль», исследование предполагает, что тщательно подобранные или инженерные микробы однажды могут использоваться вместе с иммунотерапией, чтобы превращать опухоли большего числа пациентов в поддающиеся лечению, воспалённые мишени — при условии, что эти микробы индуцируют нужный тип гибкого, провоспалительного Т‑клеточного ответа, а не успокаивающий регуляторный эффект.
Цитирование: Najar, T.A., Hao, Y., Hao, Y. et al. Microbiota-induced T cell plasticity enables immune-mediated tumour control. Nature 651, 201–210 (2026). https://doi.org/10.1038/s41586-025-09913-z
Ключевые слова: микробиота кишечника, раковая иммунотерапия, пластичность Т‑клеток, блокада контрольных точек, опухолевая микроокружение