Clear Sky Science · ru
Стресс контролирует наследование гетерохроматина через убиквитинирование гистона H3
Как клетки «помнят» стресс
Нашим клеткам нужны механизмы для «запоминания» прошлых стрессов — таких как высокая температура, нехватка питательных веществ или воздействие препаратов — чтобы при следующей встрече реагировать быстрее. Одной из мощных систем памяти является гетерохроматин: плотно упакованная ДНК, которая сохраняет определённые гены выключенными на протяжении многих делений клеток. В этой статье изучается, как клетки активно настраивают эту память в ответ на стресс, раскрывая молекулярный узел, который связывает внешние сигналы с долговременными изменениями активности генов. Понимание этой системы контроля может помочь объяснить, как грибы приобретают устойчивость к лекарствам, и как стресс перестраивает эпигенетический ландшафт наших собственных клеток.
Замок на геноме
Гетерохроматин можно представить как молекулярный замок на участках ДНК, который удерживает соседние гены в неактивном состоянии. Этот замок строится из химических меток на гистоновых белках, в частности метки H3K9me3. После установки она может копироваться каждый раз при репликации ДНК, позволяя шаблонам репрессии генов наследоваться без изменения самой последовательности ДНК. До сих пор большинство работ предполагало, что такое самокопирование в основном опирается на петлю «чтение‑запись»: ферментный комплекс распознаёт существующие метки H3K9me3 и наносит ту же метку на соседние гистоны, постепенно распространяя молчаливую область. Но эта модель не объясняла в полной мере, как условия окружающей среды ускоряют, замедляют или перенаправляют распространение гетерохроматина.
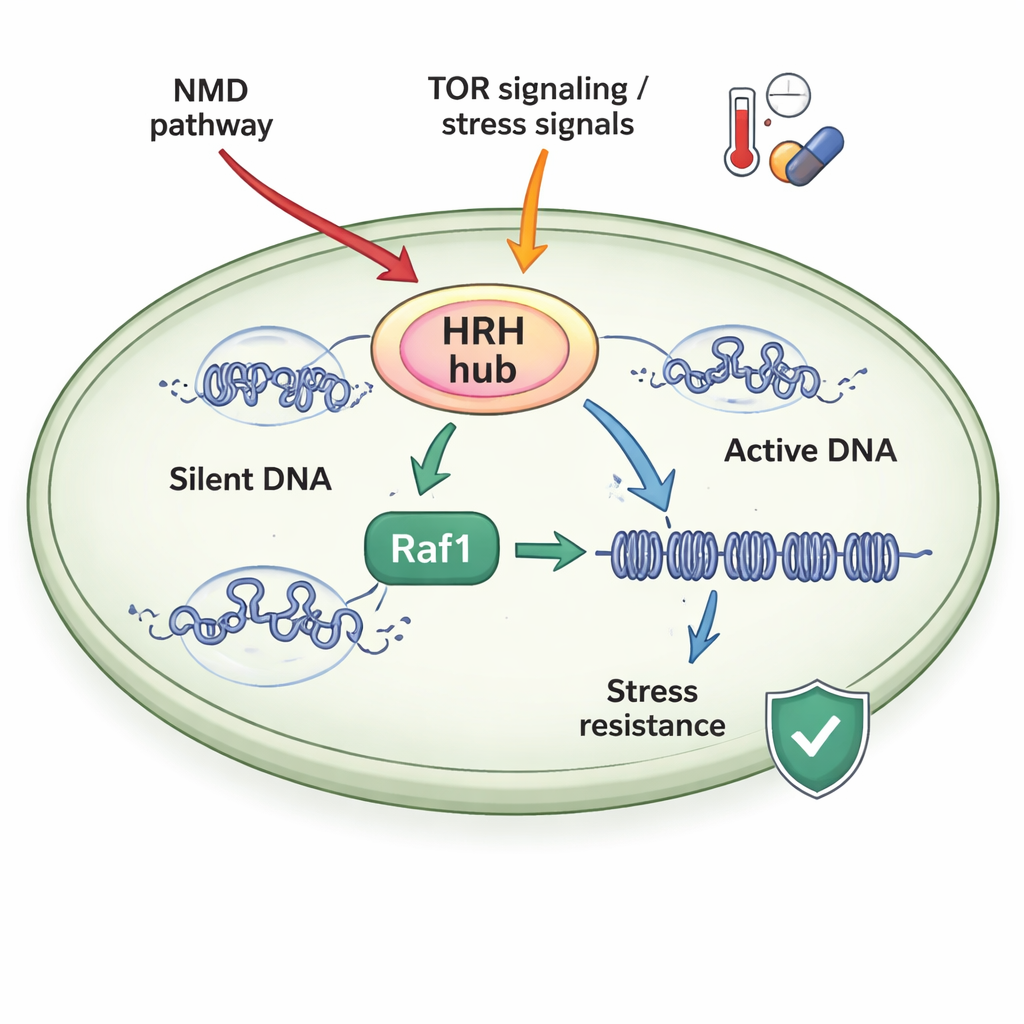
Чувствительный к стрессу центр управления
Авторы изучали делящуюся дрожжеподобную дрожжевую модель (fission yeast), простую модельную систему, чья хроматиновая машина близка к таковой у высших организмов. Они сосредоточились на комплексе ClrC, который как наносит метку H3K9me3, так и присоединяет небольшой белок убиквитин к другой позиции на гистоне H3 (H3K14ub). Ключевой субъединицей ClrC является Raf1, выступающая в роли лимитирующего «шлюзового стража»: при недостатке Raf1 большая часть основного фермента (Clr4) остаётся свободной вместо того, чтобы входить в комплекс на хроматине, и молчаливые домены не распространяются. При избытке Raf1 больше ClrC собирается и стабильно связывается с ДНК, что позволяет меткам H3K14ub и H3K9me3 простираться вдоль хромосом и усиливать подавление генов.
Тонкая настройка замка с помощью убиквитина
Картируя хроматиновые метки по всему геному, исследователи показали, что H3K14ub сильно обогащён в местах формирования гетерохроматина и фактически исчезает при удалении Raf1. Когда в клетках присутствует мутация, блокирующая шаг присоединения убиквитина (при сохранении H3K9me3 в исходной точке), молчаливые домены не в состоянии распространяться наружу. Иными словами, H3K14ub — не просто декоративная метка; она необходима для продвижения фронта гетерохроматина. Биохимические и визуализационные эксперименты объясняют причину: H3K14ub значительно повышает активность фермента Clr4 и помогает удерживать весь комплекс на хроматине, повышая локальную плотность H3K9me3 выше порога, необходимого для стабильного наследования. Примечательно, что увеличение уровня Raf1 может компенсировать несколько других факторов, обычно требующихся для поддержания этих молчаливых доменов, что подчёркивает центральную роль управляемого Raf1 убиквитинирования.
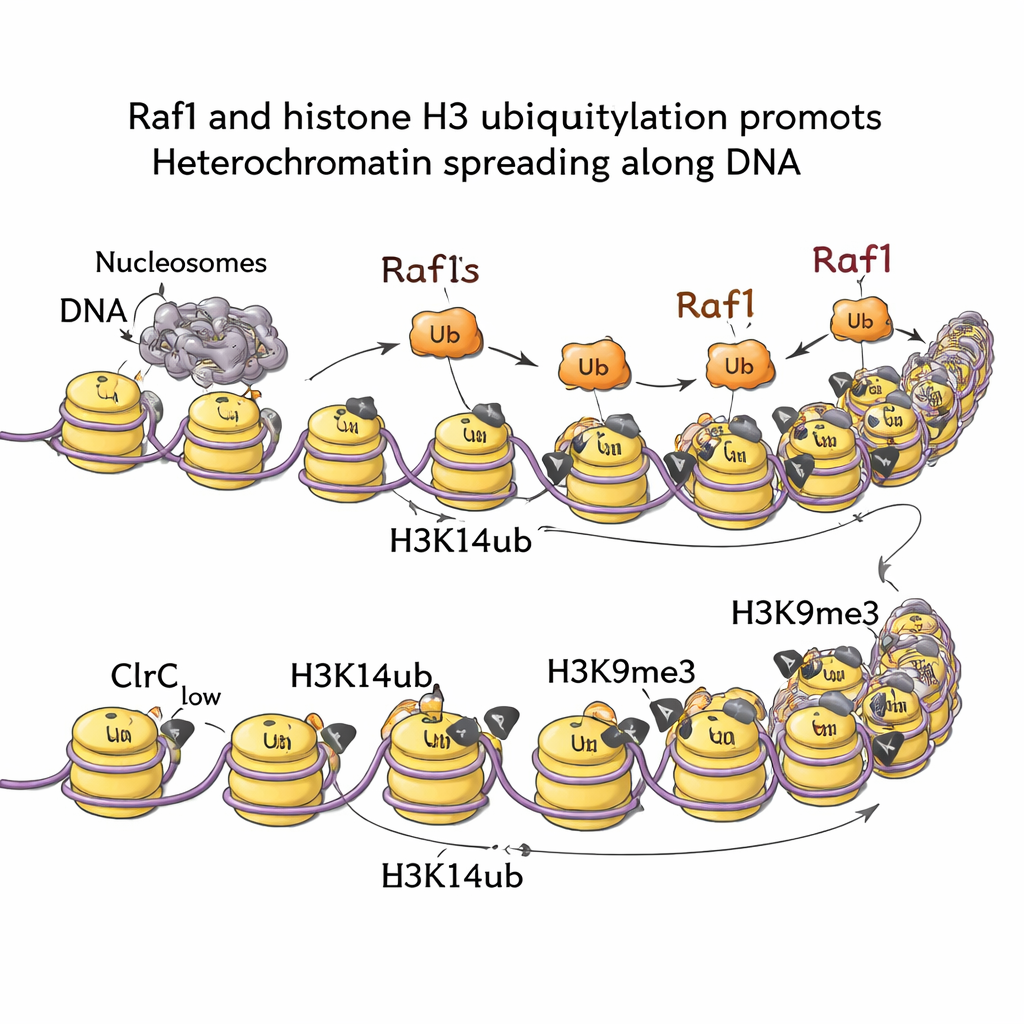
Сигналы от путей деградации РНК и регуляции роста
Клетки не оставляют уровень Raf1 на волю случая. Исследование показывает, что два основных стресс‑чувствительных пути влияют на то, что авторы называют регуляторным узлом наследуемости гетерохроматина (HRH), центром которого является Raf1. Во‑первых, путь NMD (nonsense‑mediated decay), известный разрушением дефектных мРНК, нацелен на материнскую РНК, кодирующую Raf1, удерживая уровни Raf1 низкими в нормальных условиях. Отключение NMD стабилизирует Raf1‑РНК, повышает содержание белка Raf1 и восстанавливает распространение гетерохроматина у мутантов, которые иначе не могут поддерживать молчаливые домены. Во‑вторых, сенсор роста и стресса TORC2, действующий через киназу Gad8, стимулирует экспрессию Raf1. Высокая температура выключает этот путь, снижает уровни Raf1, ослабляет гетерохроматин и усложняет поддержание молчаливых состояний, если только Raf1 не повысить экспериментально.
Стресс, лекарственная устойчивость и более широкие последствия
Далее авторы связывают этот молекулярный узел с реальными адаптациями. Воздействие кофеина — стресса, который также известен подавлением NMD в других системах — повышает уровень Raf1 и усиливает распространение гетерохроматина на новые участки, включая гены, чья инактивация даёт устойчивость к кофеину и противогрибковым препаратам. Аналогично, клетки с искусственно повышенным Raf1 становятся более устойчивыми к флуконазолу и клотримазолу, распространённым противогрибковым средствам. И, наоборот, при снижении Raf1 — из‑за тепла или потери сигнального пути TORC2–Gad8 — гетерохроматин становится нестабильным и эпигенетическая память ослабевает, если Raf1 не восстановить. Поскольку белки, подобные Raf1, комплекс ClrC и метка H3K14ub имеют аналоги у патогенных грибов и у млекопитающих, эти результаты указывают на то, что похожий стресс‑чувствительный эпигенетический узел может формировать лекарственную устойчивость, развитие и заболевания во многих видах.
Почему это важно
В практическом смысле эта работа показывает, что угнетение генов хроматином — не жёсткий замок, а умная, настраиваемая система. Клетки используют центральный узел для считывания сигналов окружения — изменения температуры, состояние питательных веществ, химические стрессы — и регулируют уровень Raf1 вверх или вниз. Это, в свою очередь, определяет, какая часть генома будет окутана долговременным молчанием и как легко клетки могут «перепрограммировать» себя без мутаций в ДНК. Открыв ключевую роль убиквитинирования гистона H3 и дозировки Raf1 в этом процессе, исследование даёт схему того, как стресс быстро перестраивает эпигенетический ландшафт, и намекает на новые подходы к влиянию на лекарственную устойчивость грибов или патологическое подавление генов у человека.
Цитирование: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Ключевые слова: гетерохроматин, эпигенетическое наследование, убиквитинирование гистонов, адаптация к стрессу, устойчивость грибов к лекарствам