Clear Sky Science · ru
Биомиметические везикулы, созданные из модифицированных опухолевых клеток, действуют как персонализированные вакцины для послеоперационной иммуннотерапии рака
Превращение опухолевых остатков в резервную линию защиты
Для многих пациентов с солидными опухолями операция — лишь первый раунд долгой борьбы. Даже если большую часть опухоли удалили, мелкие скопления раковых клеток могут ускользнуть и со временем дать смертельные метастазы. В этом исследовании рассматривается изобретательный способ превратить собственные опухолевые клетки пациента в персонализированную вакцину, нацеленную на обнаружение этих остатков после операции и помогающую иммунной системе не допустить возвращения рака.
Почему удалить оставшиеся раковые клетки так трудно
Стандартные методы испытывают трудности с клетками, которые остаются после удаления основной опухолевой массы. Эти рассеянные клетки часто прячутся в отдалённых органах и защищены от действия лекарств и иммунной атаки. Существующие иммунные вакцины пытаются обучить организм распознавать опухолевые маркеры с помощью специализированных иммунных клеток — дендритных клеток, — но эти «живые» вакцины трудно производить, они плохо мигрируют в ключевые иммунные органы и в клинике показывают скромные преимущества. Главная проблема в том, что у каждого пациента опухоль несёт уникальный набор мутаций, поэтому универсальные вакцины обычно пропускают важные цели.
Скрытый переключатель, делающий раковые клетки более заметными
Исследователи начали с поиска естественных переключателей в иммунной системе, которые делают клетки лучше в демонстрации своего внутреннего содержимого иммунным стражам. Они сосредоточились на белке под названием синтаксин 11, обычно обильном в иммунных клетках, но скудном во многих опухолях. Повысив уровень этого белка в агрессивных клетках рака молочной железы в мышиных моделях, учёные обнаружили, что раковые клетки начали вести себя больше как профессиональные иммунные «сторожевые»: на их поверхности вырос уровень молекулярных «именных табличек» и сигнальных молекул-помощников. По сути, опухолевые клетки перепрограммировались так, чтобы раскрывать свои уникальные черты иммунной системе, а не прятать их.
Создание крошечных имитаций иммунных вестников
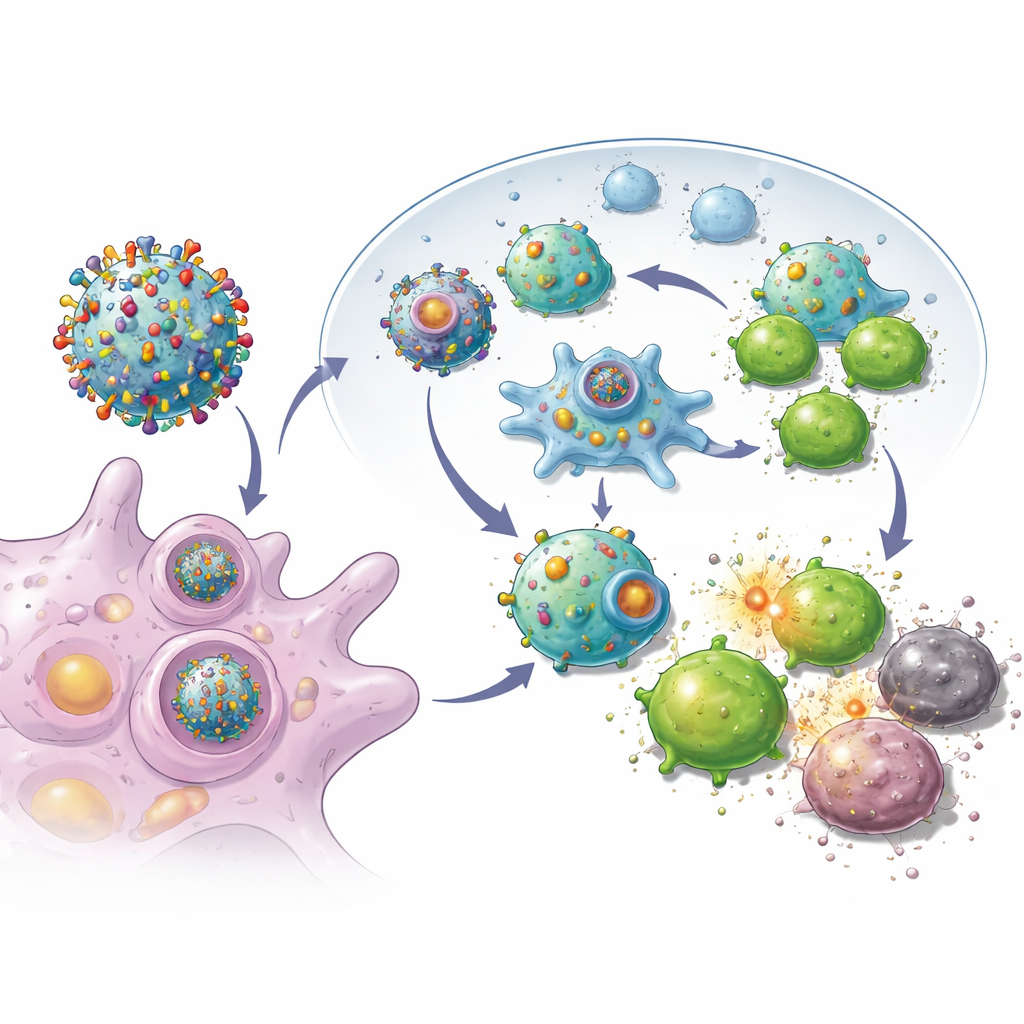
Вооружившись этими перепрограммированными опухолевыми клетками, команда сняла с них внешние мембраны и использовала их для покрытия биоразлагаемых наночастиц, загруженных небольшим иммуномодулирующим препаратом. В результате получилась стайка нанообразных пузырьков, каждый из которых нес полный набор маркеров данной опухоли плюс встроенные «сигналы отправки» для убивающих Т-клеток. При подкожной инъекции мышам после операции эти везикулы эффективно мигрировали в ближайшие лимфатические узлы, где происходит обучение иммунных клеток. Там они могли напрямую взаимодействовать с киллерными Т-клетками и поглощаться естественными иммунными сторожами, которые в свою очередь усиливали ответ. Эксперименты показали, что Т-клетки, подвергшиеся воздействию этих везикул, размножались более интенсивно и лучше уничтожали раковые клетки, чем те, которые были подготовлены более простыми нанодизайнами.
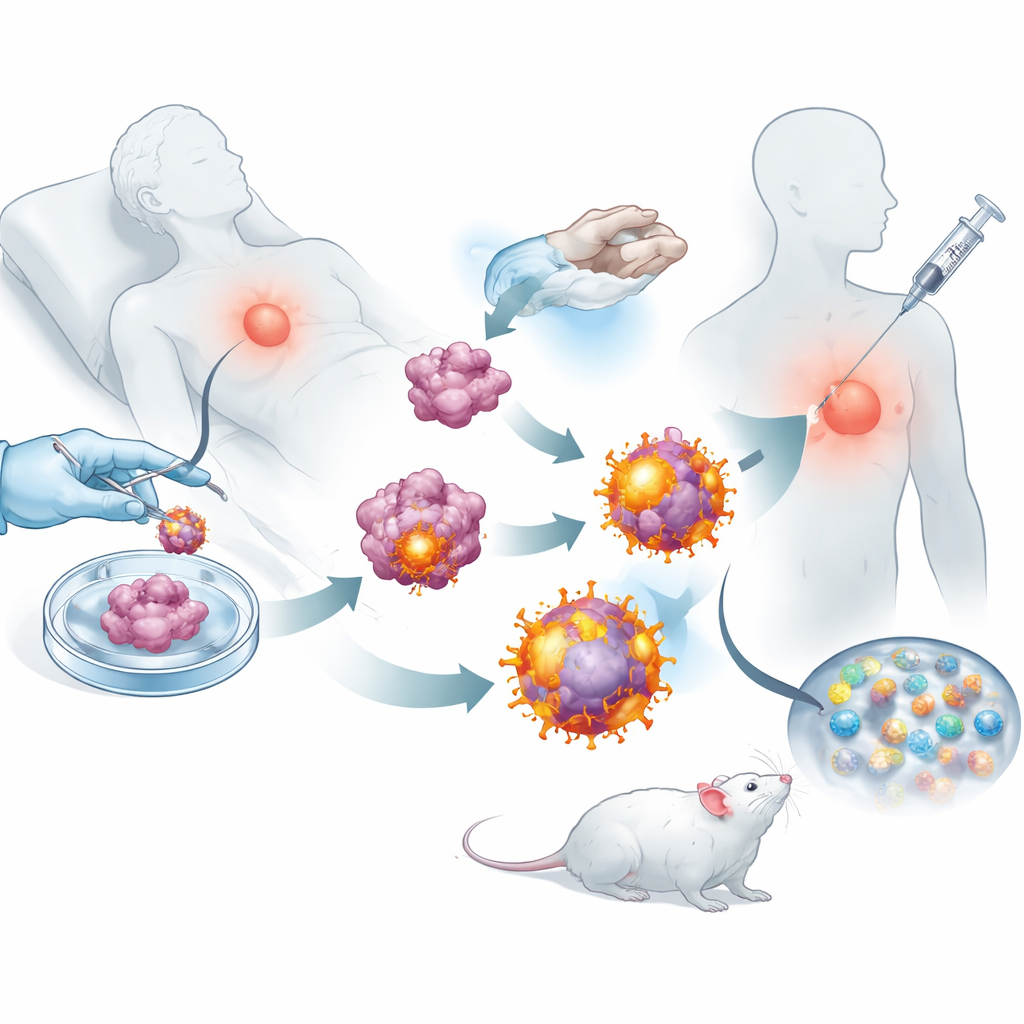
Держать рак под контролем после операции
Используя несколько мышиных моделей рака молочной железы и меланомы, исследователи проверили, может ли эта таргетированная вакцина действительно изменить ход болезни. У животных, у которых большую часть опухоли молочной железы удалили хирургически, вакцинированные мыши развивали меньшие рецидивы и значительно меньше метастазов в лёгких по сравнению с нелечеными животными. В лимфатических узлах, селезёнке и опухолях обработанных мышей наблюдалось много активных киллерных Т-клеток и долгоживущих клеток памяти, что говорит о том, что иммунная система была как пробуждена, так и обучена на длительный срок. В сочетании с одобренным антителом-блокатором контрольных точек, которое не даёт опухолям парализовать Т-клетки, вакцина обеспечивала стойкий контроль над опухолью и у многих мышей приводила к полной регрессии и длительному выживанию.
Ускорение персонализированного лечения
Одно из препятствий на пути превращения этой концепции в терапию для клиники — время: генетические методы перепрограммирования опухолевых клеток могут быть медленными. Чтобы решить эту проблему, команда проверила природные соединения и обнаружила деоксиподофиллотоксин, небольшую молекулу, которая быстро повышает уровень ключевого переключательного белка и те же иммуностимулирующие поверхностные маркеры. Используя этот обходной путь, они собрали схожие наночастицы, покрытые везикулярной оболочкой, за меньшее время, сохранив при этом способность вызывать мощные опухлеспецифические иммунные ответы. Испытания показали, что вакцины, изготовленные с помощью этого препарата, были столь же эффективны, как и полученные генетическим методом, и их эффективность зависела от распознавания правильного типа опухоли, а не от какого-либо общего отравляющего воздействия на раковые клетки.
Что это может означать для будущей онкопомощи
Для неспециалиста ключевая мысль такова: собственную опухоль пациента можно переработать в миниатюрный тренажёр для иммунной системы. Превращая раковые клетки в источники богатой персонализированной информации и упаковывая эту информацию на прочные наноносители, этот подход нацелен на то, чтобы «подмести» клетки, которые остаются после операции, и предотвратить формирование новых очагов. Хотя до того, как такие вакцины смогут регулярно предлагаться людям, предстоит ещё много этапов — включая доказательство безопасности и эффективности на людских опухолях и создание надёжных производственных цепочек, — эта работа наметила путь к высоко индивидуализированным послеоперационным методам лечения, которые привлекают защитные силы организма, чтобы довести начатое хирургом до конца.
Цитирование: Yu, P., Jin, Z., Meng, L. et al. Biomimetic vesicles engineered from modified tumour cells act as personalized vaccines for post-surgical cancer immunotherapy. Nat. Nanotechnol. 21, 443–454 (2026). https://doi.org/10.1038/s41565-025-02113-w
Ключевые слова: вакцина от рака, иммуннотерапия, наномедицина, послеоперационное лечение, персонализированная онкология