Clear Sky Science · ru
Определение целостности структуры ДНК-оригами и фармакокинетики in vivo
Наблюдение за крошечными ДНК-машинами внутри организма
ДНК можно складывать как бумагу в крошечные трёхмерные формы — это техника, известная как ДНК-оригами. Эти наноструктуры можно запрограммировать на перенос лекарств, вакцин или сигнальных молекул с выдающейся точностью. Но после введения в организм сохраняются ли они достаточно долго, чтобы сработать, или быстро распадаются? В этой статье представлена новая методика наблюдения за такими ДНК-машинами в действии в живых животных, которая показывает, как долго они выживают, как перемещаются по кровотоку и даже какие участки каждой структуры разрушаются первыми.
Почему складывание ДНК может изменить медицину
ДНК-оригами использует те же правила спаривания оснований, что и хранение нашей генетической информации, но перенаправляет их на построение наноскопических объектов. Исследователи могут располагать на этих объектах белки, лекарства или иммуностимулирующие сигналы как штыри на пластине Lego, создавая строго контролируемые терапии против рака, аутоиммунных заболеваний и инфекций. Для того чтобы такие прецизионные препараты были безопасными и эффективными, регуляторы и учёные должны знать, насколько целыми эти структуры остаются в организме и как быстро они выводятся — вместе это известно как их фармакокинетика. Существующие методы отслеживания обычно присоединяют флуоресцентные красители или просто подсчитывают фрагменты ДНК, что может заставить распавшийся мусор выглядеть как полностью интактные наноструктуры. До сих пор не существовало практического способа сказать, в живом животном, остаются ли исходные формы ДНК-оригами действительно целыми.
Молекулярный «тест целостности» для ДНК-оригами
Команда разработала метод, который назвала PLASTIQ — сокращение от proximity ligation assay for structural tracking and integrity quantification (приборная лигазная проба для отслеживания структуры и количественной оценки целостности). Ключевая идея — позволить самой ДНК-оригами докладывать о своём состоянии. В определённых позициях каждой структуры исследователи размещают пары коротких «степлов» ДНК, которые оказываются рядом вдоль спирали, когда оригами правильно сложено. Один из членов каждой пары несёт небольшую химическую метку, позволяющую им быть энзиматически соединёнными, или лигированными, но только если они по‑прежнему удерживаются близко друг к другу целой матричной нитью. Если структура расплавляется, ломается или разрушается ферментами, эти два участка расходятся и больше не могут быть лигированы. После лигирования соединённые пары амплифицируют с помощью стандартной полимеразной цепной реакции и количественно определяют чувствительным qPCR или секвенированием, превращая присутствие интактных локальных сегментов в измеримые сигналы из всего лишь микролитров крови.
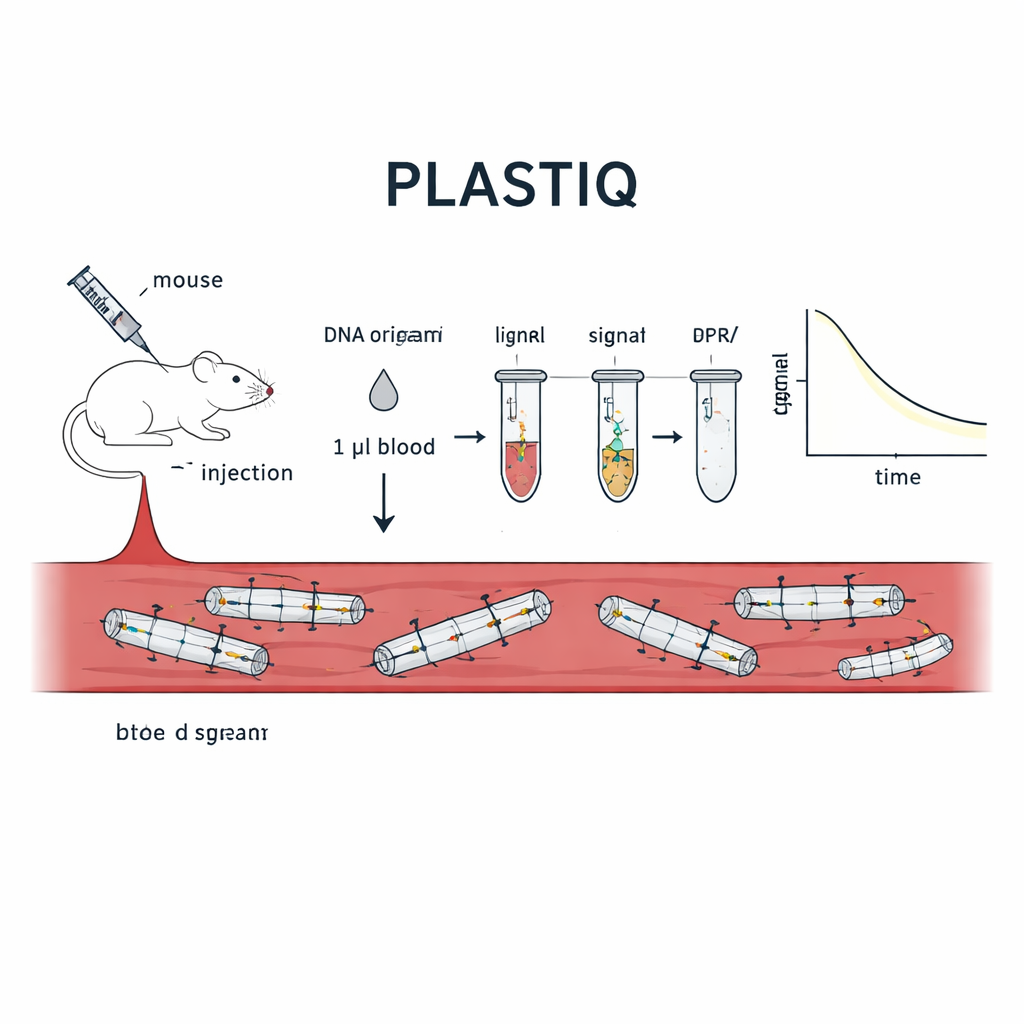
Применение теста в живых мышах
Чтобы доказать, что PLASTIQ действительно измеряет структурную целостность, авторы сначала применили его к простым стержневым конструкциям ДНК-оригами в пробирках. Сигналы появлялись только когда стержни были целы и исчезали после термически вызванного разворачивания, тогда как более традиционные ДНК‑анализы по-прежнему регистрировали ДНК независимо от формы. Затем эти стержни вводили мышам различными путями — прямо в кровоток, в брюшную полость, в мышцу и подкожно — и забирали всего по одному микролитру крови в разные моменты. PLASTIQ показал, как концентрация интактных структур всплескивала, а затем падала в зависимости от пути введения, соответствуя общим ожиданиям фармакологии препаратов, но с гораздо более тонкой структурной детализацией. Метод был чувствителен вплоть до 0,01 фемтомоля и требовал минимального объёма крови, что позволяло многократно брать пробы у одного и того же животного в течение нескольких часов.
Тестирование защитных покрытий и скрытых уязвимых мест
Многие группы пытаются защитить ДНК-оригами, покрывая их полимерами, такими как PEG, сшивая нити ультрафиолетом или добавляя химические связыватели, но было трудно увидеть, насколько эти приёмы действительно помогают in vivo. С помощью PLASTIQ авторы показали, что PEG-покрытые стержни в кровотоке сохраняют целостность немного дольше, чем необработанные, но также быстрее выводятся, как только попадают в циркуляцию, и что покрытие не препятствует работе ферментов PLASTIQ. Комбинируя PLASTIQ с простыми математическими моделями, они извлекли скорости абсорбции и элиминации для разных путей введения и покрытий и даже могли смоделировать режимы повторного введения. Затем они расширили метод с помощью двухслойной бочкообразной оригами, упакованной плотнее внутри, чем снаружи. Измерения PLASTIQ показали, что степлы на открытой внешней поверхности теряют целостность быстрее, чем те, которые обращены к внутренней полости, что прямо подтверждает, что скрытые спирали защищены от разрушающих ферментов в крови.
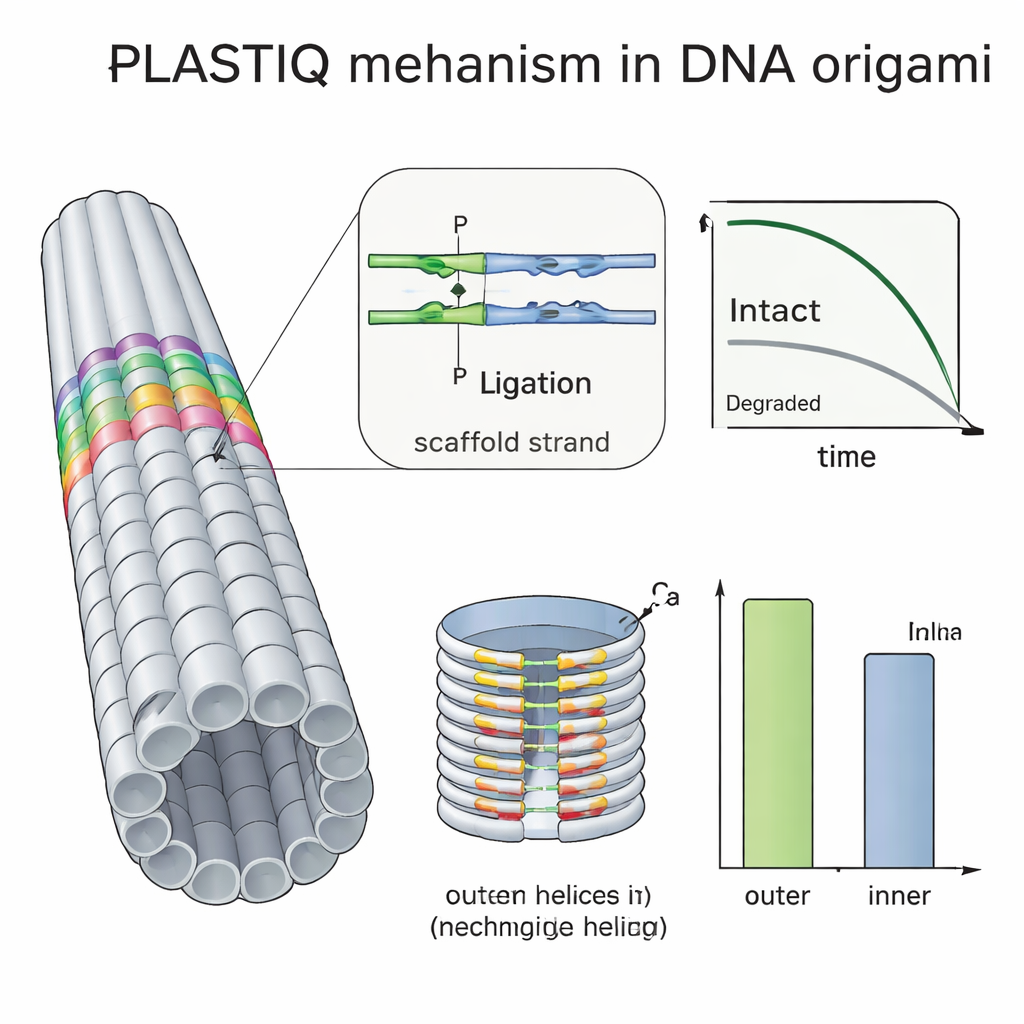
Что это значит для будущих ДНК‑на основе терапий
Для неспециалиста PLASTIQ можно рассматривать как структурную проверку для наномасштабных ДНК‑устройств, путешествующих по организму. Вместо того, чтобы просто спрашивать «здесь есть ДНК?», он спрашивает «эта ДНК по‑прежнему сложена в тот точный объект, который мы спроектировали?». Отвечая на этот вопрос с высокой чувствительностью по крошечным образцам крови, PLASTIQ даёт разработчикам препаратов способ оптимизировать дизайн, покрытие и дозирование лекарств и вакцин на базе ДНК-оригами. Со временем такое детальное количественное понимание поведения этих наноструктур в реальных биологических средах может помочь превратить ДНК-оригами из элегантной лабораторной идеи в надёжные, готовые к регуляторной оценке терапевтические средства.
Цитирование: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Ключевые слова: ДНК-оригами, наномедицина, доставка препаратов, фармакокинетика, нанотехнологии