Clear Sky Science · ru
вакцинация мРНК преодолевает вызванное гемозоином ослабление эффективности цельнопаразитарных вакцин от малярии у мышей
Почему перенесённая малярия делает вакцины менее эффективными
Малярия убивает сотни тысяч людей ежегодно, и одной из самых перспективных стратегий является использование цельных ослабленных паразитов для обучения иммунной системы. Любопытно, что этот «золотой стандарт» действует значительно лучше у людей, которые никогда не болели малярией, чем у тех, кто вырос в эндемичных районах. Это исследование на мышах задаёт простой, но ключевой вопрос: что именно в предыдущих инфекциях малярии приводит к падению эффективности высокоэффективной вакцины — и сможет ли новый тип мРНК-вакцины исправить ситуацию?
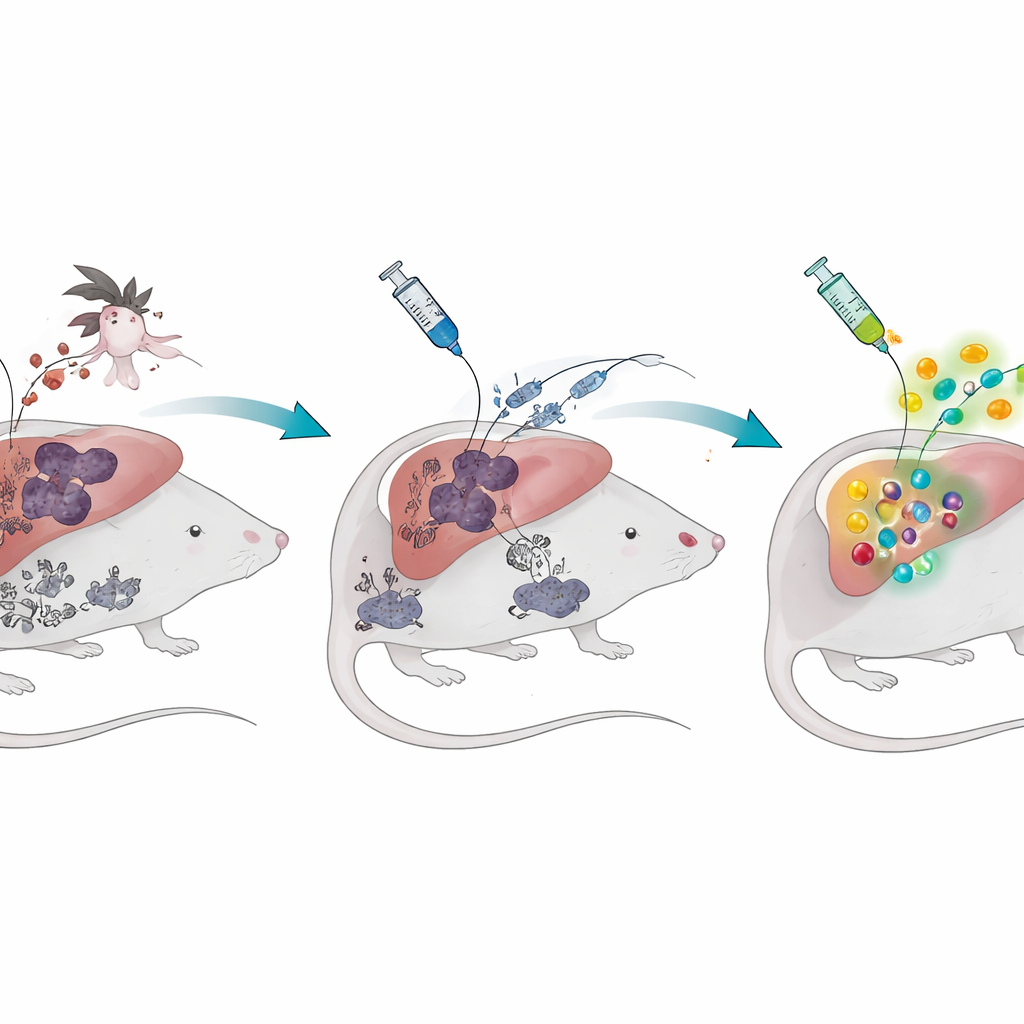
История о двух стадиях малярии
У паразита малярии в организме человека есть две основные стадии. Сначала, после укуса комара, он тихо инфицирует печень. Позже он проникает в эритроциты, вызывая лихорадку и болезнь. Цельнопаразитарные вакцины на основе радиационно-аттенуированных спорозоитов нацелены на безмолвную печёночную стадию: паразиты попадают в печёночные клетки, но не могут завершить жизненный цикл, давая иммунной системе безопасную «репетицию». У мышей, не сталкивавшихся ранее с малярией, эта стратегия формирует большое количество специализированных киллерных Т-клеток, оседающих в печени и способных уничтожать паразитов до развития болезни. Но когда исследователи предварительно инфицировали мышей кровяной стадией малярии и затем позволяли инфекции пройти, та же вакцина вызывала значительно меньше защитных Т-клеток, и животные были заметно хуже защищены при последующей встрече с живыми паразитами.
Застывший пигмент, который не уходит
Команда затем выясняла, что же отличается у этих «опытных в малярии» мышей. Главным подозреваемым оказался гемозоин — тёмный, кристаллоподобный пигмент, который паразит образует внутри эритроцитов, чтобы обезвредить железосодержащие продукты распада гемоглобина. Этот пигмент не исчезает после окончания инфекции; он может сохраняться в печени, селезёнке и костном мозге в течение многих месяцев. Учёные обнаружили, что даже более чем через год после завершения кровяной стадии у мышей всё ещё сохранялся гемозоин и наблюдалась ослабленная Т-клеточная реакция на печёночную вакцину. Введение здоровым мышам очищенного синтетического гемозоина — без каких-либо живых паразитов — было достаточно, чтобы воссоздать это длительное снижение эффективности вакцины и снизить защиту при последующем вызове малярией.
Как гемозоин сбивает с толку стражей иммунитета
Углубляясь, исследователи сосредоточились на дендритных клетках — стражах иммунной системы, которые захватывают фрагменты патогенов и представляют их Т-клеткам. Для работы цельнопаразитарной печёночной вакцины дендритные клетки должны захватывать материалы паразита, поступающие из инфицированных печёночных клеток, и демонстрировать их киллерным Т-клеткам. В экспериментах в культуре клеток команда показала, что гемозоин напрямую мешает этому этапу захвата: чем дольше дендритные клетки подвергались воздействию гемозоина, тем хуже они поглощали белковые антигены. Дефект проявлялся как в клетках мышей, так и в человеческих иммунных клетках, полученных от доноров крови, и не зависел от одного хорошо известного сенсора воспаления, что указывает на то, что сам гемозоин действует как физическое или биохимическое препятствие для нормальной обработки антигенов.
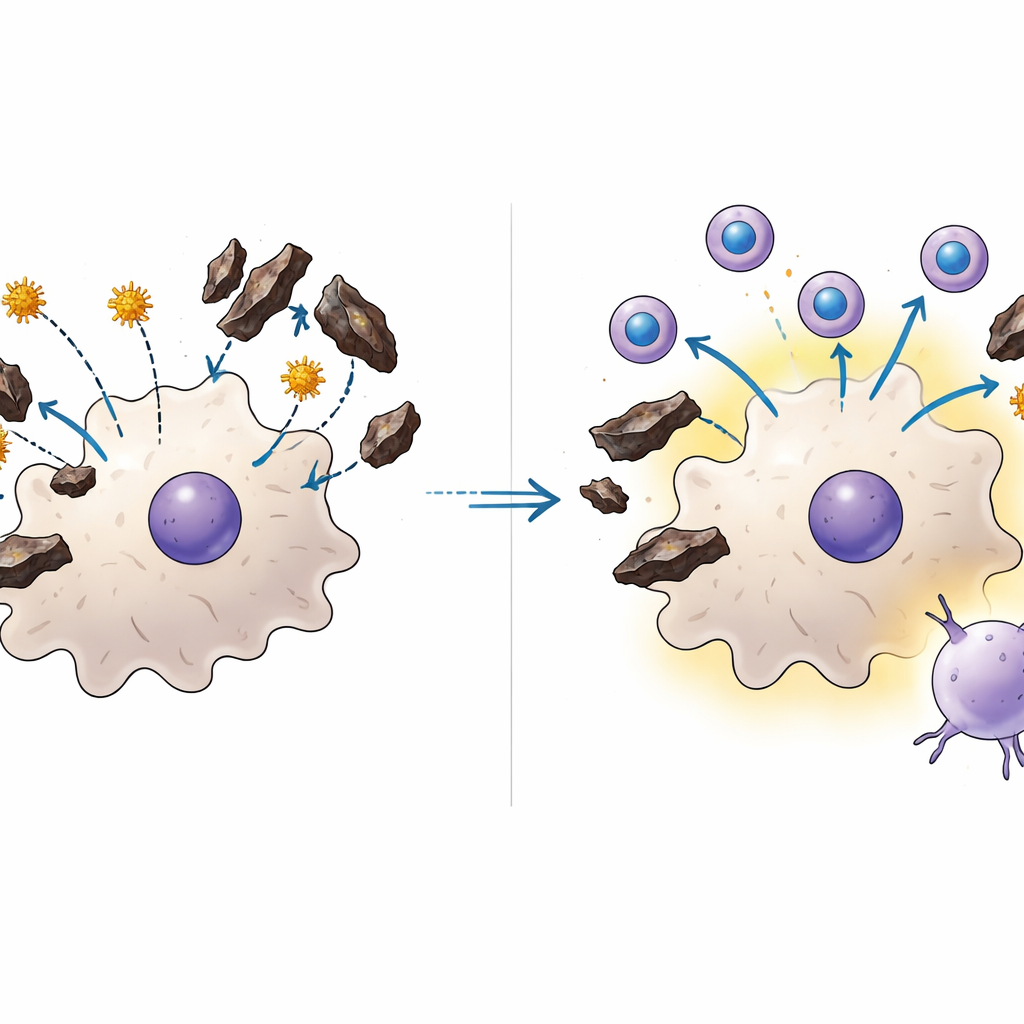
мРНК-вакцины обходят это препятствие
Чтобы выяснить, сможет ли другой формат вакцины избежать этой проблемы, учёные разработали мРНК-вакцину, упакованную в липидные наночастицы. Вместо того чтобы доставлять паразитарные белки извне, этот подход даёт клеткам хозяина генетические инструкции для синтеза коротких фрагментов нескольких паразитарных белков внутри клетки. У мышей как с предшествующей малярией, так и без неё мРНК-вакцина вызывала примерно одинаково сильные ответы киллерных Т-клеток и улучшала контроль печёночной инфекции. Поразительно, что при сочетании мРНК-вакцины с одной дозой цельнопаразитарной печёночной вакцины у мышей формировались особенно большие популяции Т-клеток, которые надолго оседали в печени — клеточная популяция, известная как ключ к быстрой защите. В культурах гемозоин не блокировал захват или функцию мРНК-загруженных наночастиц, что объясняет, как эта стратегия может сработать там, где более старая вакцина поодиночке оказывается неэффективной.
Что это значит для будущих прививок от малярии
Проще говоря, исследование показывает, что перенесённые инфекции малярии оставляют микроскопические минеральоподобные остатки, которые нарушают обучение некоторых иммунных клеток при вакцинации, ослабляя действие ведущей цельнопаразитарной вакцины от малярии. Но переход на мРНК-вакцину или её комбинирование с цельнопаразитарной платформой — которое даёт инструкции для синтеза паразитарных фрагментов прямо внутри клеток — позволяет обойти эти остатки и восстановить сильную защиту у животных с опытом малярии — по крайней мере у мышей. Работа указывает на гемозоин как на важное препятствие для вакцин у людей, живущих в эндемичных регионах, и предполагает, что тщательно спроектированные мРНК- или комбинированные режимы вакцинации могут стать перспективным путём к более эффективной, широко применимой иммунизации против малярии.
Цитирование: Hassert, M., Drewry, L.L., Pewe, L.L. et al. mRNA vaccination overcomes haemozoin-mediated impairment of whole-parasite malaria vaccines in mice. Nat Microbiol 11, 718–730 (2026). https://doi.org/10.1038/s41564-026-02263-0
Ключевые слова: вакцины от малярии, гемозоин, вакцина мРНК, Т-клеточный иммунитет, инфекция Plasmodium