Clear Sky Science · ru
Кожные андрогены регулируют патогенность Staphylococcus aureus через кворумное зондирование
Почему гормоны на коже важны
У мужчин склонность к более тяжёлым кожным инфекциям выше, чем у женщин, но причины долгое время оставались неясными. В этом исследовании показано, что гормоны, находящиеся прямо на поверхности кожи, особенно мужской гормон тестостерон, могут переключать поведение обычной бактерии из спокойного соседа в опасного захватчика. Понимание этого скрытого диалога между нашими гормонами и микробами не только объясняет давнее различие в риске инфекции между полами, но и указывает на неожиданный способ обезвреживания антибиотикоустойчивых микроорганизмов без опоры на традиционные лекарства.
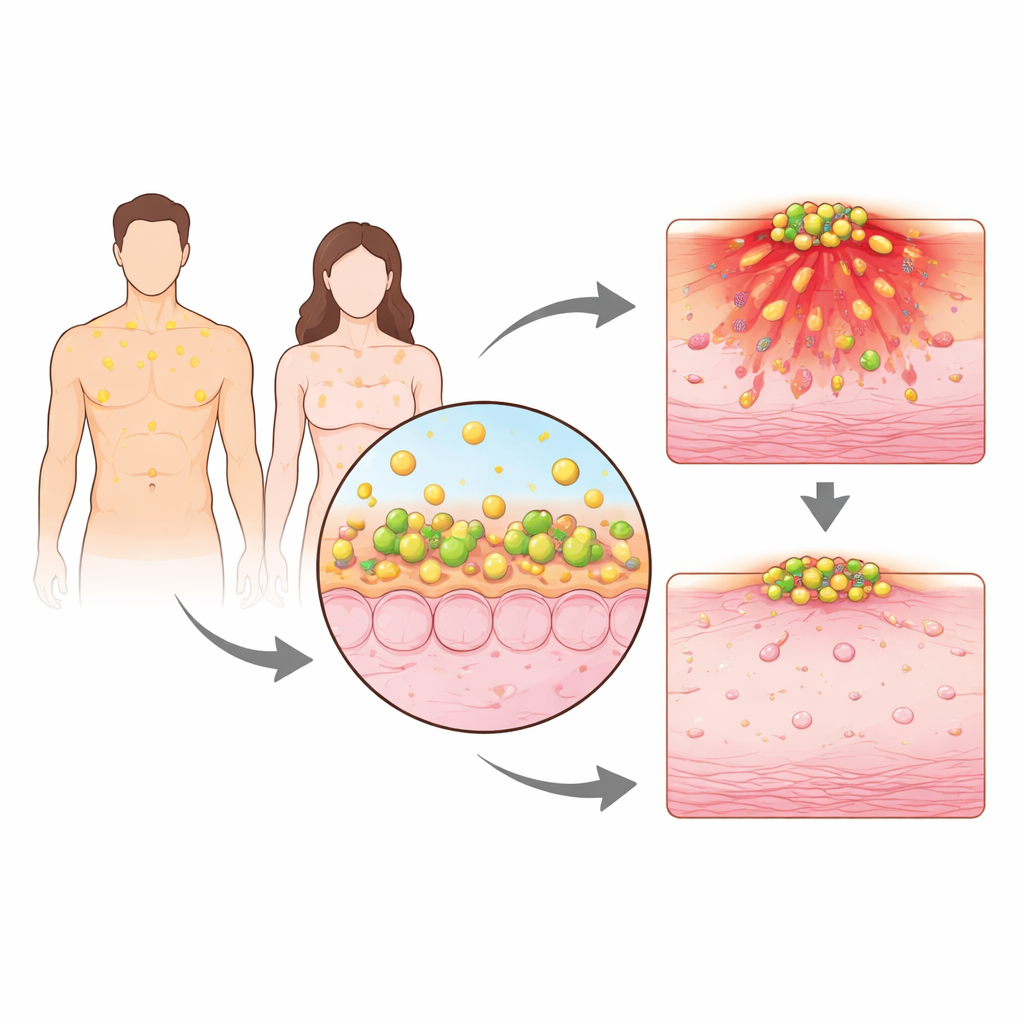
Повседневные гормоны, омывающие кожу
Кожа делает больше, чем просто защищает нас от внешнего мира; она также синтезирует и выделяет собственный набор гормонов. Используя крошечные клейкие полоски, впитывающие кожные масла, исследователи измеряли тестостерон на лицах здоровых мужчин и женщин в течение нескольких дней. Оба пола продуцировали стабильные наносомолярные количества тестостерона, но у мужчин на поверхности кожи постоянно было больше. У мышей самцы также имели более высокие уровни тестостерона и его близкого аналога дигидротестостерона в кожных выделениях. Эти повышенные уровни андрогенов сочетались с более тяжёлыми инфекциями, когда животные подвергались воздействию Staphylococcus aureus, главной причины инфекций кожи и мягких тканей у людей.
Снижение кожных гормонов защищает от инфекции
Чтобы проверить, действительно ли важны гормоны, производимые кожей, команда создала мышей, у которых клетки кожи лишены ключевого фермента, необходимого для локального синтеза тестостерона, при этом уровни гормонов в крови оставались неизменными. Эти «андроген‑дефицитные» мыши имели нормальную структуру кожи и барьерную функцию, но выделяли гораздо меньше тестостерона, прогестерона и дигидротестостерона на поверхность кожи. При заражении метициллин‑резистентным Staphylococcus aureus (MRSA) у этих мышей наблюдались слабее выраженные бактериальные сигналы, менее выраженное покраснение и отёк, меньше повреждений тканей и лучше сохранившаяся барьерная функция по сравнению с нормальными мышами. Поразительно, что когда самкам‑андроген‑дефицитным мышам наносили каплю тестостерона на кожу, их инфекции ухудшались и начинали напоминать те, что наблюдаются у самцов. Это показало, что андрогены на поверхности кожи, а не общий гормональный статус организма, задают предпосылки для развития заболевания S. aureus.
Как бактерии подслушивают наши гормоны
S. aureus использует систему связи, называемую кворумным зондированием, чтобы решать, когда продуцировать токсины, повреждающие клетки хозяина. Сердцем этой системы является пара сенсоров, AgrC и AgrA, которые обычно реагируют на небольшие бактериальные пептиды. Когда исследователи обмакивали разные штаммы S. aureus в ничтожные количества тестостерона или дигидротестостерона, бактерии усиливали экспрессию генов, обычно включающихся при кворумном зондировании, включая гены, кодирующие мощные токсины. Это происходило во многих клинических штаммах, включая MRSA и изоляты от людей с атопическим дерматитом. Тестостерон усиливал способность бактерий убивать человеческие эритроциты, клетки кожи и нейтрофилы, но сам рост бактерий не увеличивался. У мышей с низким уровнем кожных андрогенов репортерный штамм для кворумного зондирования показывал значительно слабее активацию, что подтверждало: гормоны на коже стимулируют это бактериальное «групповое принятие решений» в живой ткани.
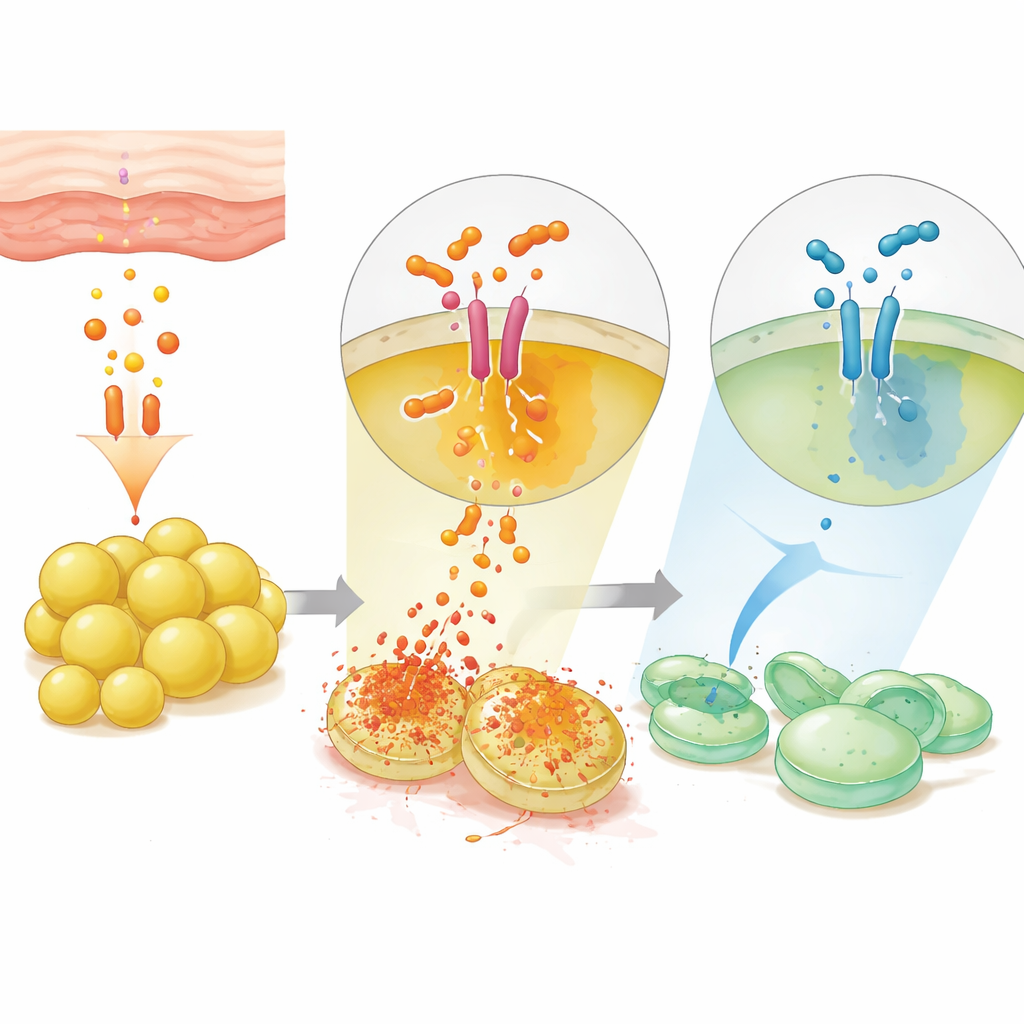
Прямое молекулярное рукопожатие и встроенный выключатель
Удивительно, но тестостерон мог активировать кворумное зондирование даже у мутантных бактерий, неспособных синтезировать собственные сигнальные пептиды, то есть гормон может замещать обычный бактериальный триггер. Однако для этого был необходим целый сенсор AgrC на поверхности бактерии и его партнёр AgrA; при нарушении любого из них тестостерон больше не повышал экспрессию генов токсинов и не вызывал клеточных повреждений. Компьютерное моделирование предложило, что тестостерон встраивается в гидрофобный карман на AgrC, отличающийся от обычного участка связывания пептида, физически сдвигая рецептор в активное состояние. Команда затем перевернула задачу, испытав зеркальную версию тестостерона, называемую энантиомером тестостерона (ent‑T). Хотя химически похожий, ent‑T блокировал кворумное зондирование, снижал продукцию токсинов и защищал человеческие клетки от бактериального повреждения. При нанесении на заражённую кожу мышей ent‑T ослаблял активность кворумного зондирования в обоих полах, действуя как молекулярный тормоз вирулентности.
Что это значит для будущих лечений
Проще говоря, исследование показывает, что S. aureus буквально «чуяет» тестостерон на нашей коже и использует этот сигнал, чтобы решить, когда атаковать. Более высокие уровни андрогенов на коже у мужчин помогают объяснить, почему они более склонны к тяжёлым инфекциям S. aureus. Не менее важно, что работа предлагает новую терапевтическую идею: вместо того чтобы уничтожать бактерии напрямую, можно уменьшать их агрессию, блокируя гормонные сенсоры. Соединения вроде ent‑T или стратегии, снижающие уровень андрогенов на поверхности кожи, могли бы ослабить MRSA и родственные штаммы, облегчая контроль инфекций и уменьшая ущерб при одновременном снижении давления, стимулирующего развитие антибиотикорезистентности.
Цитирование: John, M.S., Chinnappan, M., Sturges, C.I. et al. Skin androgens regulate Staphylococcus aureus pathogenicity via quorum sensing. Nat Microbiol 11, 704–717 (2026). https://doi.org/10.1038/s41564-026-02261-2
Ключевые слова: кожные гормоны, Staphylococcus aureus, кворумное зондирование, инфекция MRSA, тестостероновая сигнализация