Clear Sky Science · ru
Сравнительный анализ данных глубокого сканирования мутаций у энтеровирусов A и B выявляет функциональную дивергенцию и терапевтические мишени
Почему мелкие РНК‑вирусы важны для нас
Энтеровирусы представляют собой большую группу небольших РНК‑вирусов, которые повсеместно циркулируют в мире, обычно вызывая лёгкие простуды или желудочно‑кишечные расстройства, но иногда — паралич, повреждение сердца и другие тяжёлые болезни. У нас мало вакцин и ещё меньше препаратов, действенных против широкого круга этих вирусов, отчасти потому, что они быстро эволюционируют. В этом исследовании поставлен на первый взгляд простой, но крайне практичный вопрос: при мутациях вируса какие части его «механизма» могут свободно меняться, а какие настолько важны, что эволюция удерживает их почти неподвижными? Ответы указывают на новые стратегии создания лекарств, которым вирус трудно будет противостоять.
Чтение инструкции вируса — по одной мутации
Исследователи сосредоточились на двух человеческих энтеровирусах, вызывающих очень разные заболевания: энтеровирусе A71, связанном с тяжёлыми неврологическими заболеваниями у детей, и коксакивирусе B3, ассоциированном с воспалением сердца и даже раком поджелудочной железы. С помощью метода, называемого глубоким сканированием мутаций, они создали библиотеки вирусов, в которых практически каждая позиция в белках вируса была систематически изменена. Эти мутантные вирусы инфицировали клетки в культуре, а высокопроизводительное секвенирование применялось для измерения влияния каждой замены на рост вируса. Сравнивая каждый мутант с исходным вирусом, команда составила подробную карту сайтов в вирусном протеоме, которые терпимы к изменениям, и тех, которые сильно ограничены. 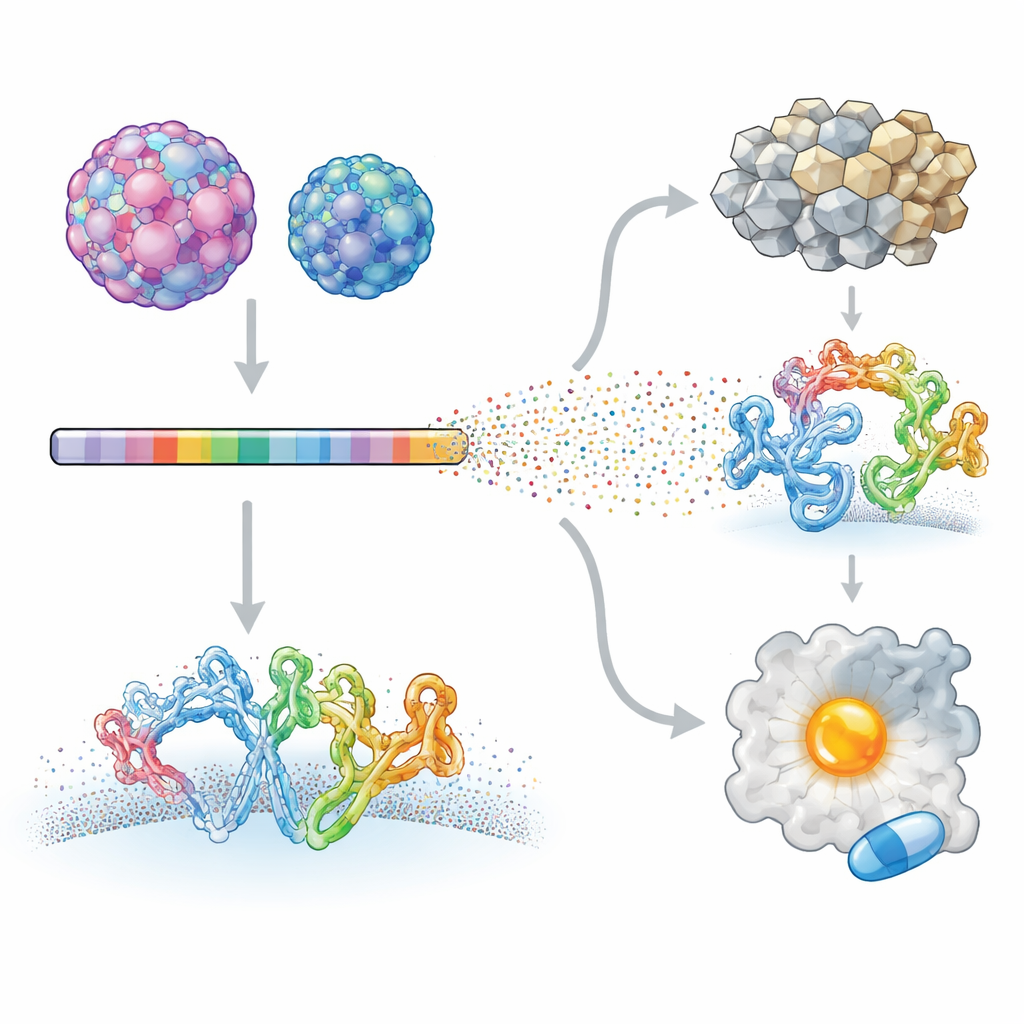
Общие жёсткие пределы и вирус‑специфическая гибкость
Несмотря на то, что они разделяют всего около половины аминокислотных последовательностей, оба вируса продемонстрировали поразительно схожие общие паттерны ограничений. Внутренние ферментные «трудяги», которые копируют геном, расщепляют вирусные белки и раскручивают РНК, были чрезвычайно чувствительны к мутациям в обоих вирусах. Точно так же скрытые поверхности, скрепляющие белковую оболочку — капсид, — оказывались трудноизменяемыми без дестабилизации вируса. Напротив, многие обращённые наружу и взаимодействующие с хозяином участки были более свободны в изменениях и часто сильно различались между двумя видами. Структурный анализ показал, что консервативные, нетерпимые к мутациям регионы сходились вокруг активных центров и интерфейсов сборки, тогда как участки, контактирующие с рецепторами хозяина, мембранами или иммунными молекулами, представляли собой очаги видоспецифической гибкости.
Как вирусы связываются с клетками и уходят от защиты
Затем команда сосредоточилась на молекулярном рукопожатии между вирусом и хозяином. Энтеровирус A71 и коксакивирус B3 используют разные клеточные рецепторы для входа, и исследование показало, что точечные контакты на поверхности капсида являются одними из наиболее различающихся участков по терпимости к мутациям. Остатки, которые удерживают рецептор у одного вируса, сильно ограничены в этом вирусе, но относительно допускаемы в другом — что отражает то, как каждый вид «подогнал» свою платформу стыковки. Похожая дивергенция проявилась в небольшом мембранно‑связанном белке 3A, который помогает перестраивать клеточные мембраны и привлекать факторы хозяина для репликации генома. Моделирование показало, что два вируса используют частично разные контактные поверхности в 3A для взаимодействия с одним и тем же фактором хозяина GBF1 и, возможно, встраивают этот белок в мембраны на разную глубину. Эти различия помогают объяснить, почему близкородственные вирусы инфицируют разные ткани и вызывают разные схемы заболеваний.
Что лабораторная эволюция упускает — и что отражает верно
Чтобы поместить эксперименты в клеточных культурах в контекст реального мира, авторы сравнили свои карты мутаций с тысячами природных вирусных последовательностей из образцов пациентов. В целом участки, гибкие в лаборатории, как правило, также были вариабельны в природе, особенно при более широких межвидовых сравнениях. Однако при анализе предпочтительных аминокислот в каждой позиции природная эволюция и лабораторный отбор совпадали наиболее тесно в пределах одного типа вируса. Примечательно, что наибольшие расхождения сконцентрировались на внешней поверхности капсида и на участках взаимодействия с хозяином в нестуктурных белках 2A и 3A — именно там, где ожидаемо сильное влияние иммунного ответа и сложной среды хозяина. Это указывает на то, что глубокое сканирование мутаций фиксирует базовые механические ограничения белков вируса, в то время как реальные инфекции накладывают дополнительные давления со стороны иммунитета и тканевого тропизма, которые трудно воспроизвести in vitro.
Поиск общей уязвимости для будущих лекарств
Наконец, исследователи спросили, могут ли эти карты выделить общую ахиллесову пяту для разработки препаратов. С помощью вычислительных инструментов они искали в обоих вирусах карманы на поверхностях белков, которые, в принципе, могли бы связывать малые молекулы. Затем они наложили данные по мутациям, чтобы увидеть, какие карманы состоят из остатков, которые вирус не может легко изменить без вреда для себя. Один карман, расположенный на хеликазе 2C — кольцевом моторе, помогающем раскручивать вирусную РНК, выделился особенно. Его форма и составные остатки высоко консервативны среди четырёх основных человеческих видов энтеровирусов, он находится вне уже известных активных центров, и изменения там как редки в природе, так и сильно вредны в лабораторных тестах. 
Что это означает для будущих терапий
Систематически исследуя, как каждая возможная однобуквенная замена влияет на два важных энтеровируса, это исследование выявляет чёткое разделение между общим, жёстким ядром вирусного механизма и более гибкими, видоспецифическими интерфейсами с хозяином. Консервативное ядро включает вновь выделенный карман на хеликазе 2C, который, по‑видимому, трудно мутировать без потери фитнеса вируса, что делает его привлекательной мишенью для широкоспектральных антивирусных средств с высокой барьерностью для развития резистентности. В то же время более адаптируемые внешние поверхности и сайты контакта с хозяином объясняют, почему родственные вирусы ведут себя по‑разному в организме, и указывают на области, где вакцины и иммунно‑ориентированные терапии должны считаться с быстрой эволюцией. В совокупности эти результаты дают дорожную карту для разработки стратегий лечения, использующих эволюционные ограничения самого вируса.
Цитирование: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Ключевые слова: энтеровирусы, вирусная эволюция, глубокое сканирование мутаций, антивирусные мишени, хеликаза 2C