Clear Sky Science · ru
Встроенные H2‑пути обеспечивают биосовместимую гидрирование метаболических алкенов в бактериях
Превращение микробов в крошечные «зеленые» фабрики
Представьте, что обычные кишечные бактерии могли бы заменить ископаемое топливо при производстве повседневных химикатов — от консервантов до пластиков — и при этом помогать убирать пищевые отходы. В этом исследовании показано, что стандартные лабораторные штаммы Escherichia coli могут именно это: они естественным образом генерируют молекулярный водород внутри клетки, и этот водород можно использовать на поверхности клетки для проведения промышленных химических реакций в мягких водных условиях. Сочетая живые микробы с твердым металлическим катализатором, авторы предлагают путь к более чистому, сокращающему выбросы углерода производству.
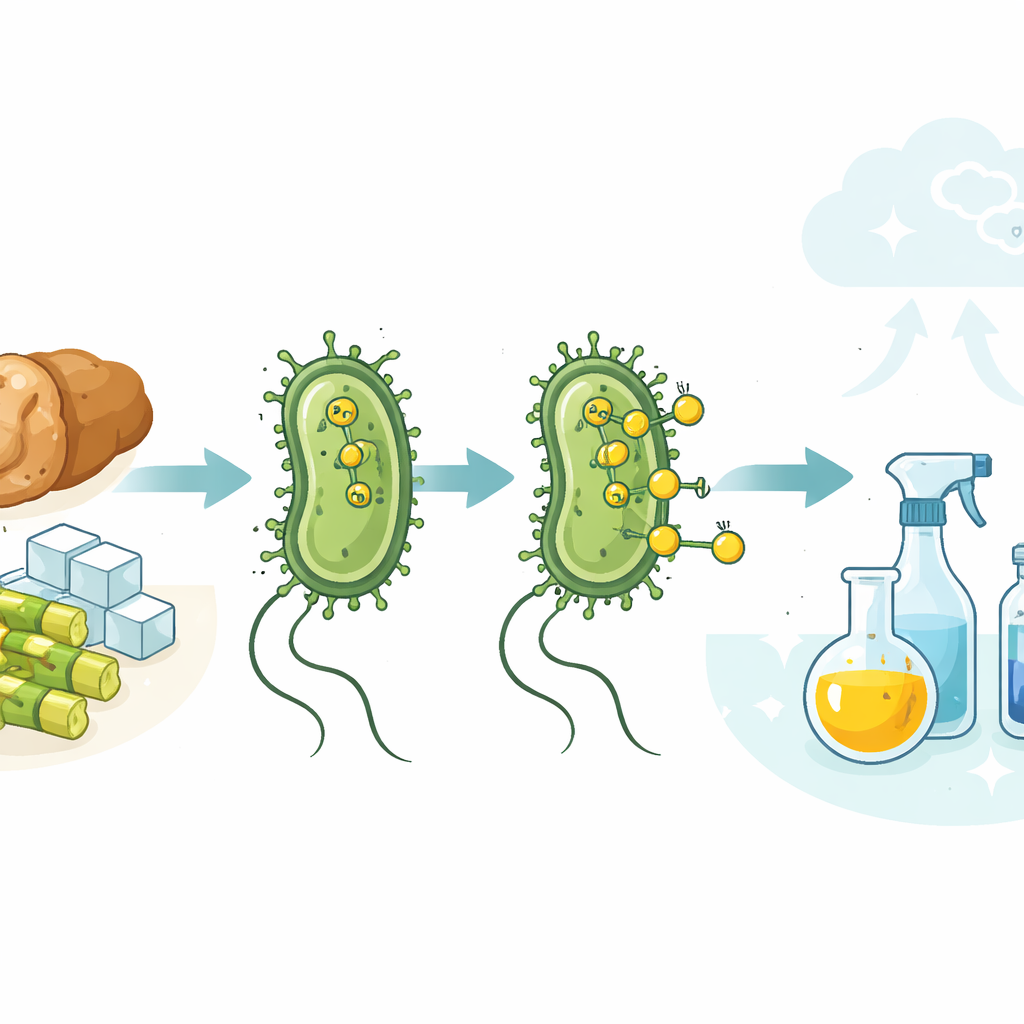
Почему водород важен для повседневной продукции
Молекулярный водород — ключевой реагент современной химии. Его используют для превращения жидких масел в намазки, улучшения топлива и синтеза многих ингредиентов для лекарств и пластмасс. Сегодня почти весь такой водород получают из ископаемого топлива, главным образом природного газа и угля, что приводит к большим выбросам CO2. В то же время многие микроорганизмы естественно выделяют водород при разложении сахаров в условиях дефицита кислорода. Задача авторов — показать, как использовать этот мягкий биологический поток водорода для тех же реакций, которые промышленность сейчас выполняет при высоком давлении, в органических растворителях и с ископаемым газом.
Позволяя бактериям питать металлический катализатор
Команда сосредоточилась на простых реакциях присоединения водорода, где двойная связь в молекуле «насыщается» водородом. Они выращивали несколько немодифицированных штаммов E. coli на сахаросодержащих средах, затем добавляли тонко диспергированный палладиевый катализатор, совместимый с живыми клетками. В бескислородных условиях нативный метаболизм бактерий превращал сахар в формиат, а затем в молекулярный водород на внутренней стороне клеточной мембраны. Микроскопия показала, что положительно заряженные частицы катализатора оседают на отрицательно заряженной поверхности клетки, где встречают выходящий водород. Там металл использует микробный водород для восстановления тестовой молекулы — кофеевой кислоты — в насыщенный продукт с очень высоким выходом, часто превосходящим результаты ранее сильно модифицированного штамма.
Расширение ассортимента продуктов и сырья
Когда базовая реакция заработала, исследователи опробовали широкий набор молекул с двойными связями C–C, включая растительные кислоты и длинноцепочечные жирные соединения. Многие из них гладко превращались в свои насыщенные аналоги, некоторые почти количественно. Они также создали штаммы E. coli, усиливающие образование водорода за счёт перераспределения метаболического потока в нативный путь образования H2. Эти усиленные штаммы обеспечивали те же преобразования при меньшем количестве металлического катализатора. В одном из неожиданных ходов команда заменила чистый сахар расплавленным хлебным тестом в качестве питательной среды. Ферменты расщепляли черствый хлеб до глюкозы, которую бактерии ферментировали столь же эффективно, превращая обычные пищевые отходы как в биологический водород, так и в химически ценные продукты.
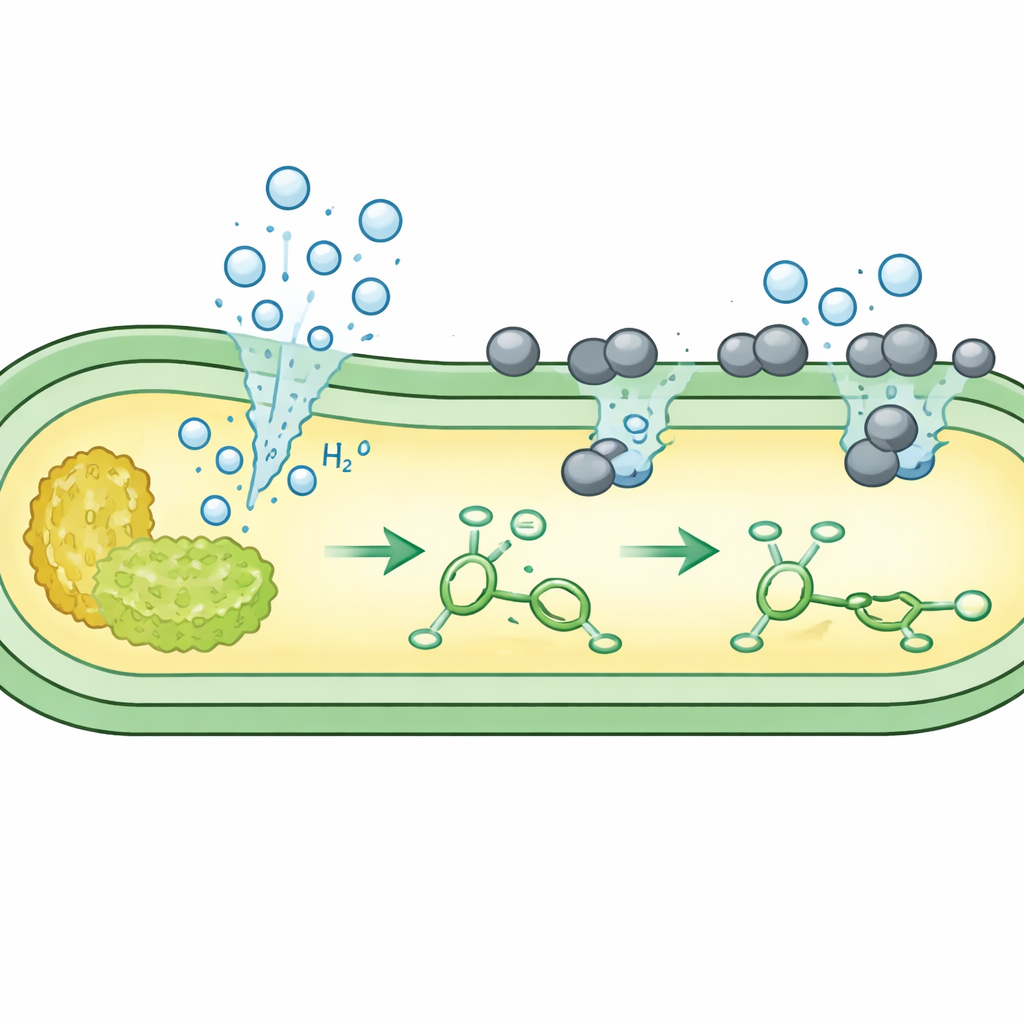
Создание и реагента, и топлива в одной клетке
Далее авторы поинтересовались, может ли одна и та же бактерия производить не только водород «реагент», но и ненасыщённый «субстрат», который требуется преобразовать. Они модифицировали E. coli так, чтобы сахар сначала шёл в пути синтеза ароматических строительных блоков, таких как коричная и кумаровая кислоты, и одновременно в путь, генерирующий водород. Когда в культуре накопились эти внутриклеточные метаболиты, добавляли палладиевый катализатор. На поверхности клетки катализатор использовал внутриклеточно образованный водород для превращения новообразованных двойных метаболитов в полностью насыщенные продукты — например, гидрокоричную кислоту, десаминотирозин и адипиновую кислоту, ключевой предшественник нейлона. В некоторых вариантах совместный метаболизм давал почти полное превращение, всё это происходило в одной и той же живой культуре.
Оценка климатической выгоды
Чтобы понять, действительно ли эта хитрая биохимия полезна для планеты, команда провела оценку жизненного цикла, сравнив их гибридный «хемо‑микробный» подход со стандартными маршрутами гидрирования, питаемыми ископаемым или электролитическим водородом. Когда биологический водород и внутриклеточное производство субстратов объединялись в одном теплоэффективном процессе, суммарные выбросы парниковых газов существенно снижались. Использование хлебных отходов в качестве сырья ещё больше улучшало показатели: избегая захоронения или сжигания и превращая отброшенную пищу в химикаты, некоторые сценарии становились углеродно‑отрицательными в целом, т.е. удаляли из атмосферы больше парниковых газов, чем выпускали.
Что это значит для будущего производства
Проще говоря, исследование демонстрирует, что повседневные бактерии можно побудить выступать одновременно источником энергии и фабрикой ингредиентов для важных химических реакций, а твердый металл на их поверхности аккуратно завершает процесс. Поскольку всё происходит в воде, при близкой к телесной температуре и с использованием возобновляемых или отходных сахаров, этот подход в перспективе может предложить более чистую альтернативу традиционным нефтехимическим заводам. При дальнейшем инженерном улучшении микробных путей и катализаторов эта платформа «живых клеток» может дать новое поколение устойчивых процессов, превращающих возобновляемый углерод и отброшенную пищу в полезные продукты с гораздо меньшим климатическим следом.
Цитирование: White, M.F.M., Trotter, C.L., Steele, J.F.C. et al. Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria. Nat. Chem. 18, 535–543 (2026). https://doi.org/10.1038/s41557-025-02052-y
Ключевые слова: микробный водород, зеленая химия, биокатализ, отходы-в-химикаты, устойчивое производство