Clear Sky Science · ru
Моновалентные псевдо-натуральные вещества усиливают деградацию IDO1 его родным E3-лигазой KLHDC3
Выключение фермента, благоприятствующего раку
Наша иммунная система постоянно патрулирует в поисках раковых клеток, но опухоли нередко парируют, захватывая молекулярные механизмы организма. Один из ключевых участников этой борьбы — фермент IDO1, который помогает опухолям обезвреживать иммунные клетки. В этой работе описан новый класс малых молекул, которые делают больше, чем просто блокируют активность IDO1 — они убеждают клетки избавиться от самого фермента. Используя естественную систему утилизации клеточного «мусора», эти соединения могут восстановить иммунные атаки на опухоли способами, недоступными старым препаратам.
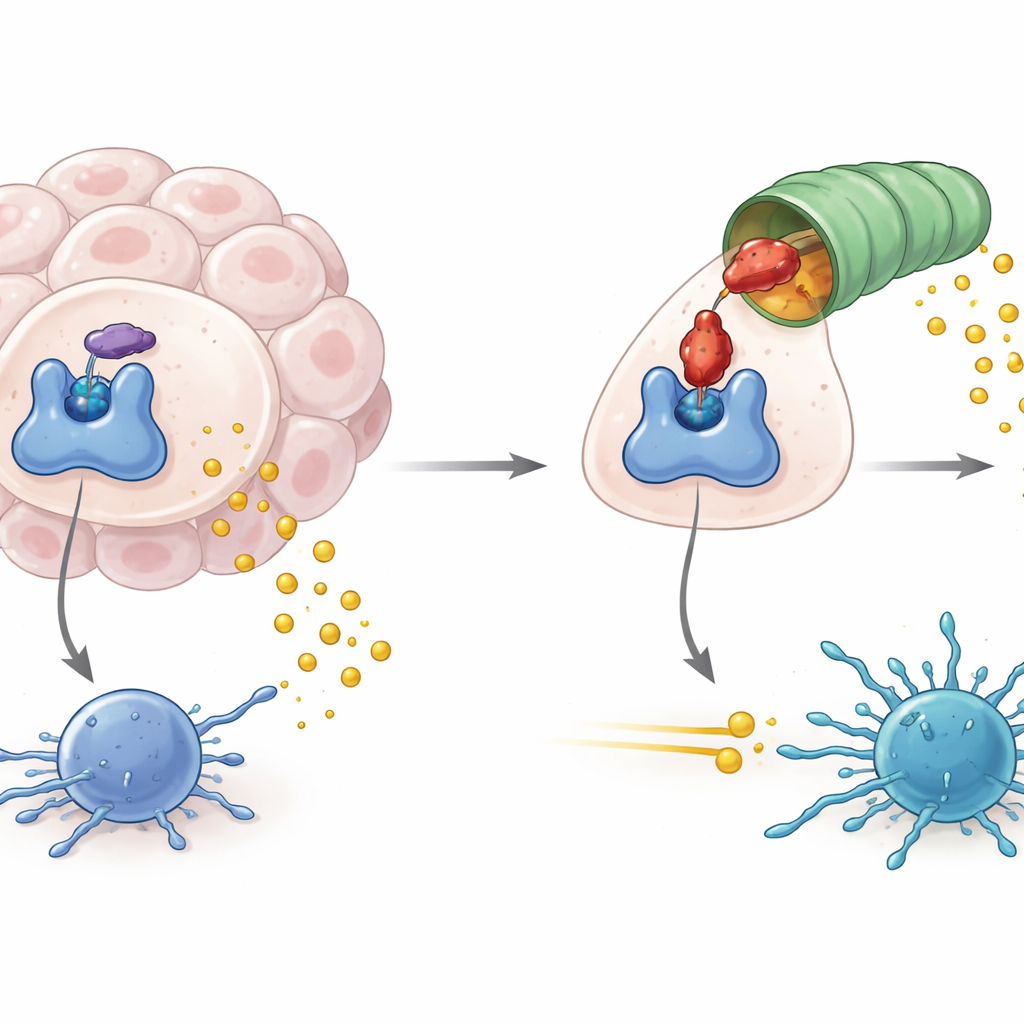
Как опухоли используют метаболического «шлюза»
IDO1 расположена в начале метаболического пути, расщепляющего аминокислоту триптофан до продукта под названием кинуренин. При высоком уровне и активности IDO1 концентрация триптофана падает, а кинуренина — растет, создавая химическую среду, подавляющую активность иммунных клеток, включая Т-лимфоциты, борющиеся с опухолью. Повышенная активность IDO1 связывается не только со слабой противоопухолевой иммунностью, но и с вирус-индуцированными лимфомами и некоторыми формами нейродегенерации. Поэтому разработчики лекарств сосредоточились на блокировании ферментативной активности IDO1 в надежде прервать этот иммуносупрессивный сигнал и повысить эффективность существующих иммунотерапий рака.
Почему простых ингибиторов оказалось недостаточно
Несмотря на обнадеживающие результаты в экспериментах на животных, клинические испытания традиционных ингибиторов IDO1 оказались разочаровывающими. Одно из объяснений в том, что IDO1 — не просто каталитический белок. Даже при блокировке его химической активности сам белок может выступать сигнальным узлом, продолжая способствовать росту и распространению опухоли. Некоторые ингибиторы даже стабилизируют IDO1, повышая его количество в клетке. Иными словами, отключение только каталитической функции может оставить нетронутыми его проопухолевые, неэнзимные роли — а в худшем случае усилить их.
Проектирование соединений, запускающих самоуничтожение
Авторы просеяли большую библиотеку «псевдо-натуральных» молекул — синтетических соединений, собранных из фрагментов, вдохновлённых природными продуктами и перекомбинированных новыми способами. Они обнаружили семейство молекул, названных iDegs, происходящих от растоподобного строительного блока (−)-миртанола. Эти соединения связываются в привычном кармане IDO1 для железосодержащего кофактора гема. Смещая гем, iDegs как ослабляют способность IDO1 синтезировать кинуренин, так и, что важно, перестраивают часть хвостовой области белка. Кристаллические структуры высокого разрешения показывают, что при занятии гемового места iDegs расслабляют и частично дезорганизуют С-концевую спираль, которая в норме удерживается в компактной, защищённой конформации.
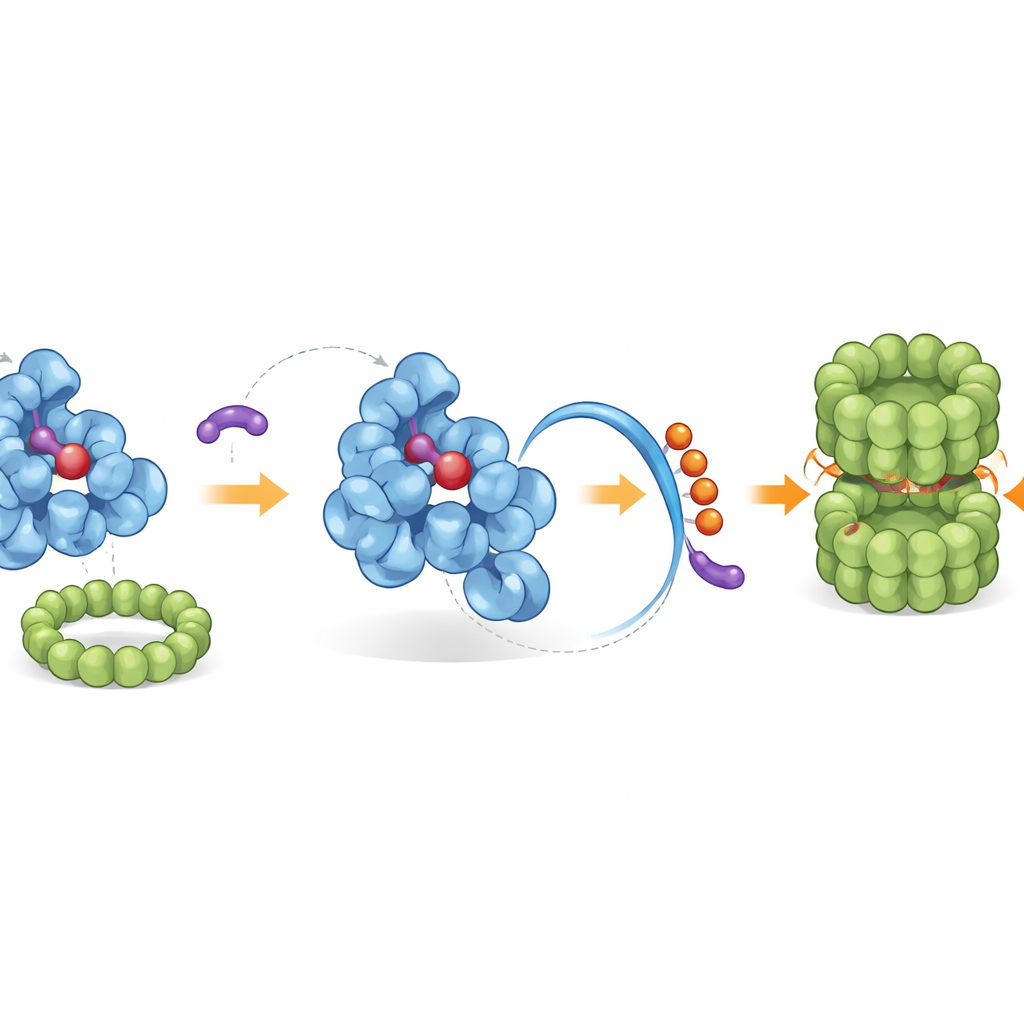
Привлечение родной уборочной бригады клетки
Перестроенный хвост обнажает встроенный «концевой ярлык», который распознаёт механизм утилизации клетки. С помощью генетических скринингов и биохимической реконституции исследователи выявили специфический комплекс лигаз, называемый CRL2–KLHDC3, который естественным образом присоединяет к открытому хвосту IDO1 небольшие «флаги» убиквитина, маркируя его для разрушения протеасомой — молекулярной «теркой» клетки. При нормальных условиях эффективно метится именно гем-свободная форма IDO1, тогда как гем-связанная форма защищена. iDegs смещают этот баланс, связываясь только с гем-свободной формой и усиливая природный путь деградации. Мощные представители серии не только блокируют образование кинуренина, но и повышают уровень убиквитинирования IDO1 и резко сокращают его содержание в различных раковых клетках.
Изменение судьбы IDO1 — и иммунных ответов
Это двойное действие имеет важные функциональные последствия. В тестах миграции на клетках рака яичников клинически исследованный ингибитор IDO1, который стабилизирует фермент, фактически ускорял движение клеток, что согласуется с проопухолевой, неэнзимной ролью IDO1. Напротив, соединение iDeg замедляло миграцию, что соответствует как ингибированию ферментативной функции, так и утрате самого белка. Таким образом, исследование раскрывает новый способ манипуляции IDO1: не насильно направляя его к чужеродной лигазе с громоздкой дизайнерской молекулой, а «усиляя» существующий в клетках природный путь деградации.
Что это может значить для будущих противораковых терапий
Для неспециалистов ключевой вывод в том, что важна не только степень, но и характер ингибирования фермента. Эти новые малые молекулы действуют как точные переключатели: они фиксируют IDO1 в уязвимой форме, которую клетка готова уничтожить, перекрывая и метаболический, и сигнальный вклад фермента в выживание опухоли. Поскольку iDegs компактны, обладают лекареподобными свойствами и полагаются на собственную лигазу клетки для удаления IDO1, они могут предложить более тонкий и широко применимый подход по сравнению с ранними «дегрейдерами» белков. Если подобные стратегии удастся применить к другим проблемным белкам, эта работа открывает перспективу нового поколения терапий, заставляющих больные клетки разрушать собственные молекулярные «оружия».
Цитирование: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Ключевые слова: IDO1, иммунотерапия рака, таргетная деградация белков, убиквитин-лигаза, малые молекулы-деградеры