Clear Sky Science · ru
Биосовместимое уравновешивание лигандов в координации переходных металлов обеспечивает мягкую внутри‑клеточную артилизацию белков
Превращение металлов в бережные инструменты для клеток
Многие мощные химические реакции опираются на металлы, но если поднести те же металлы к живым клеткам, обычно возникают проблемы: повреждение, стресс и гибель. В этом исследовании показано, что при правильной «ручке» вокруг атома никеля можно провести сложную реакцию внутри живых клеток, не нанося им вреда. Это прорыв позволяет учёным помечать тысячи конкретных участков в белках и отслеживать появление трудноуловимых патогенов, открывая новые способы картирования того, что действительно происходит внутри клеток при здоровье и болезни.
Почему металлы и друзья, и враги
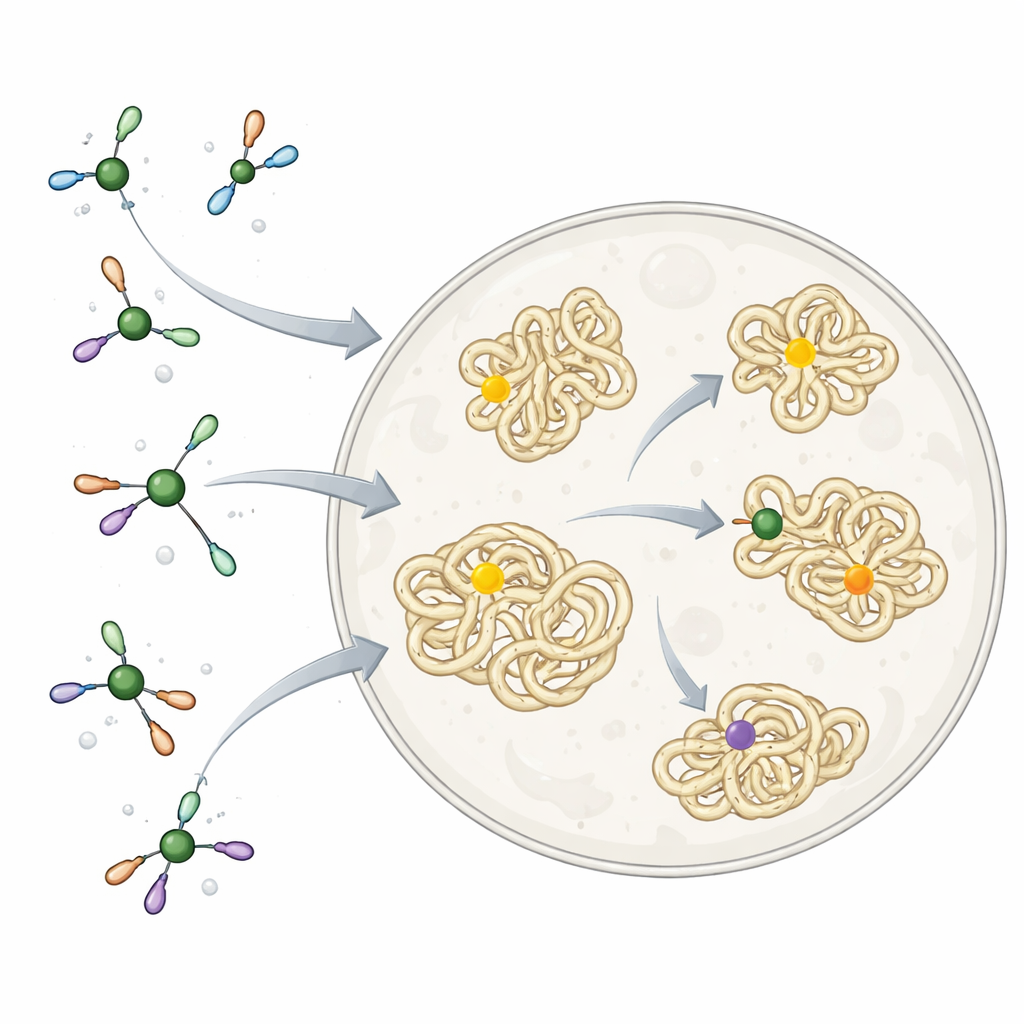
Никель и другие металлы уже тихо работают в наших организмах как части природных ферментов, но они также могут быть токсичны, если связываются не там, где нужно. Природа решает эту проблему, окружая металлы тщательно подобранными малыми молекулами и белками, которые направляют их к правильным мишеням и блокируют нежелательные реакции. Химики же часто используют металлические реагенты, которые чрезвычайно реакционноспособны и вовсе не адаптированы для жизни. Эти реагенты отлично подходят для сборки сложных молекул во флаконе, но слишком агрессивны для свободного применения внутри клеток, особенно когда цель — присоединить маленький «тег» к конкретной аминокислоте в белке, не нарушая остального клеточного устройства.
Проектирование более мягкого никелевого реагента
Исследователи черпали вдохновение в том, как сами клетки обращаются с никелем. Они создали набор никелевых комплексов, окружённых простым биосовместимым лигандом TMEDA. Эта малая молекула действует как мягкий зажим: достаточно тугой, чтобы не дать никелю прилипнуть к неправильным клеточным компонентам, но достаточно свободный, чтобы позволить ему выполнить ключевую реакцию. Реакция присоединяет «арил» — плоскую, кольцевую группировку, часто встречающуюся в лекарствах — к атому серы аминокислоты цистеина в белках. На очищенных белках в растворе эти никелевые комплексы очень быстро и селективно присоединяли арильные группы к отдельным цистеиновым позициям и работали с различными формами и положениями белков, показывая, что химия совместима с реальными биологическими молекулами.
Редактирование белков внутри живых клеток
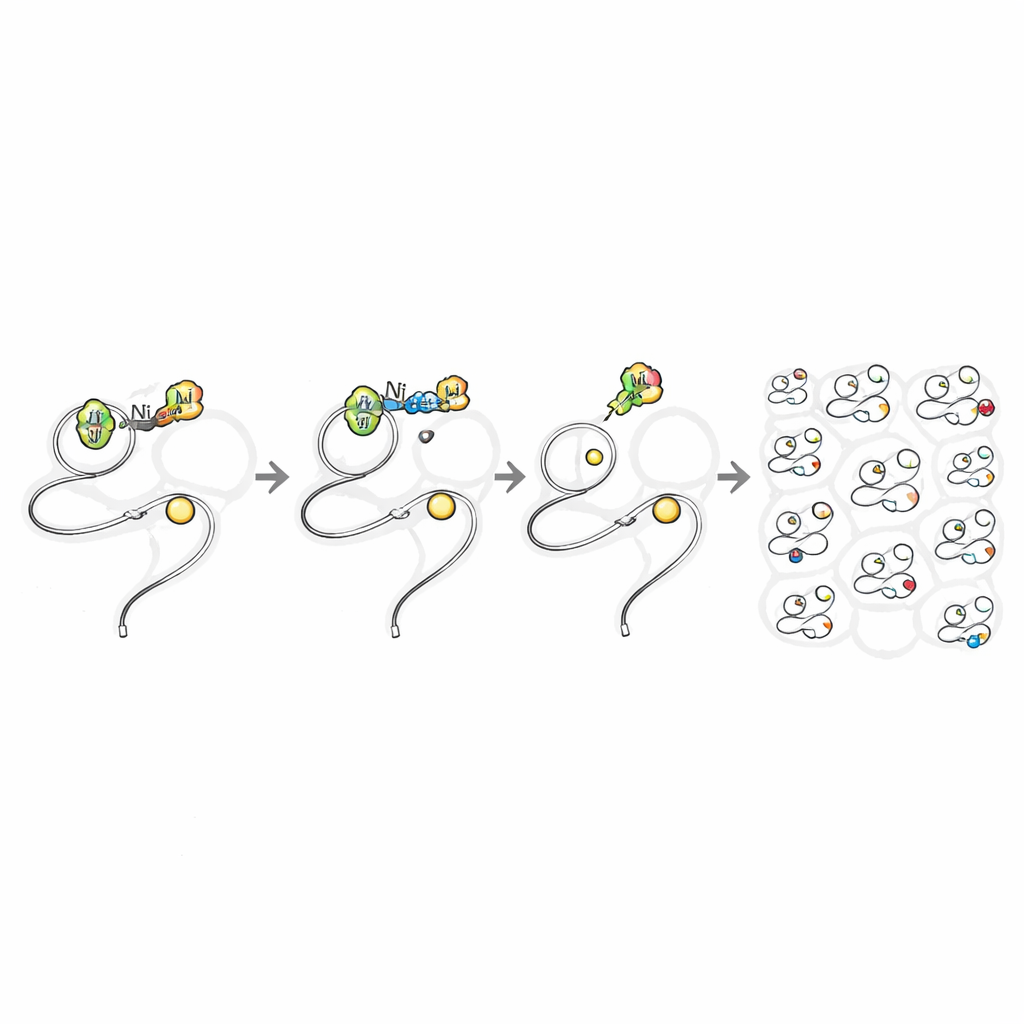
Далее команда проверила, смогут ли эти же реагенты работать внутри живых клеток без грибельного эффекта. Они сравнили простые никелевые соли, известные своей вредностью, с никелевыми комплексами, связанными с TMEDA. В клетках млекопитающих простые источники никеля вызывали значительную гибель при относительно низких дозах, тогда как лиганд‑сбалансированные комплексы оставались хорошо переносящимися даже при миллимолярных концентрациях. Это окно безопасности позволило исследователям вымачивать бактериальные и млекопитающие клетки в никелевых реагентах достаточно долго, чтобы те проникали внутрь и модифицировали белки. Встроив азидную «ручку» в одну версию арильной группы, они могли затем присоединять флуоресцентные красители или биотиновые метки после реакции, что выявляло чёткое, зависимое от дозы окрашивание белков по всему цитоплазме и ядру живых клеток.
Картирование реактивных участков белков по всему протеому
Имея безопасную и быструю внутри‑клеточную реакцию, авторы превратили её в инструмент для открытий. Они обработали живые клетки человека никелевым реагентом с азидной меткой, затем использовали фоторасщепляемую биотиновую метку и современные методы масс‑спектрометрии, чтобы точно увидеть, какие цистеины были модифицированы. В одном эксперименте они обнаружили почти 11 000 цистеиновых сайтов в рамках почти 5 000 белков — примерно вдвое больше белков, чем во всех предыдущих исследованиях по профилированию цистеинов в живых клетках вместе взятых. Метки были высокоселективны к цистеину и мало зависели от конкретных типов белков, локализации или известных активных сайтов. Поразительно, многие из нацеленных белков считались «нелигандируемыми» по современным стандартам поиска лекарств, включая низкоабундантные сигнальные белки и редокс‑чувствительные переключатели, которые трудно изучать только с помощью генетики.
Отслеживание скрытых патогенов в реальном времени
Та же химия оказалась чувствительной настолько, что улавливала чужеродные белки, синтезируемые во время инфекции. В человеческих клетках, несущих латентные вирусные последовательности, метод обнаружил вирусные факторы транскрипции, присутствующие в экстремально низких количествах, включая альтернативные сплайс‑варианты. Затем команда инфицировала клетки двумя очень разными патогенами: внутриклеточной бактерией Chlamydia trachomatis и вирусом Синдбис, РНК‑вирусом, родственником чикунгуньи. Импульсно обрабатывая инфицированные клетки никелевым реагентом в разные моменты времени, они смогли зафиксировать цистеиновые сайты на ключевых бактериальных рибосомных и регуляторных белках по мере переключения бактерии между стадиями жизненного цикла, а также на критически важных виральных нестуктурных белках, отвечающих за репликацию РНК. Эти помеченные сайты теперь выделяются как потенциальные уязвимые точки для будущих антивирусных или антибактериальных стратегий.
Что это значит для будущей клеточной химии
Тщательно уравновесив лигандную оболочку вокруг никеля, эта работа показывает, что традиционно рискованный металл может выполнить точную ковалентную реакцию редактирования белков глубоко внутри живых клеток с минимальным вредом. Это делает возможным создание детальной функциональной карты реактивных цистеиновых сайтов по всему протеому, включая белки, которые редки, кратковременны или труднодоступны для лекарственной разработки. Также это даёт способ отслеживать и исследовать патогены в их клетках‑хозяевах на уровне отдельных аминокислот. В более широком смысле исследование предполагает, что многие другие «запрещённые» металлические химии могут быть укрощены аналогичным образом, открывая новую эру, в которой мощные инструменты синтетической химии безопасно работают внутри живых систем.
Цитирование: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Ключевые слова: профилирование цистеина, никелевое биоконъюгирование, маркировка белков в живых клетках, хемопротеомика, картирование протеома патогенов