Clear Sky Science · ru
Убиквитинирование по лизину-11 запускает индукцию интерферонов типа I/III через cGAS–STING и Toll-подобные рецепторы 3 и 4
Как наши клетки подают сигнал тревоги
Когда вирусы или опасные молекулы проникают в организм, клетки должны в течение минут решить, запускать ли мощные противовирусные сигналы — интерфероны. Эти сигналы помогают защититься от тяжёлых инфекций, но при ошибочной активации они могут приводить к повреждающим аутоиммунным заболеваниям. В этом исследовании выявлена ранее скрытая молекулярная «переключательная панель» внутри клеток, которая помогает решать, когда включать интерферонный ответ, а когда его сдерживать. Понимание этой панели даёт подсказки для улучшения вакцин, антивирусной терапии и лечения расстройств, вызванных интерферонами.
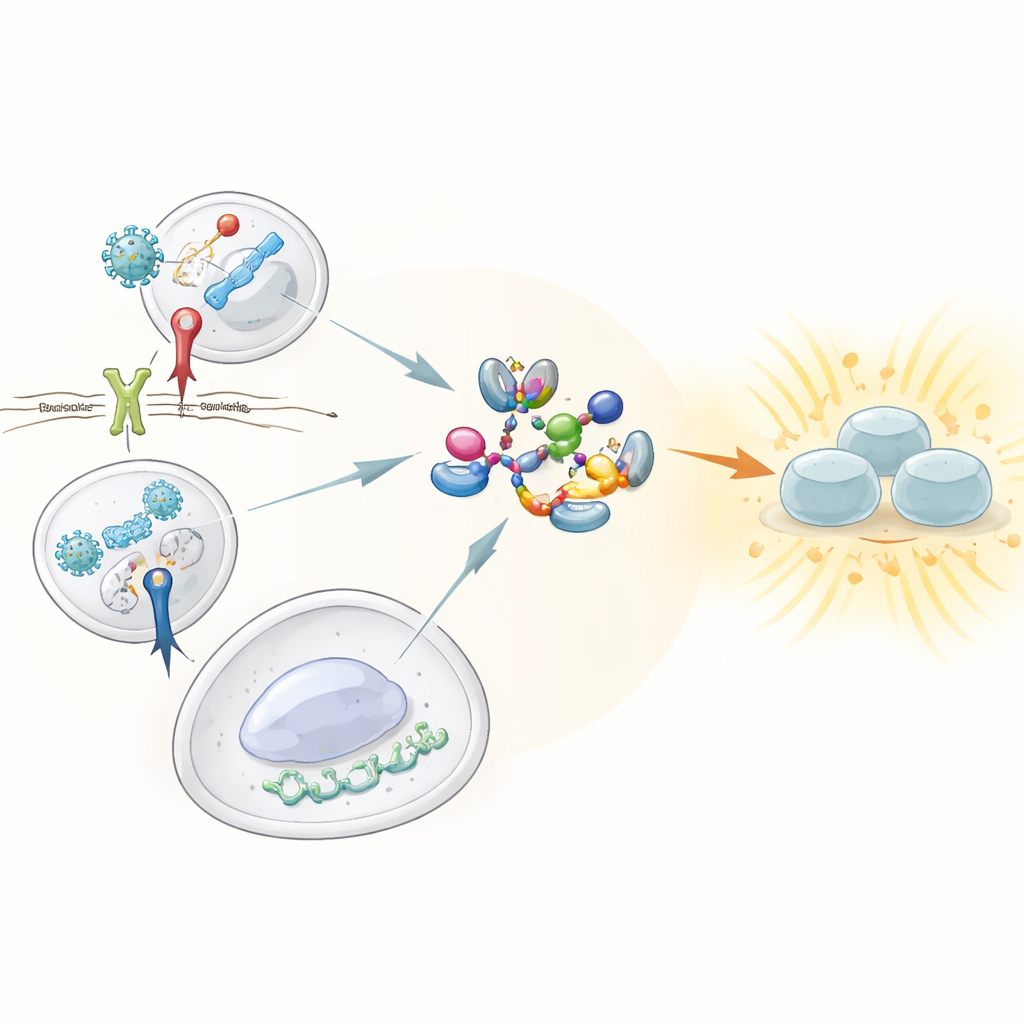
Стражи, которые улавливают угрозу
Врожденная иммунная система опирается на стражей — рецепторы распознавания паттернов, которые высматривают характерные признаки вирусов и бактерий. Среди них три особенно выделяются способностью вызывать сильный интерферонный ответ: Toll-подобный рецептор 3 (TLR3), обнаруживающий двуспиральную вирусную РНК; Toll-подобный рецептор 4 (TLR4), распознающий компонент бактериальной клеточной стенки; и путь cGAS–STING, реагирующий на чужеродную ДНК, оказавшуюся в неправильном месте внутри клетки. Все три активируют центральный фермент TBK1, который затем включает транскрипционный фактор IRF3, запускающий синтез интерферонов типов I и III. До настоящего времени было мало понятно, как эти сенсоры сходятся на TBK1, чтобы перевести его в активное состояние.
Скрытый молекулярный соединитель
Исследователи обнаружили, что белок ANKIB1 действует как ключевой соединитель между этими сенсорами и TBK1. ANKIB1 — фермент, который присоединяет к другим белкам небольшие молекулярные метки, так называемые цепочки убиквитина. Важно, что он собирает специфический тип цепочки, основанный на связи «K11», которая ранее была больше известна своей ролью в делении клетки, чем в иммунитете. В человеческих клетках, лишённых ANKIB1, стимуляция TLR3 или активация STING больше не приводила к правильной активации TBK1 и IRF3, и гены интерферонов практически не включались. Восстановление ANKIB1 возвращало ответ, что показывает — этот одиночный фермент необходим и достаточен для запуска этого ответа противовирусной тревоги.
Создание плацдарма для ретрансляционных белков
Более детальный анализ показал, как действует ANKIB1. При распознавании опасности TLR3 или STING собирают многобелковые платформы, называемые сигналосомами. ANKIB1 привлекается к этим платформам через участок, распознающий убиквитин. Оказавшись там, он модифицирует несколько ключевых компонентов — включая адаптерные белки TRIF и сам STING, а также другие сигнальные молекулы — цепочками убиквитина, связанными через K11. Эти цепочки не метят белки для разрушения; напротив, они действуют как молекулярный «липучка». Другой белок, оптионерин (OPTN), специфически притягивается к таким модифицированным участкам. Выступая в роли адаптера-ретранслятора, OPTN затем приносит TBK1 в комплекс, чтобы тот мог активироваться и передать сигнал далее к IRF3 и генам интерферонов. При удалении OPTN активация TBK1 разрушалась, что подчёркивает, что K11-связанное помечание ANKIB1 и связывание OPTN образуют единый, жизненно важный осевой путь.
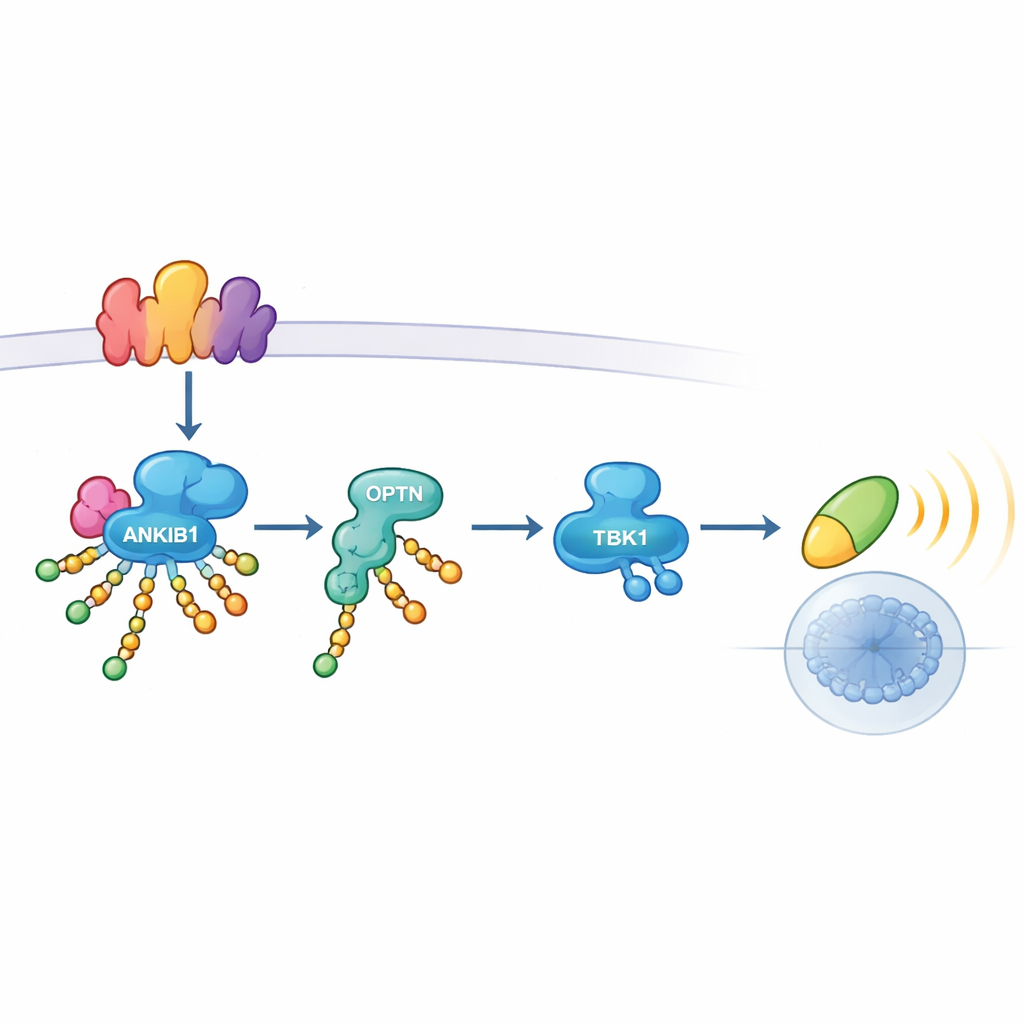
Когда этот путь важен — и когда нет
Далее команда исследовала, является ли этот механизм универсальным для всех противовирусных сенсоров. Оказалось, что ANKIB1 критически важен для индукции интерферонов через TLR3, TRIF-зависимую ветвь TLR4 и путь cGAS–STING — все они используют OPTN как основной адаптер для TBK1. Напротив, другой сенсор, RIG-I, распознающий вирусную РНК, опирается на другой набор адаптерных белков и не требует ANKIB1 или OPTN для активации TBK1. Эксперименты на мышах подтвердили эти клеточные данные. Животные без Ankib1 вырабатывали значительно меньше интерферона после активации TLR3 или STING, были защищены от летального воспалительного синдрома, вызванного избыточными интерферонами, но при этом становились гораздо более уязвимы к инфекции вирусом простого герпеса 1 — ДНК-вирусу, контроль над которым в значительной мере зависит от cGAS–STING-индуцированного интерферона. Реакции на вирус гриппа, который в основном распознаётся RIG-I, оставались в значительной степени сохранными.
Баланс между защитой и вредом
Вместе эти результаты выявляют K11-связанные цепочки убиквитина, создаваемые ANKIB1, как центральную «валюту» в важной ветви врождённого противовирусного сигнального пути. Создавая посадочные места для OPTN, ANKIB1 помогает собирать точную молекулярную ретрансляционную цепочку, которая превращает сигнал опасности, улавливаемый TLR3, TLR4 (через TRIF) и cGAS–STING, в мощное производство интерферонов. Эта ось двусторонняя: она необходима для защиты от некоторых вирусов, но также подпитывает интерферон-зависимое воспалительное заболевание при чрезмерной активации. Поскольку каталитическая активность ANKIB1 и его специфические домены требуются для этой функции, они представляют привлекательные мишени для будущих препаратов, направленных либо на ослабление вредных интерферонных ответов при аутоиммунных состояниях, либо на усиление противовирусного иммунитета там, где он недостаточен.
Цитирование: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Ключевые слова: врожденный иммунитет, сигналы интерферона, убиквитинирование, путь cGAS–STING, вирусная инфекция