Clear Sky Science · ru
Периопухолевая жировая ткань способствует уклонению от иммунного надзора при колоректальном раке через адипозно-мезенхимальную трансформацию
Почему подкожный жир вокруг опухолей имеет значение
Колоректальный рак растет в стенке кишечника, но соседствует с плотным слоем брюшного жира. Большинство людей воспринимает этот жир как пассивную прокладку. В этом исследовании обнаружено неожиданное явление: жир, окружающий опухоль, может тихо оттягивать противоопухолевые иммунные клетки от самой опухоли, помогая раку скрываться от иммунной системы. Понимание этой скрытой борьбы за клетки подсказывает новые способы предсказания ответа на иммунотерапию и методы повышения ее эффективности.
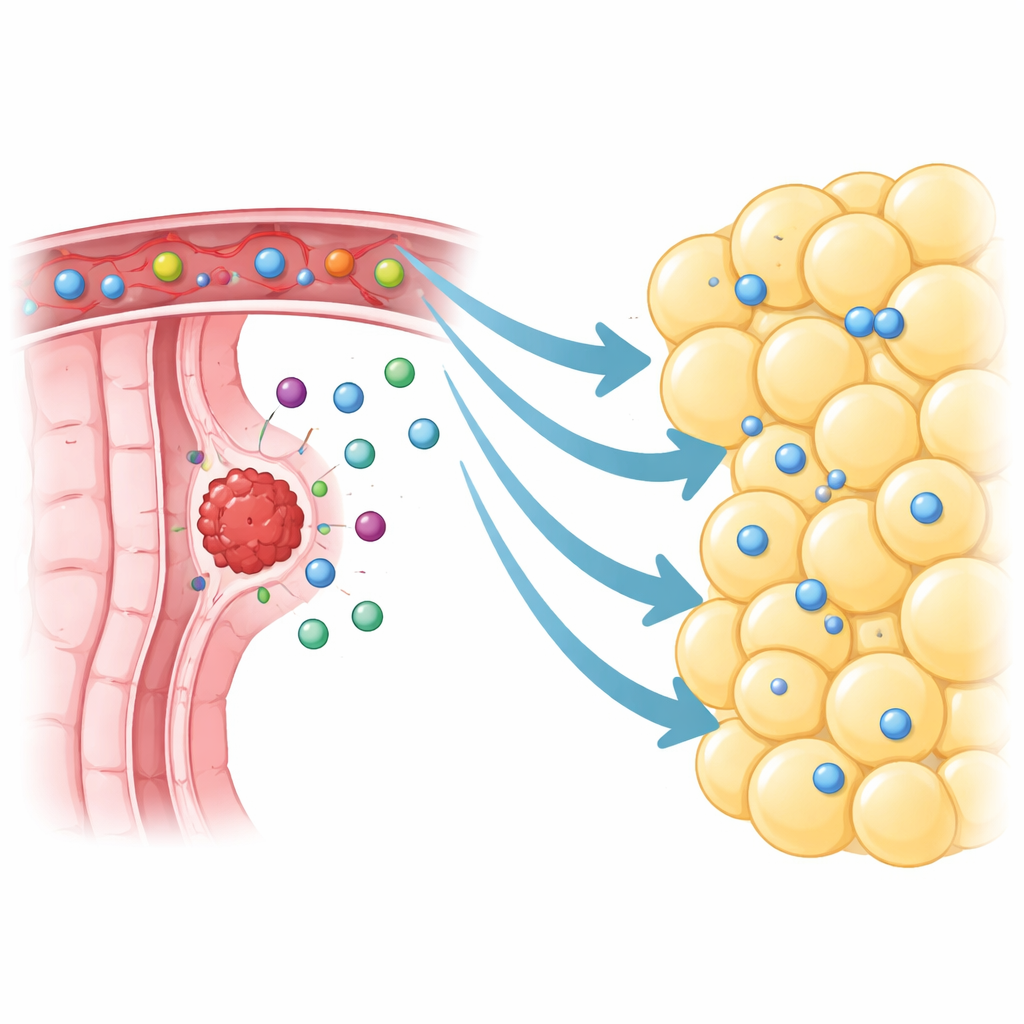
Оживленный иммунный район рядом с опухолью
Исследователи сосредоточились на висцеральной жировой ткани, непосредственно прилегающей к колоректальным опухолям, называемой периопухолевой висцеральной жировой тканью. С помощью секвенирования одиночных клеток (single-cell RNA sequencing) они картировали более 370 000 отдельных клеток из опухолей, ближнего жира, отдаленного жира и нормальной ткани. Вместо того чтобы быть спокойной и инертной, жир рядом с опухолями оказался наполнен иммунными клетками, особенно Т- и В-клетками. Они даже обнаружили организованные скопления, напоминающие мини-лимфатические узлы — признак того, что эта ткань может поддерживать активные иммунные реакции. По сравнению с более отдаленным жиром, периопухолевая жировая ткань содержала гораздо больше лимфоцитов, включая клетки памяти и опухолеспецифические цитотоксические Т-клетки, которые в принципе должны патрулировать в поисках рака.
Когда полезные иммунные клетки оказываются не в том месте
Чтобы понять, помогает ли этот богатый иммунной составляющей жир или мешает, команда использовала модели на мышах, где опухоли имплантировали рядом с жировой подушкой, напоминающей человеческий случай. Затем они хирургически удаляли этот близлежащий жир или химически его растворяли. Парадоксально, но удаление периопухолевого жира замедляло рост опухоли. У мышей, у которых убрали этот жир, в опухолях обнаруживалось больше CD4- и CD8-Т-клеток, включая Т-клетки, распознававшие опухолевые антигены. Дополнительные эксперименты с отслеживанием донорских иммунных клеток показали, что при наличии жира значительная часть этих клеток накапливалась в жировой подушке, а не в опухоли. Удаление жира перенаправляло клетки в опухоль, усиливая противораковый ответ. Другими словами, жир действовал как конкурентный резервуар, впитывавший иммунные клетки и мешавший им достичь настоящей цели.
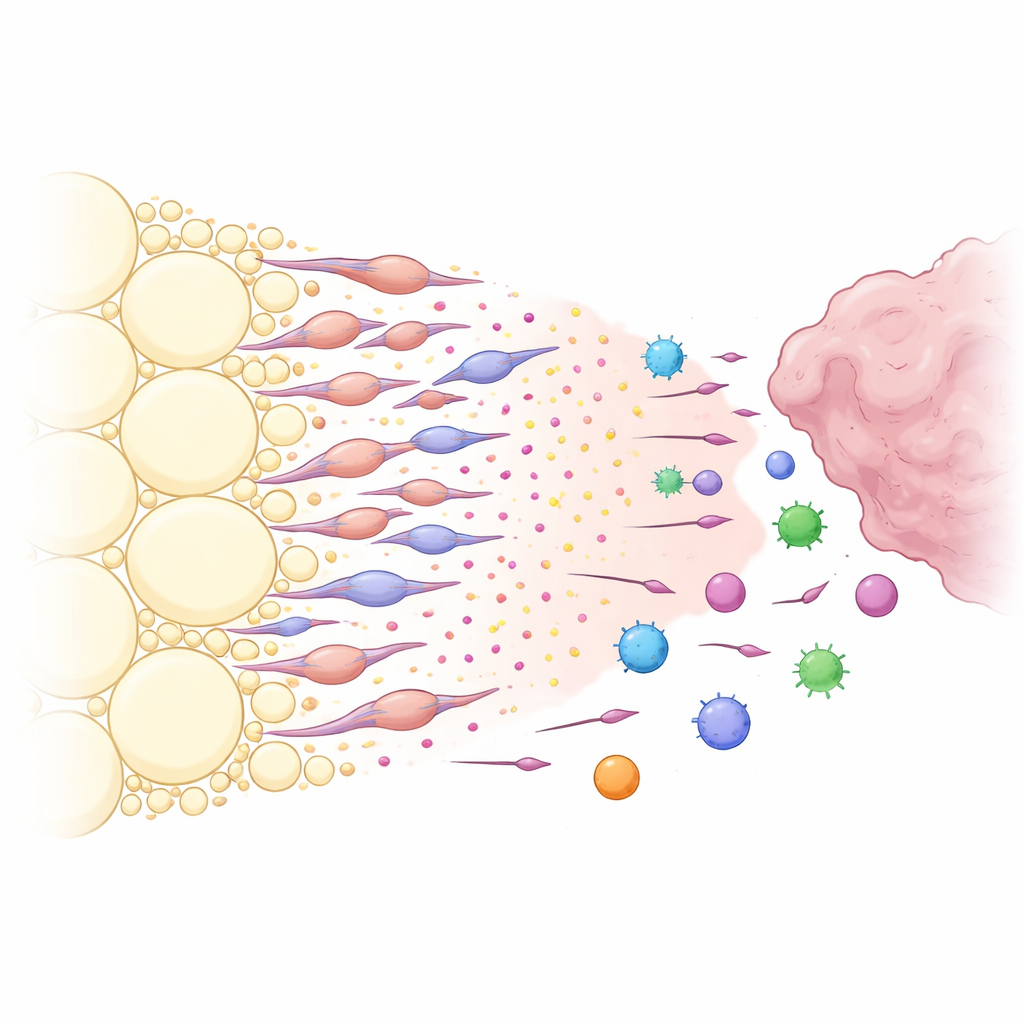
Химическая приманка, созданная трансформированными жировыми клетками
Почему же периопухолевая жировая ткань была столь эффективна в улавливании иммунных клеток? Анализ сигналов межклеточной коммуникации выявил мощный химический путь, центрированный вокруг молекулы CXCL12 и ее рецептора CXCR4. Стромальные клетки в жире рядом с опухолью продуцировали высокие уровни CXCL12, тогда как многие иммунные клетки экспрессировали CXCR4 и были восприимчивы к этому сигналу. Локальная блокада CXCL12 в жире или генетическое удаление его в строме жировой ткани приводили к уменьшению опухолей и позволяли большему числу CXCR4-положительных иммунных клеток проникать в опухоль, а не отклоняться. Команда затем обнаружила, что основными производителями CXCL12 были не обычные адипоциты, а специальная группа жировых клеток, преобразовавшихся в фибробластоподобные клетки, которую они назвали адипозо-ассоциированными фибробластами опухоли. Факторы, выделяемые опухолью, особенно ростовой фактор TGF-β1, заставляли местные стромальные клетки жировой ткани превращаться в эти фибробластоподобные клетки, которые в свою очередь секретировали большие количества CXCL12 и других сигналов, способствующих росту.
Преобразование щита в уязвимое место
Поскольку эти трансформированные клетки способствуют оттоку иммунных клеток от опухолей, исследователи проверили, улучшит ли разборка этого «иммунного стока» эффективность иммунотерапии. У мышей, у которых адипозо-ассоциированные фибробласты можно было избирательно устранить, лечение антителом, блокирующим PD-1, стало значительно более эффективным: опухоли росли меньше, а в опухоль проникавало больше опухолеспецифических и CXCR4-положительных Т-клеток. Аналогичным образом препараты или антитела, блокирующие либо CXCL12, либо его рецептор CXCR4, действовали синергетически с блокадой PD-1 в моделях колоректального рака как подкожных, так и ортотопических. Эти комбинации не только уменьшали размер опухолей, но и перестраивали иммунный ландшафт внутри опухоли.
Подсказки из сканирования пациентов и дальнейшие шаги
Затем команда выяснила, имеют ли их находки значение для реальных пациентов. В группе больных с локально распространенным колоректальным раком, получавших комбинированную химио- и радиотерапию вместе с PD-1-иммунотерапией, пациенты с полным ответом, как правило, имели меньший объем периопухолевой висцеральной жировой ткани на МРТ до лечения. В количественном выражении площадь этой жировой ткани предсказывала ответ на терапию лучше, чем некоторые стандартные тканевые маркеры, а у пациентов с большим объемом периопухолевого жира показатели ответа были значительно ниже. Для неспециалиста вывод впечатляет: важна не только сама опухоль, но и жир, непосредственно ее окружающий — он может определять, насколько эффективной будет иммунотерапия. Сфокусировавшись на этом жире — либо измеряя его для принятия решений о лечении, либо нацеливаясь на его трансформированные стромальные клетки и сигнал CXCL12–CXCR4 — возможно превратить защитный щит опухоли в терапевтическую уязвимость.
Цитирование: Wang, JH., Zheng, YQ., Qian, ZY. et al. Peritumoural adipose tissue drives immune evasion in colorectal cancer via adipose–mesenchymal transformation. Nat Cell Biol 28, 581–595 (2026). https://doi.org/10.1038/s41556-026-01885-0
Ключевые слова: колоректальный рак, опухолевый микросреда, висцеральный жир, иммунотерапия, CXCL12 CXCR4