Clear Sky Science · ru
Ремоделирование ЭПР — признак старения и зависит от ER‑фagии
Почему внутренние складки клетки важны с возрастом
Клетки в наших организмах полны сетью мембран, напоминающей лабиринт, — эндоплазматическим ретикулумом (ЭПР). Эта структура помогает синтезировать липиды и белки, управлять сахаром и кальцием и постоянно «переговаривается» с другими клеточными компонентами. Поскольку через эту сеть проходит множество ключевых процессов, любое долгосрочное изменение формы и объёма ЭПР может повлиять на старение тканей, их устойчивость к стрессу и, в конечном счёте, на продолжительность здоровой жизни. В этом исследовании поставлен на первый взгляд простой вопрос: стареется ли сам ЭПР упорядоченно и специфически, и если да, то является ли это вредным износом или встроенной стратегией защиты?
Скрытое смещение в «мастерской» клетки
Используя современные микроскопы и флуоресцентные метки в крошечной нематоде Caenorhabditis elegans, авторы отслеживали ЭПР в живых животных по мере их перехода от молодой взрослости к старости. В молодых клетках ЭПР образует широкие, уложенные в стопки пластины с аппаратом синтеза белка, напоминая аккуратно организованные производственные цеха. По мере старения у нематод эти пластины уменьшаются в объёме и уступают место более тонкой, трубчатой сети, занимающей меньше пространства. Измерения показали, что общий содержательный объём ЭПР заметно сокращается, а его форма меняется — что указывает не просто на случайные повреждения, а на координированное уменьшение и переконфигурацию органеллы.
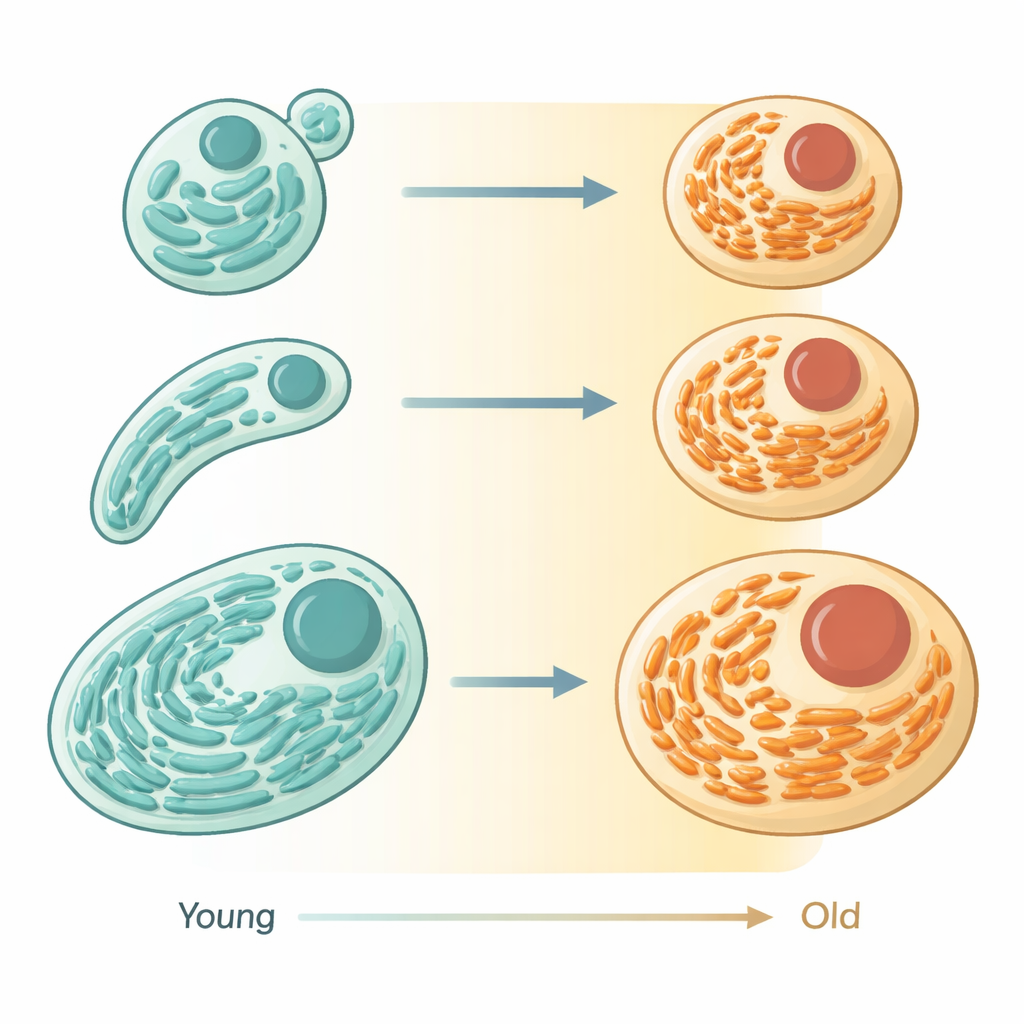
От производства белков к управлению липидами
Форма в биологии часто сигнализирует о функции — и здесь это подтвердилось. Исследователи сравнили, как со временем меняются белки, связанные с ЭПР, в разных тканях нематод. Белки, участвующие в синтезе, свёртывании и контроле качества других белков, снижались с возрастом параллельно утрате пластинчатого ЭПР. Напротив, многие белки ЭПР, связанные с метаболизмом липидов и мембран, оставались на прежнем уровне или даже возрастали. В совокупности эти закономерности свидетельствуют о том, что стареющие клетки сокращают массовое производство белков и перераспределяют ресурсы ЭПР в пользу управления липидами и мембранами. Примечательно, что при анализе больших наборов данных по стареющим мышам наблюдалась аналогичная картина: белки ЭПР, связанные с секрецией и обработкой белков, как правило, снижались, тогда как компоненты, вовлечённые в липидный обмен и аутофагию, относительно сохранялись или увеличивались.
Клеточный маршрут переработки как причина ремоделирования
Что инициирует это масштабное перераспределение? Команда связала изменения с ER‑фагией — формой селективного самопоедания, при которой клетка упаковывает фрагменты ЭПР в везикулы для утилизации в лизосомах. Блокирование ключевых генов аутфагии у нематод предотвращало нормальную возрастную потерю массы ЭПР и сдвиг от пластин к трубочкам, показывая, что этот путь переработки не просто убирает мусор, а активно формирует органеллу. Независимые эксперименты на дрожжах подтвердили, что компоненты ЭПР перенаправляются в клеточный «центр переработки» по мере старения, также в зависимости от аутфагии. Электронная микроскопия выявила фрагменты ЭПР внутри дегенеративных компартментов, что служит физическим доказательством целенаправленного удаления частей сети.

Тканеспецифическое управление общим программой старения
Хотя ремоделирование ЭПР наблюдалось во множестве тканей нематод — кишечнике, гиподермисе, мышцах и нейронах — триггеры оказались тканеспецифичными. В гиподермисе ранее малоизвестный мембранный белок TMEM‑131 связывал turnover ЭПР с обработкой коллагена. При снижении уровня TMEM‑131 возрастная потеря ЭПР в этой ткани в значительной мере предотвращалась, что подразумевает: ЭПР уменьшается, когда сокращается число его «клиентов» — коллагеновых молекул. В кишечнике, напротив, ключевым регулятором была ветвь ответа на накопление неСВЁРНУТЫХ белков IRE‑1–XBP‑1 — центральный путь обнаружения стрессов. Подавление этого сигнального звена сохраняло кишечный ЭПР при старении, что говорит о том, что в этом органе сигналы стресса ЭПР помогают решать, когда жертвовать его частями.
Перенастройка ЭПР ради более долгой жизни
Исследование также связывает ремоделирование ЭПР с долголетием. У нематод несколько известных вмешательств, увеличивающих продолжительность жизни — ослабление инсулиноподобной сигнализации, подавление мишени рапамицина (mTOR), удаление зародышевой линии или небольшое замедление синтеза белка — вызывали уменьшение ЭПР и увеличение доли трубчатой сети уже в ранней взрослости, а не только в старости. Важно, что при выключенной ER‑фагии продлённая жизнь, обычно вызываемая ингибированием mTOR у дрожжей и нематод, значительно сокращалась или исчезала. Это указывает на то, что тщательно контролируемая «подрезка» ЭПР — не просто побочный эффект старения или терапии, а один из механизмов, с помощью которых клетки достигают более устойчивого состояния.
Что это значит для здорового старения
На первый взгляд потеря значительной части ключевой клеточной структуры с возрастом может показаться исключительно вредной. Работа, описанная здесь, рисует более тонкую картину. Похоже, что ЭПР активно перестраивается — посредством селективного самопоедания и тканеспецифических регуляторов — так, чтобы стареющие клетки производили меньше новых белков, больше инвестировали в управление липидами и мембранами и, возможно, уменьшали риск хронического стресса. Это ремоделирование консервативно от дрожжей до млекопитающих и необходимо для по крайней мере некоторых форм продления жизни. Однако в долгосрочной перспективе уменьшение ЭПР может иметь компромиссы, влияя на способность клеток ремонтировать другие органеллы и справляться с позднесрочной деградацией. Выявляя ER‑фагию и динамику ЭПР как ключевые черты нормального и замедленного старения, это исследование подчеркивает новый набор рычагов, которые когда‑нибудь можно будет настраивать для поддержания более здоровых и устойчивых тканей.
Цитирование: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
Ключевые слова: эндоплазматический ретикулум, аутфагия, клеточное старение, гомеостаз белков, метаболизм липидов