Clear Sky Science · ru
Функциональная геномика с разрешением по времени с применением глубокого обучения выявляет глобальный иерархический контроль аутофагии
Как клетки перерабатывают себя — и знают, когда остановиться
Наши клетки переживают голодные периоды, перерабатывая собственные компоненты в процессе, называемом аутофагией — буквально «самопоедание». Слишком мало переработки ведёт к накоплению повреждённых структур; слишком много — к самопожиранию клетки. В этом исследовании поставлен на вид казалось бы простой, но важный вопрос для старения и болезней: как живая клетка включает и выключает аутофагию в нужные моменты при изменении уровня питательных веществ?
Наблюдая за тысячами клеток в цикле от обилия к голоду
Чтобы ответить, исследователи использовали пекарские дрожжи как модель и наблюдали почти шесть тысяч различных мутантных штаммов в условиях голодания и восстановления. Каждый штамм нес флуоресцентные метки, помечающие структуры, связанные с аутофагией, что позволило мощному микроскопу снимать изображения каждый час при удалении и последующем восстановлении питательных веществ. Вместо ручной сортировки изображений команда обучила алгоритмы глубокого обучения распознавать, когда клетка находится в состоянии аутофагии, опираясь исключительно на признаки изображения, а не на человеческую интерпретацию. Это дало точные временные кривые активности аутофагии почти для всего генома дрожжей, показав, как быстро и с какой интенсивностью каждый мутант реагировал на смену питания. 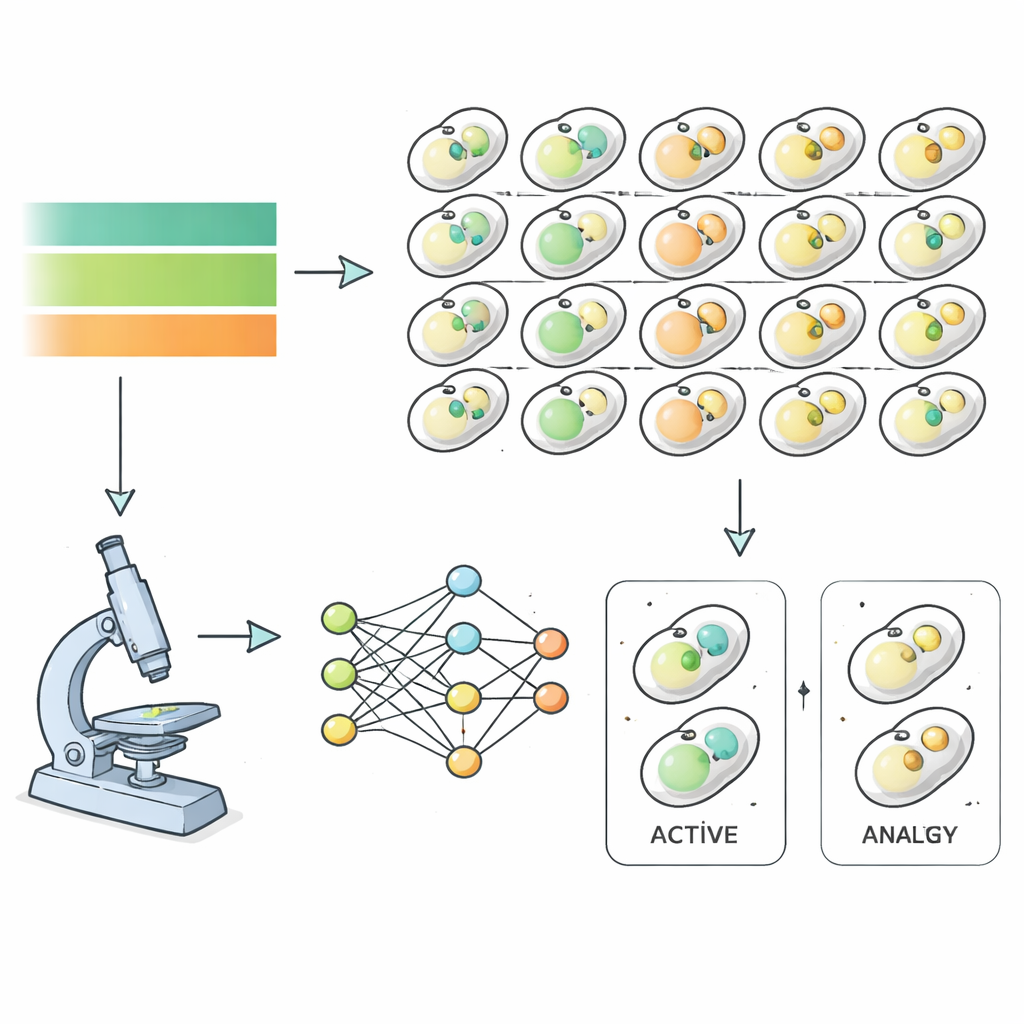
Шесть различных способов, которыми клетки некорректно управляют переработкой
Математически аппроксимируя эти временные кривые, авторы извлекли детальные «кинетические отпечатки» для каждого мутанта — как быстро включалась аутофагия, как долго она оставалась высокой и насколько резко выключалась. Кластеризация этих сигнатур выявила шесть широких типов поведения. Некоторые мутанты были «ультрачувствительными», быстро реагируя и на голод, и на возвращение питательных веществ. Другие — «гипочувствительными», реагировали вяло. Группа «гиперактивных» показывала аномально высокий базовый уровень переработки, тогда как несколько групп демонстрировали различную степень неспособности адекватно ответить вообще. Важно, что известные ключевые гены аутофагии попали в наиболее тяжёлые классы, что подтверждает: метод отражает реальную биологию, а не шум измерений.
Картирование иерархии контроля над аутофагией
Аутофагия не происходит в изоляции; она встроена в более широкие регуляторные сети клетки. Команда наложила свои динамические профили на большие карты генетических и белковых взаимодействий у дрожжей. Гены, потеря которых приводила к сильным дефектам аутофагии, как правило, располагались близко к известной «основной машине» аутофагии в этих сетях, в то время как более тонкие мутанты находились дальше, что согласуется с более опосредованным контролем. Анализ обогащённых в каждом классе клеточных процессов показал, что активация, вызванная голодом, сильно формируется путями, связанными с РНК, белковым синтезом и энергетическим обменом, тогда как выключение аутофагии после восстановления питательных веществ больше зависит от мембранного трафика и шагов слияния, которые очищают везикулы переработки.
Углублённый взгляд на формирование и очистку везикул
Аутофагия проходит через две основные стадии: формирование везикул с грузом и их слияние с компартментом клетки для разложения. Чтобы детально изучить эти этапы, исследователи проанализировали «латентное пространство» внутри своей нейронной сети — сжатое представление, которое сеть использует для различения изображений. Проецируя это внутреннее представление на двумерную карту, они могли наблюдать, как популяции клеток перемещаются из области без везикул через область с многочисленными свободными везикулами и, наконец, в область, где везикулы были очищены. Сравнивая статистически с референсными мутантами, «запертыми» на разных стадиях, они количественно определили для каждого гена, влияет ли он преимущественно на формирование везикул, на их очистку или на оба процесса. Анализ показал, что контроль формирования везикул сильно чувствителен к уровням азота во времени, тогда как механизмы очистки ведут себя более стабильно и часто являются основным лимитирующим фактором общего потока переработки. 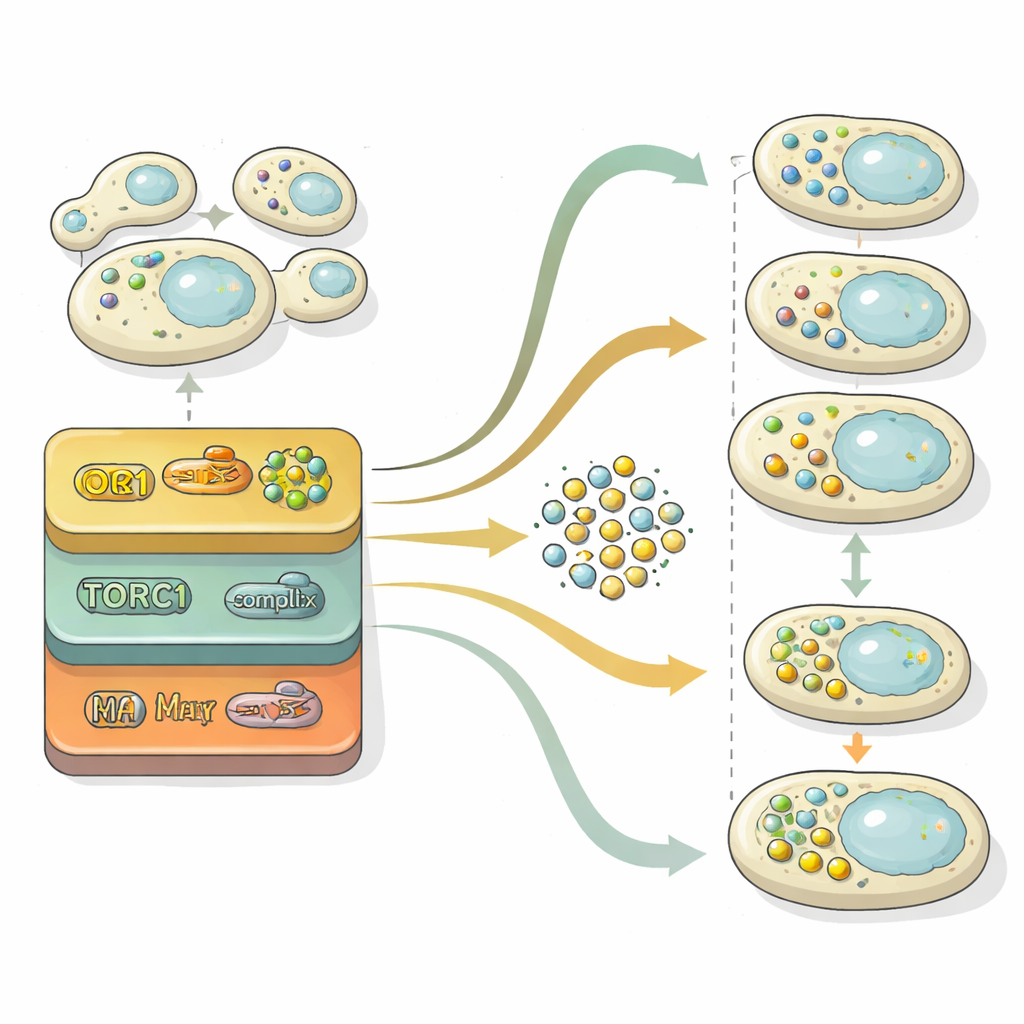
Скрытый тормоз переработки: ретроградный путь
Одно из самых впечатляющих открытий касалось так называемого ретроградного (RTG) пути, который передаёт сигналы от митохондрий к ядру. Дрожжевые клетки, лишённые компонентов RTG, образовывали слишком много аутофагосом даже при изобилии питательных веществ и испытывали трудности с их устранением после возвращения питательных веществ. Детальные дополнительные эксперименты показали: этот путь контролирует экспрессию ключевых генов аутофагии, особенно главного инициатора ATG1, во многом независимо от хорошо известного сенсора питательных веществ TORC1, на который действуют такие препараты, как рапамицин. По сути, сигналы RTG выступают в роли временно изменяющегося тормоза, который предотвращает неконтролируемую аутофагию в условиях изобилия и помогает завершить ответ, когда условия улучшаются.
Почему это важно для здоровья и терапии
В целом эта работа предоставляет геномную карту с разрешением по времени того, как клетки настраивают аутофагию при изменяющихся питательных условиях. Показано, что активация и выключение не являются симметричными: гораздо больше генов влияет на запуск переработки, чем на её остановку, а долгосрочное равновесие во многом зависит от очистки везикул и транскрипционных тормозов, таких как RTG-путь. Для широкого читателя основной вывод таков: клеточное самопоедание находится под многослойным иерархическим контролем, и теперь мы можем с высокой точностью картировать эти уровни. Такой системный взгляд в перспективе может помочь в разработке более тонких терапий, которые регулируют аутофагию на конкретных этапах — усиливают полезную переработку, не вызывая вредных эффектов хронического неконтролируемого самопереваривания.
Цитирование: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Ключевые слова: аутофагия, глубокое обучение, генетика дрожжей, сенсорика питательных веществ, клеточный рецирклинг