Clear Sky Science · ru
Уточнённый фенотипирование ответов на вакцину выявляет транскриптомные детерминанты гетерогенности нейтрализующих антител
Почему одни вакцины работают лучше для некоторых людей
Когда мы делаем прививку от COVID-19, можно предположить, что иммунная система у всех реагирует одинаково. На деле люди сильно различаются по скорости и силе выработки защитных антител. В этом исследовании наблюдали взрослых, получивших инактивированные вакцины против SARS-CoV-2, и показали, что ответы на вакцину группируются в отдельные паттерны, каждый из которых определяется различными ранними иммунными сигналами, зафиксированными в генах и клетках крови. Понимание этих паттернов могло бы в будущем помочь адаптировать графики вакцинации, чтобы каждый получил нужную защиту.
Три пути к защите после одной и той же прививки
Исследователи отслеживали 73 здоровых взрослых, получивших две дозы инактивированной вакцины против COVID-19. Они измеряли нейтрализующие антитела — те, что способны блокировать вирус — до вакцинации, через неделю после второй дозы и снова примерно через месяц. Вместо простого деления людей на «высоких» и «низких» ответчиков, использовали методы, опирающиеся на данные, чтобы сгруппировать участников по тому, как менялись уровни антител со временем. Выявились три чётких паттерна: группа «низкая‑задержанная» с медленным и скромным ростом антител; группа «быстро‑стабилизирующаяся», у которой уровень антител быстро подскакивал, а затем выравнивался; и группа «постоянного роста», у которой антитела продолжали нарастать до наивысших значений. Эти паттерны не объяснялись возрастом, полом или массой тела и лишь частично зависели от марки инактивированной вакцины.
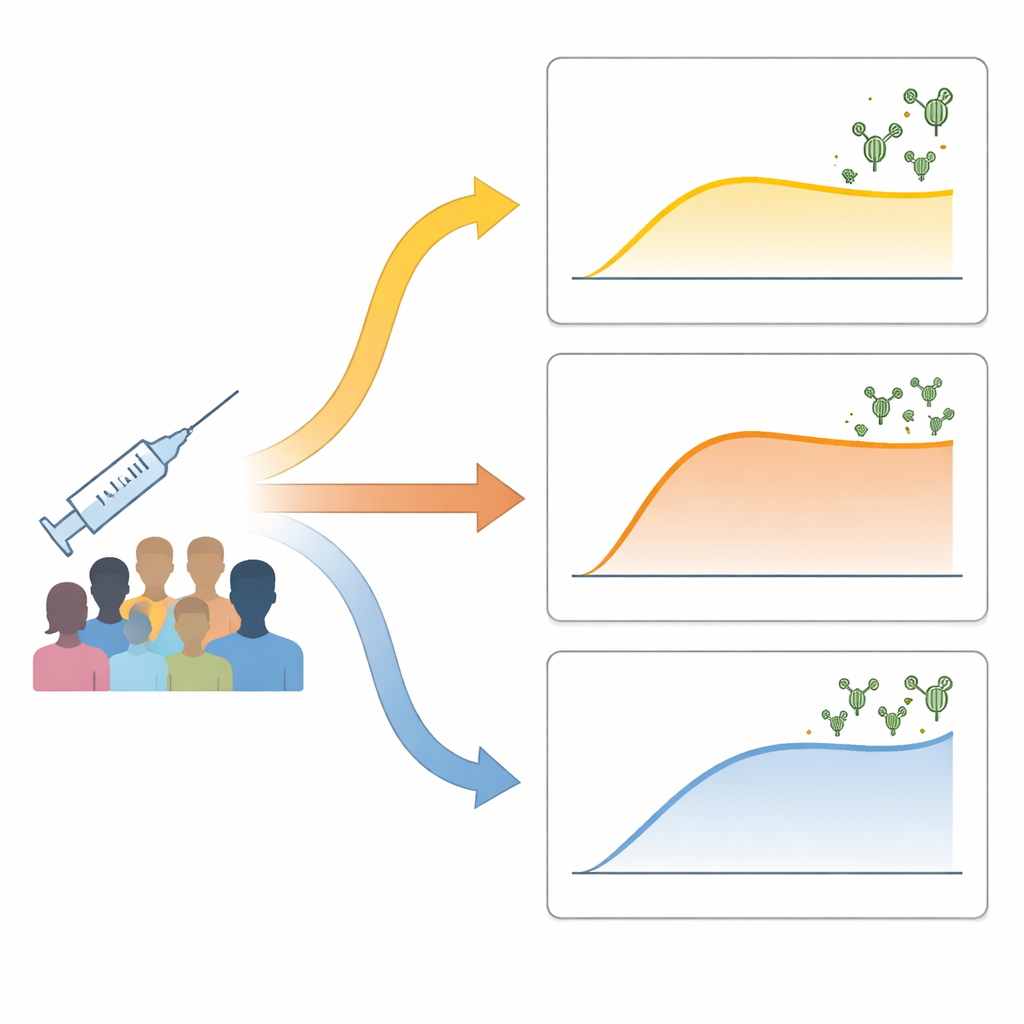
Как ранняя иммунная активность формирует исход
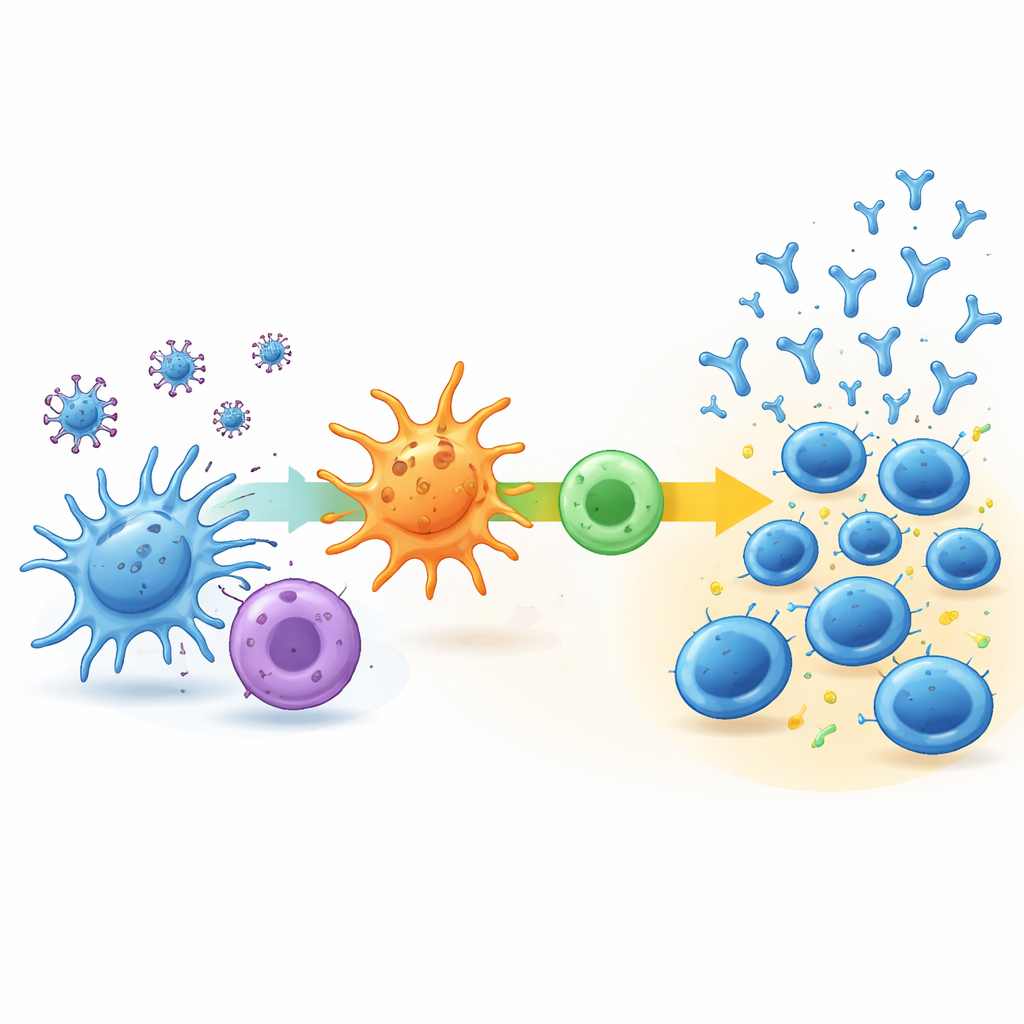
Чтобы понять, что определяет эти разные траектории, команда проанализировала генетическую активность иммунных клеток в крови в исходной точке и через неделю после второй прививки. В группе низкая‑задержанная почти ничего не менялось: ключевые иммунные пути были едва активированы, а состав типов иммунных клеток в крови оставался по сути тем же. Напротив, у групп быстро‑стабилизирующейся и постоянного роста наблюдались явные признаки ранней иммунной активации. У сильнейших ответчиков отмечалась скоординированная активность путей, обрабатывающих фрагменты вируса, представляющих их другим иммунным клеткам и поддерживающих тип хелперных Т‑клеток, известный своей ролью в усилении продукции антител. У этих людей также было больше наивных B‑клеток и хелперных T‑клеток, готовых к ответу, а позднее они демонстрировали несколько более сильную вирус‑специфическую T‑клеточную активность.
Скрытые уровни регуляции в РНК и B‑клетках
Помимо простых включений и выключений генов, учёные изучили более тонкие уровни регуляции, заложенные в РНК — промежуточных молекулах между ДНК и белком. В группе с наилучшим ответом иммуноучаствующие гены, вовлечённые в представление вирусных фрагментов иммунной системе, показывали различные шаблоны «сплайсинга» и более короткие хвостовые регионы в конце их РНК. Эти признаки считаются такими, что облегчают синтез определённых белков и поддерживают сильную сигнализацию. Команда также реконструировала репертуар рецепторов B‑клеток — уникальных «антенн» на клетках, продуцирующих антитела — из тех же образцов крови. Несмотря на то, что общая диверсификация выглядела схожей между группами, каждый паттерн ответа использовал слегка разные комбинации и формы этих рецепторов, и сильнейшие ответчики предпочитали типы рецепторов, ранее связанные с мощными антителами против спайкового белка коронавируса.
Выявление потенциальных низких ответчиков до вакцинации
Поскольку люди из группы низкая‑задержанная могут хуже защищаться после стандартной схемы вакцинации, исследователи проверили, можно ли заранее их отфильтровать. Они сосредоточились на небольшом наборе генов, которые в исходном состоянии умеренно различались между самыми слабыми и самыми сильными ответчиками. С помощью методов машинного обучения они создали модель, основанную всего на восьми генах, измеренных до вакцинации. Эта модель могла с высокой точностью отличать низкая‑задержанных ответчиков в их наборе данных; два гена, вовлечённые в базовую клеточную сигнализацию и воспаление, вносили наибольший вклад в предсказательную силу. Хотя эту работу нужно проверить на больших и более разнообразных популяциях, она указывает на то, что простой анализ крови однажды сможет направлять более персонализированные планы вакцинации.
Что это значит для будущих вакцин
В целом исследование показывает, что люди не просто демонстрируют «сильные» или «слабые» антительный ответы; они следуют разным временным траекториям, сформированным ранними, трудноуловимыми иммунными событиями. Наиболее защищённые индивиды активируют скоординированные сети генов и клеток, которые помогают быстро распознать вакцину и сформировать прочные антитела, тогда как низкие ответчики показывают приглушённую раннюю реакцию. Картируя эти внутренние различия и создавая инструменты для прогнозирования, кто ответит слабо, работа закладывает основу для персонализированной вакцинации — например, более ранние бустеры или альтернативные формулы для групп риска — чтобы обещание вакцин стало доступным более равномерно.
Цитирование: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
Ключевые слова: ответы на вакцину, нейтрализующие антитела, вакцинация против COVID-19, иммунная гетерогенность, персонализированные вакцины