Clear Sky Science · ru
Аджювант для усиления перекрестной презентации антигена в противораковой вакцине для расширения Т‑клеток и синергии с анти‑PD‑1
Превращение иммунной системы в точный инструмент борьбы с опухолью
Раковые вакцины часто описывают как способ «обучить» иммунную систему распознавать и уничтожать опухоли, но на практике они редко оправдывают эти ожидания. В этом исследовании рассматривается новый подход к «суперзарядке» таких вакцин, чтобы они могли вызывать более сильные и длительные цитотоксические T‑клеточные ответы и лучше работать в сочетании с популярными препаратами иммунотерапии, такими как анти–PD‑1. Для читателей, интересующихся тем, как завтра могут комбинироваться биологические препараты, вакцины и иммунная инженерия, эта работа даёт представление о том, какой может быть следующая генерация высокоточной иммунотерапии.
Почему раковым вакцинам нужен более мощный «тыл»
Терапевтические раковые вакцины нацелены не на профилактику, а на лечение уже существующих опухолей, стимулируя сильные опухолепецифичные иммунные ответы. Ключевые игроки — CD8 «киллерные» T‑клетки, которые могут распознавать и разрушать раковые клетки, на поверхности которых представлены характерные антигены. К сожалению, опухолевые антигены слабо стимулируют иммунитет, поскольку в основном представляют собой изменённые версии собственных белков организма. Постоянное воздействие во время развития рака также может приводить к истощению или толерантности T‑клеток, ослабляя эффект вакцины. Чтобы преодолеть это, вакцины должны сочетаться с адъювантами — вспомогательными компонентами, которые активируют врождённый иммунитет, улучшают презентацию антигенов и формируют большой и устойчивый пул опухолепецифичных T‑клеток.
Гибридный иммуностимулятор, собранный из двух мощных сигналов
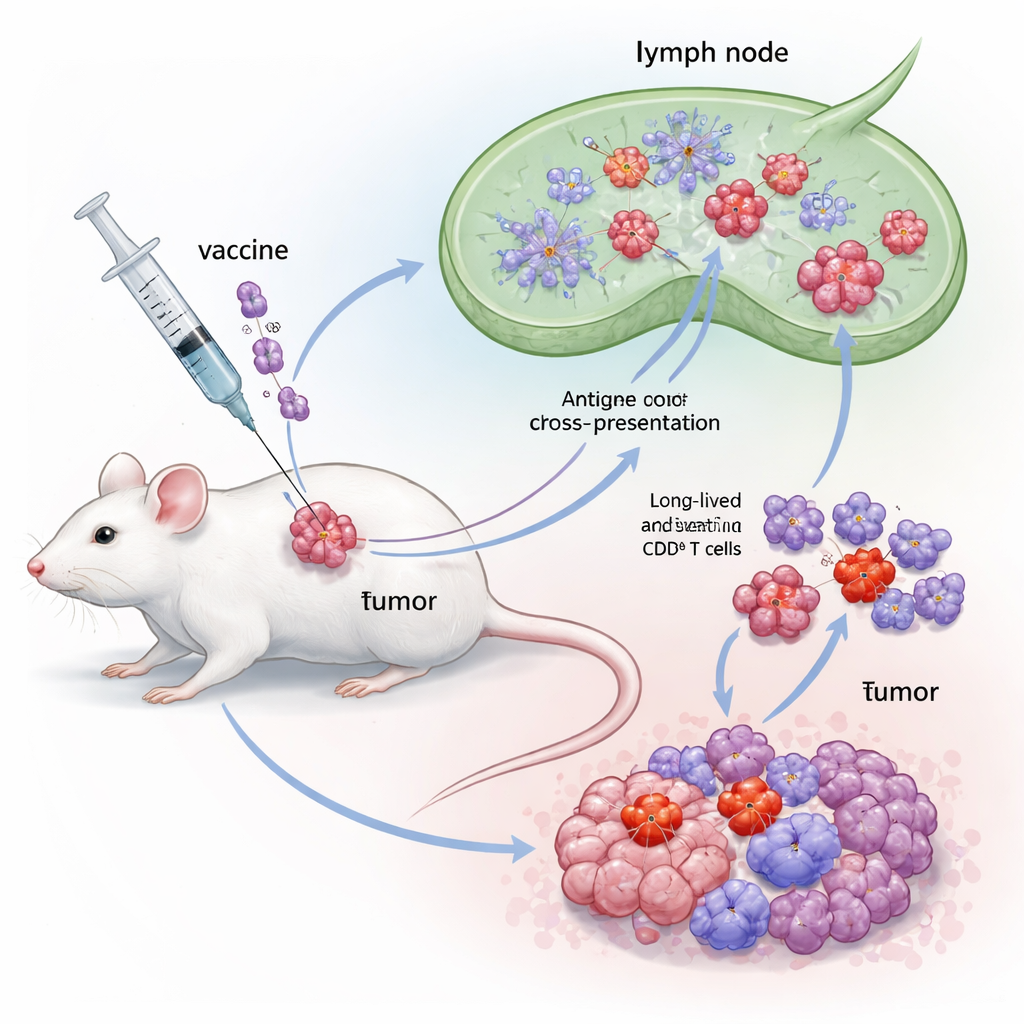
Исследователи разработали гибридный адъювант под названием Flt3L‑FlaB, или FB, объединив два иммуностимулирующих молекулы в один белок. Одна часть, Flt3L, — естественный фактор роста, расширяющий специализированную группу дендритных клеток, известных как cDC1. Эти клетки особенно хорошо выполняют «перекрёстную презентацию» — захваченные фрагменты опухолевого материала они показывают CD8‑клеткам так, чтобы вызвать сильный ответ. Другая часть, FlaB, представляет собой фрагмент бактериального флагеллина, который активирует врождённый сенсор TLR5 и служит мощным сигналом опасности. Объединив их, авторы стремились одновременно расширить cDC1 и перевести их в высокоактивное состояние, улучшив презентацию опухолевых антигенов T‑клеткам и продлив длительность этой стимуляции.
Испытание нового адъюванта в моделях опухолей
Для проверки FB команда использовала хорошо зарекомендовавшую себя мышиную модель опухоли на основе клеток, запрограммированных нести онкопротеины человека папилломавируса (ВПЧ). Мышам сначала имплантировали небольшую опухоль, затем вводили терапевтическую вакцину с антигеном E7 ВПЧ в сочетании либо с одним Flt3L, либо с FlaB, либо с новым фьюжн‑белком FB. Все вакцины вводили рядом с опухолью. В то время как каждый из одиночных адъювантов замедлял рост опухоли в некоторой степени, вакцина на основе FB выделялась: она значительно замедляла прогрессию опухоли, продлевала выживаемость и у заметной доли животных полностью устраняла опухоль. Иммунные анализы показали, что вакцинация с FB вызвала необычно сильные E7‑специфичные CD8‑ответы в крови, лимфоузлах и селезёнке, с высоким уровнем интерферона‑гамма и активной пролиферацией T‑клеток — доказательство того, что фьюжн не просто суммировала эффекты своих двух компонентов.
Формирование стойкой иммунной памяти и лучший партнёр для анти–PD‑1
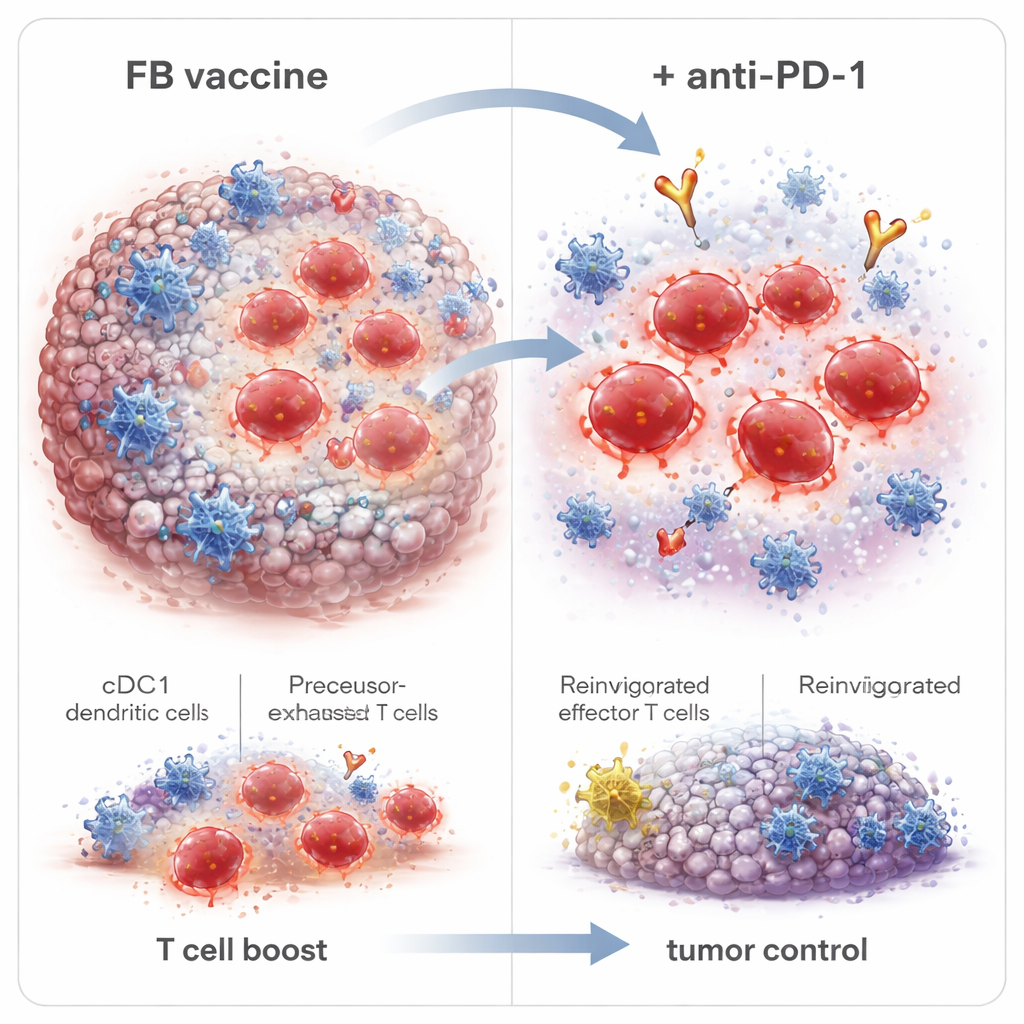
Глубже изучая механизм, учёные обнаружили, что FB меняет не только количество CD8‑клеток, но и их типы. Он усиливал как короткоживущие эффекторные клетки, атакующие опухоль немедленно, так и клетки‑предшественники памяти и «стволовоподобные» клетки памяти, которые могут сохраняться и отвечать повторно в будущем. Важно, что FB также расширял группу так называемых предшественников истощённых T‑клеток (Tpex) в опухоли — клеток, находящихся на грани между истощением и полноценной активностью и особенно чувствительных к анти–PD‑1 препаратам. Когда выживших животных повторно подвергали воздействию высокого числа опухолевых клеток спустя долгое время после вакцинации, большинство сопротивлялось росту новой опухоли, что свидетельствует о прочной иммунной памяти. Блокирование выхода иммунных клеток из лимфатических узлов устраняло преимущества FB, что указывает на то, что опухоль-убийственные T‑клетки формировались в этих узлах при участии cDC1, а затем мигрировали в опухоль.
Сильнее вместе: вакцины плюс блокада контрольных точек
Поскольку терапия анти–PD‑1 работает лучше, когда уже существует пул отзывчивых T‑клеток, команда объединила вакцинацию с адъювантом FB и антителом анти–PD‑1. В модели ВПЧ‑опухоли добавление анти–PD‑1 к вакцинации с FB ещё более замедляло рост опухоли, увеличивало долю животных, полностью избавившихся от рака, и обеспечивало полную защиту при чрезвычайно высокой дозе повторного введения опухолевых клеток. Важно было правильно выбрать временную последовательность: начало терапии анти–PD‑1 после второй, а не первой дозы вакцины умеренно улучшало полную эрадикацию опухоли, что согласуется с необходимостью дождаться расширения Tpex‑клеток. Адъювант FB также улучшал ответы на пептидные вакцины, включая опухолепецифичные неоантигены в модели рака толстой кишки, что указывает на то, что эта стратегия может иметь более широкое применение, выходя за пределы заболеваний, связанных с ВПЧ.
Что это может означать для будущего онкологической помощи
Для неспециалистов главный вывод таков: эта работа уточняет, как «обучать» иммунную систему бороться с раком. Комбинируя фактор роста дендритных клеток с мощным сигналом опасности в одном стабильном белке, адъювант FB увеличивает количество нужных клеток‑презентёров антигена, помогает им эффективнее демонстрировать опухолевые антигены и формирует популяцию киллерных T‑клеток, которые одновременно мощны сейчас и готовы ответить на последующую терапию контрольными точками. Хотя эти результаты получены на мышах и до применения у людей ещё много шагов, исследование очерчивает ясную дорожную карту: более умные адъюванты, координирующие перекрёстную презентацию и «стволовость» T‑клеток, могут сделать терапевтические раковые вакцины значительно более эффективными партнёрами для препаратов вроде анти–PD‑1, что потенциально приведёт к более глубокому и длительному контролю опухоли у пациентов.
Цитирование: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
Ключевые слова: раковые вакцины, иммунотерапия, дендритные клетки, блокада PD‑1, опухоли, связанные с ВПЧ