Clear Sky Science · ru
Универсальная широкоспектровая мукозальная вакцина против человеческих коронавирусов, вдохновлённая искусственными антителами
Почему всё ещё важна лучшая вакцина против коронавируса
Хотя COVID-19 всё больше принимает сезонный характер, продолжают появляться волны новых вариантов, и несколько других человеческих коронавирусов по-прежнему вызывают серьёзные заболевания. Нынешние вакцины неплохо защищают от тяжёлого течения, но менее эффективны в предотвращении заражения и передачи, особенно в носоглотке — там, где вирусы сначала закрепляются. В этом исследовании описывается новый тип интраназальной вакцины, вдохновлённый инженерными антителами, которая нацелена на долговременную, широкую защиту от многих коронавирусов на мукозальном рубеже организма.
Создание более умного каркаса вакцины
Исследователи начали с хорошо знакомой молекулы: человеческого IgG1, основного типа антител, используемого во многих одобренных антителесодержащих препаратах. Они переработали тяжёлую цепь так, чтобы она могла служить гибким «каркасом» для представления рецептор-связывающих доменов (RBD) спайкового белка коронавируса — тех частей, которыми вирус захватывает наши клетки. Удалив обычную лёгкую цепь и введя определённые мутации, учёные снизили связывание с иммунными рецепторами, связанными с побочными эффектами, такими как цитокиновые штормы, и усилили связывание с неонатальным Fc-рецептором (FcRn). FcRn широко представлен на мукозальных поверхностях и помогает переносить антитела через барьер и дольше сохранять их. На оптимизированный каркас команда прикрепила один, два, три или четыре разных RBD от SARS, MERS, сезонных коронавирусов и нескольких вариантов SARS‑CoV‑2, включая линии Омикрон, создав моно-, би-, три- и тетравалентные кандидаты вакцин.
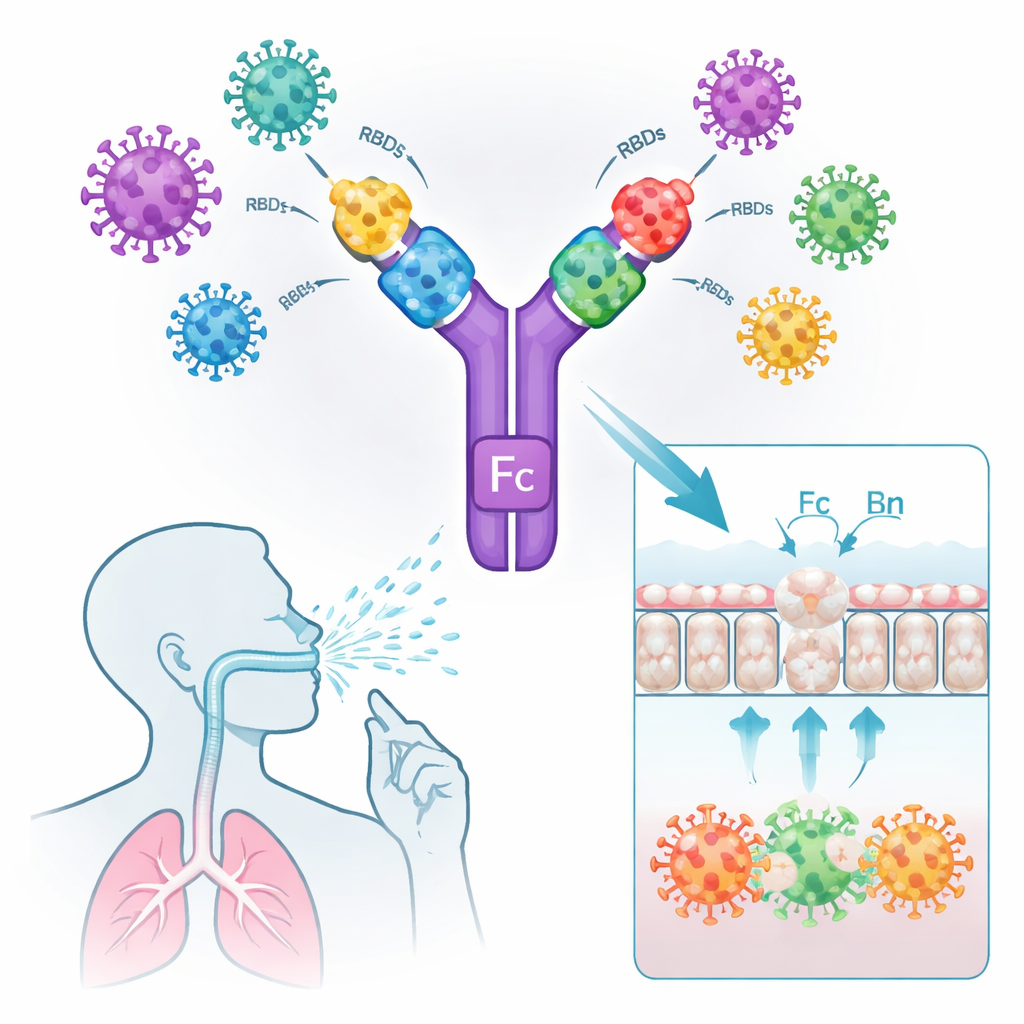
Пересечение мукозального барьера и активация местной защиты
Чтобы работать как назальный спрей, антигены вакцины должны достигать и задерживаться на эпителии дыхательных путей и эффективно распознаваться иммунными клетками. В культурах клеток конструкции с Fc сильно связывались как с ACE2 (рецептором для входа SARS‑CoV‑2), так и с человеческим или мышиным FcRn и активно транспортировались через слой мукозальных клеток. Похожий RBD-димер без Fc не смог пройти через этот слой. Когда флуоресцентные версии вакцин вводили в нос мышам, антигены с Fc сохранялись в лёгочной слизистой часами, тогда как «голый» RBD-димер быстро исчезал. Микроскопия показала, что модифицированные Fc-вакцины привлекали и активировали антиген-презентирующие клетки непосредственно под мукозальной поверхностью, о чём свидетельствовали повышенные уровни маркера иммунитета CD80 и колокализация с FcRn.
Усиление антител и Т-клеток там, где это нужно
Затем команда сравнила иммунные ответы после внутримышечной инъекции и интраназальной доставки у мышей. Во многих составах вакцины на основе Fc вызывали очень высокий уровень IgG в крови как против исходного штамма SARS‑CoV‑2, так и против Omicron XBB.1.5. Интраназальная вакцинация, особенно в сочетании с современным адъювантом — агонистом STING (CF501), выделялась сильной индукцией IgA не только в крови, но и в носовых выделениях и омывах лёгких — именно там, где мукозальная защита наиболее важна. Конструкции с Fc также стимулировали более мощные клеточные ответы по сравнению с «голыми» RBD-диимерами, расширяя популяции вспомогательных Т-клеток, цитотоксических Т-клеток и долговременных тканево-резидентных Т-клеток в лёгких. Считается, что эти типы клеток играют ключевую роль в устранении респираторных вирусов и предотвращении их распространения в чувствительные органы, такие как мозг.
Широкая защита против многих вариантов и видов
Ключевым испытанием было, сможет ли бивалентная вакцина, сочетающая RBD прототипного вируса и Omicron XBB.1.5 (названная XBB.1.5 + PT‑Fc), защитить животных от нескольких вирусных вызовов. У мышей, экспрессирующих человеческий ACE2, которым дали две низкие интраназальные дозы, этот кандидат вызвал мощные нейтрализующие антитела и полностью защитил животных от смертельной инфекции как исходным вирусом, так и XBB.1.16: вакцинированные мыши сохраняли вес, выживали и не имели обнаруживаемого вируса в мозге, лёгких или носовых тканях, тогда как контрольные животные заболевали и умирали. Та же вакцина блокировала заболевание и смерть при заражении другими крупными вариантами, включая Бету, Дельту и несколько сублайней Омикрона. У хомяков, которые хорошо подходят для изучения передачи, у вакцинированных животных после прямого заражения наблюдались значительно меньшие вирусные нагрузки, и в экспериментах с совместным содержанием они в основном были защищены от воздушной передачи. Уровни антител и память Т-клеток у мышей и хомяков оставались высокими как минимум 48 недель, и животные оставались полностью защищёнными от смертельных вызовов почти через год после вакцинации.
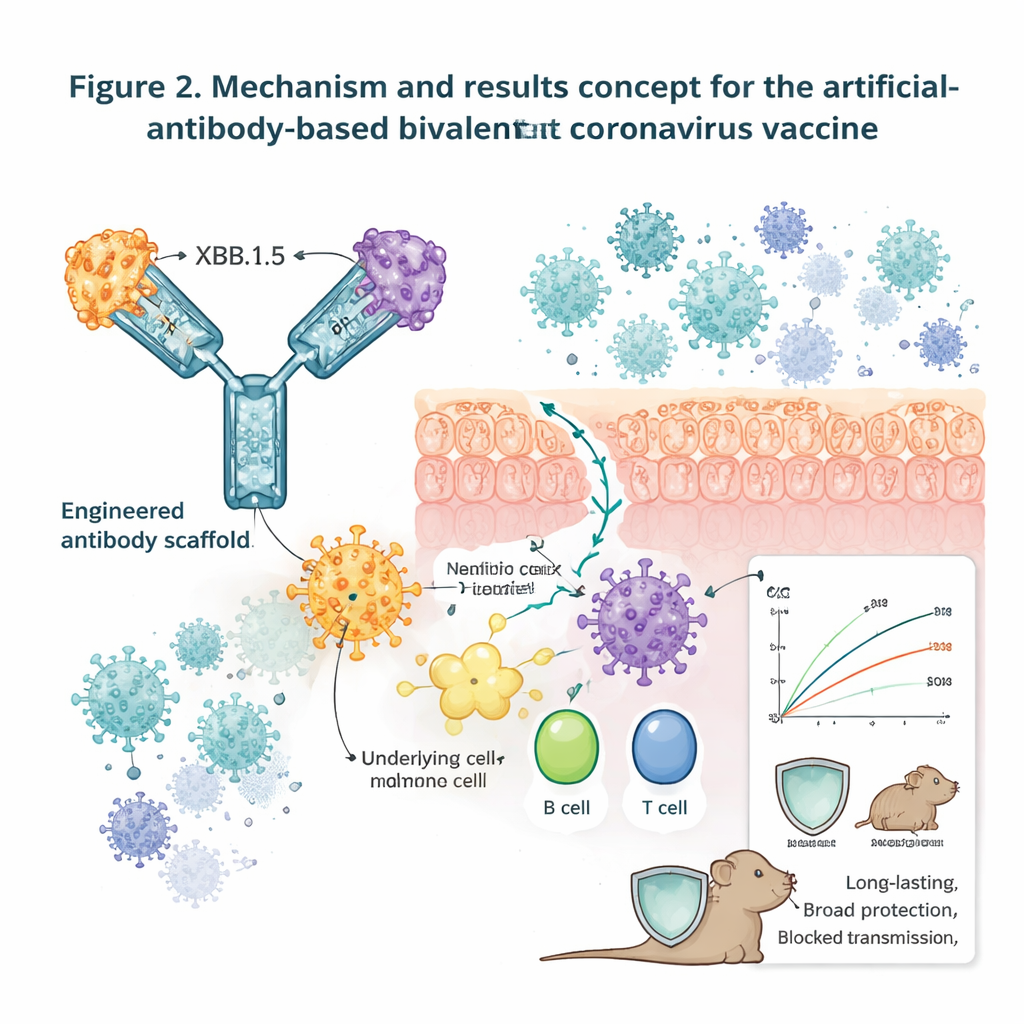
К универсальному назальному спрею против коронавирусов
Наконец, исследователи продвинули платформу в сторону действительно универсального дизайна. Они смешали несколько бивалентных конструкций, покрывающих SARS‑CoV‑2, SARS, MERS и несколько сезонных коронавирусов, а также создали тетравалентные молекулы, несущие четыре разных RBD или фрагмента спайка на одном каркасе. Эти комбинации вызывали антитела, распознававшие широкий набор человеческих коронавирусов и, в экспериментах на мышах, снижали вирусные нагрузки для нескольких представителей, включая эндемический вирус NL63. Хотя необходимы дальнейшие испытания в моделях, ближе к человеку, и в клинических исследованиях, работа демонстрирует, что инженерный каркас антителы может безопасно переносить разнообразные коронавирусные антигены через носовой барьер, стимулировать сильный местный и системный иммунитет и обеспечивать широкую, долговременную защиту. Для неспециалистов главное сообщение таково: будущие «универсальные» бустеры против коронавирусов могут вовсе не быть инъекциями, а мягкими назальными спреями, построенными на тех же антительных каркасах, которые уже доказали свою безопасность во многих лекарственных средствах.
Цитирование: Wu, Y., Lu, J., Fang, L. et al. Universal broad-spectrum mucosal vaccine design for human coronaviruses inspired by artificial antibodies. npj Vaccines 11, 55 (2026). https://doi.org/10.1038/s41541-026-01375-2
Ключевые слова: интраназальная вакцина, широкоспектровый коронавирус, мукозальный иммунитет, каркас искусственного антитела, штаммы SARS-CoV-2