Clear Sky Science · ru
Преодоление резистентности к ТKI, опосредованной сосудистой нишей, при остром миелоидном лейкозе посредством ингибирования miR-126
Почему это важно для пациентов с раком
Острый миелоидный лейкоз (ОМЛ) — одно из наиболее агрессивных заболеваний крови, и даже при современных таргетных препаратах многие пациенты испытывают рецидив. В этом исследовании задаётся на первый взгляд простая, но важная вопрос: проблема заключается не только в самих раковых клетках, но и в «окрестностях», где они обитают в костном мозге? Построив подробную компьютерную модель, основанную на лабораторных данных, авторы исследуют, как крошечные кровеносные сосуды могут защищать стволовые клетки лейкемии от препаратов — и как блокада одного малого РНК-сигнала может разрушить эту защиту.
Скрытое убежище в костном мозге
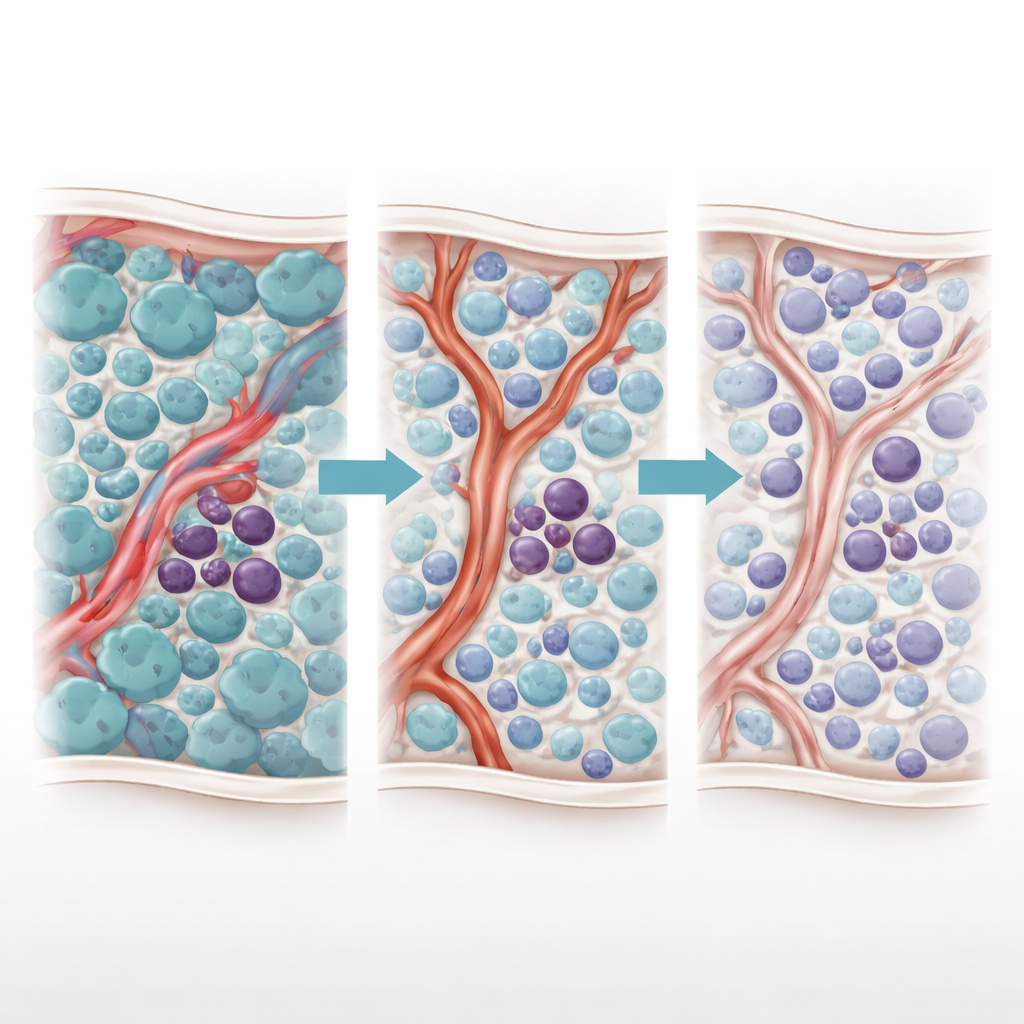
ОМЛ развивается в костном мозге, где злокачественные бластные клетки вытесняют нормальное кроветворение. В этой массе прячется меньшая популяция стволовых клеток лейкемии, способных к самоподдержанию и переживанию терапии, что приводит к рецидиву. Эти стволовые клетки не плавают свободно; они устраиваются в специализированных нишах вокруг мелких артерий и капилляров, известных в целом как сосудистая ниша. Исследование сфокусировано на пациентах, чьи лейкемические клетки несут мутацию FLT3-ITD и лечатся ингибиторами тирозинкиназы (ТKI). Хотя эти препараты могут резко уменьшать опухолевую нагрузку, многие пациенты всё равно рецидивируют, что указывает на то, что некоторые клетки скрываются или защищаются.
Двуликий эффект лечения
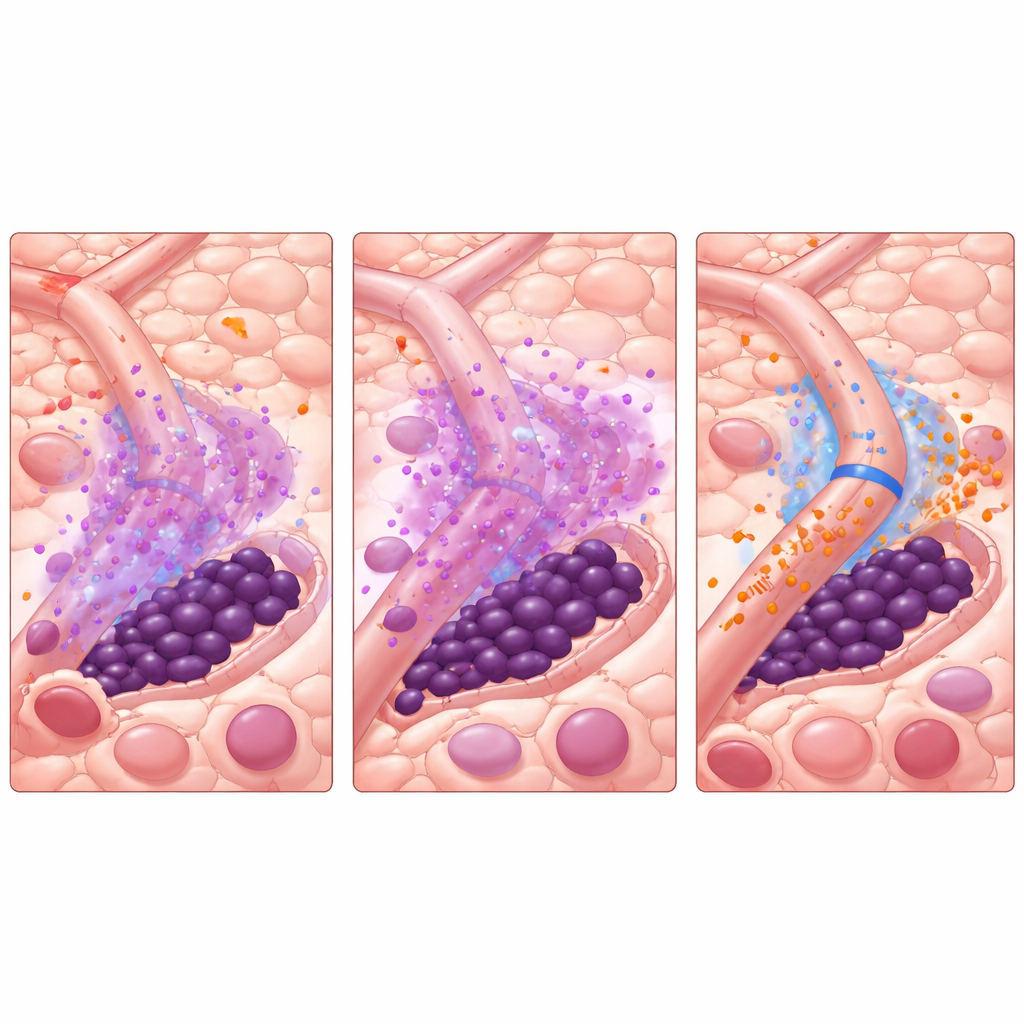
Ранее авторы обнаружили загадочное «явление Януса» — двуликий ответ на терапию ТKI. По мере того как ТKI уничтожают быстро делящиеся бласты, уровень провоспалительного молекулы TNF-α падает. Это снижение неожиданно позволяет соседним клеткам сосудистой стенки увеличить продукцию малой регуляторной РНК, называемой miR-126. Эта miR-126 передаётся от эндотелиальных клеток к стволовым клеткам лейкемии, подталкивая их в тихое, неделящиеся состояние, которое делает их высокорезистентными к лекарствам. Иными словами, само лечение, которое уничтожает большинство раковых клеток, ремоделирует костный мозг так, что самые опасные клетки оказываются защищёнными.
Построение виртуального костного мозга
Чтобы проанализировать эту динамику, команда создала агент-ориентированную вычислительную модель костного мозга при ОМЛ. Каждый ключевой участник — бластные клетки, стволовые клетки лейкемии и эндотелиальные клетки, выстилающие сосуды — представлен отдельным «агентом», который следует биологически обоснованным правилам. Диффундирующие молекулы, такие как TNF-α, miR-126, ТKI AC220 и препарат, блокирующий miR-126 под названием miRisten, распространяются по смоделированной ткани. Модель калибрована по данным визуализации у мышей, которые отображают реальные сосудистые схемы, включая участки, богатые или бедные сосудами, продуцирующими miR-126. В симуляциях стандартная терапия ТKI воспроизводила эффект Януса: число бластов падало, TNF-α снижался, miR-126 из сосудов нарастал, стволовые клетки уходили в защитные ниши, и заболевание впоследствии рецидивировало.
Выключение щита с точным таймингом
Имея в распоряжении эту виртуальную систему, исследователи протестировали способы разорвать порочный круг. Простое добавление miRisten одновременно с ТKI помогало, но редко приводило к излечению в модели. Более стратегический подход оказался эффективнее: короткий «предварительный курс» miRisten в одиночку для снижения сосудистой miR-126, а затем либо ТKI в одиночку, либо продолжающаяся комбинированная терапия. В различных смоделированных сосудистых конфигурациях даже несколько дней предварительной терапии miRisten до начала AC220 резко уменьшали или устраняли рецидив при одновременном ограничении общей лекарственной нагрузки. Модель также показала, что близость стволовых клеток лейкемии к сосудам сильно влияет на их судьбу — клетки, прижатые вплотную к сосудам, получают наибольшую защиту, если miR-126 не блокируется.
Что это может значить для будущей терапии
Проще говоря, исследование предполагает, что некоторые стволовые клетки лейкемии выживают не потому, что ТKI слабы, а потому, что мелкие кровеносные сосуды костного мозга во время лечения временно переключаются в режим «защитника». Кратковременное выключение одного сигнала, miR-126, перед введением ТKI может лишить эту защиту, вытащить стволовые клетки из укрытия и сделать их уязвимыми для существующих препаратов. Поскольку эта работа основана на компьютерных моделях, подкреплённых лабораторными данными, а не на клинических испытаниях, она предлагает конкретную стратегию: вводить препарат, нацеленный на микроокружение, непосредственно перед и во время стандартной терапии. Если подтвердится, такой подход может не только улучшить исходы для пациентов с FLT3-мутацией ОМЛ, но и вдохновить аналогичные тактики при других гематоонкологических и солидных опухолях, где «окрестности» опухоли помогают ей уклоняться от лечения.
Цитирование: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
Ключевые слова: острый миелоидный лейкоз, стволовые клетки лейкемии, микроокружение костного мозга, резистентность к ингибиторам тирозинкиназы, ингибирование miR-126