Clear Sky Science · ru
Пространственный FBA выявляет гетерогенные ворбурговские ниши в опухолях почки и потребление лактата в колоректальном раке
Почему имеет значение пространственная организация метаболизма опухоли
Раковые клетки ведут себя не одинаково, даже внутри одной опухоли. Одни находятся рядом с кровеносными сосудами, другие — глубже, в плохо снабжаемых зонах, и эти местоположения определяют, как они добывают и используют энергию. В этом исследовании представлен новый способ чтения скрытой «метаболической карты» по современным пространственным данным экспрессии генов. Это позволяет авторам выявлять неожиданные схемы обращения с ключевой молекулой — лактатом, бросая вызов классическому представлению о том, что рак лишь выводит лактат как отход.
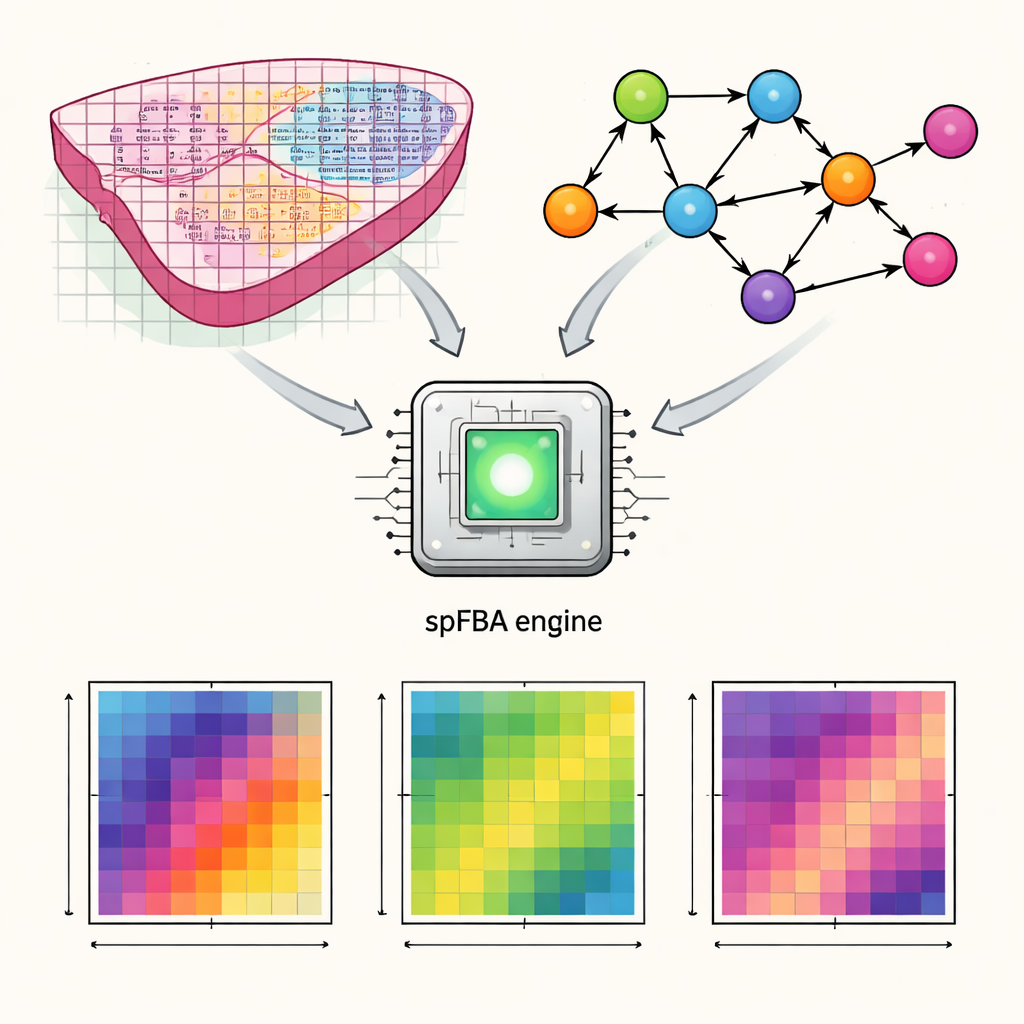
Преобразование карт генов в метаболическую активность
Авторы разработали вычислительную схему, названную пространственным анализом баланса потоков (spFBA). Технологии пространственной транскриптомики измеряют, какие гены активны в тысячах небольших точек на тонком срезе ткани. spFBA объединяет эти пространственные карты активности генов с детальными моделями человеческого метаболизма, которые описывают, как такие питательные вещества, как глюкоза, кислород и аминокислоты, трансформируются внутри клеток. Вместо предположения, что все участки ткани имеют одну и ту же метаболическую цель, spFBA рассматривает каждую точку независимо, исследуя, какие паттерны реакций возможны там в рамках законов химии и баланса масс. На выходе получается набор «оценок обогащения потоков», которые указывают, насколько сильно в каждом месте могут протекать разные метаболические реакции и в каком направлении.
Тестирование метода на опухолях почки
Чтобы проверить, дает ли spFBA биологически осмысленные результаты, группа сначала обратилась к прозрачноклеточному раку почки — виду рака почки, известному сильной зависимостью от расщепления сахара (гликолиза) и выброса лактата, явления, называемого эффектом Варбруга. Используя опубликованные пространственные данные из десяти образцов почечной опухоли, они проверили, соответствуют ли предсказанные метаболические паттерны известной структуре ткани. Оказалось, что точки, сгруппированные по рассчитанным потокам, хорошо совпадали с гистологической организацией, видимой под микроскопом, и с кластерами, выделенными по одной только экспрессии генов. Важно, что spFBA восстановил ожидаемый метаболический контраст между опухолевой и нормальной почечной тканью: в опухолевых зонах было более интенсивное потребление глюкозы, усиленное производство биомассы (как прокси роста клеток) и выраженная секреция лактата. При этом использование кислорода оставалось значительным, что показывает: разные части одной и той же опухоли могут сочетать брожение и дыхание в зависимости от местного кровоснабжения.
Колоректальные раки показывают другую историю лактата
Исследователи затем применили тот же анализ к новым высокоразрешающим пространственным данным от пациента с первичным колоректальным раком и сопоставимыми метастазами в печени, а также к независимому публичному набору колоректальных данных, полученных другой технологией. Здесь результаты оказались поразительно иными. Вместо экспорта лактата как отхода большинство областей колоректального рака — как в исходной опухоли кишечника, так и в метастазах в печени — были предсказаны как поглощающие лактат из окружения. Клетки стромы в близлежащей поддерживающей ткани склонялись к небольшому выделению лактата, тогда как опухолевые клетки выступали в роли его активных потребителей. Анализ на уровне реакций показывает, что эти метастатические клетки не просто окисляют лактат в обычном энергетическом цикле в митохондриях. Скорее, они превращают лактат в строительные блоки, которые вовлекаются в пути синтеза липидов и других компонентов, необходимых для роста клеток — своего рода «псевдо‑обратный эффект Варбруга», при котором лактат становится сырьем для биосинтеза.
Метаболические ниши и фронт опухоль‑строма
Поскольку spFBA сохраняет пространственную привязку, он может точно указывать, где происходят те или иные метаболические обмены. В опухолях почки метод выявил сосуществующие метаболические «районы»: более оксигенированные, богатые кровью интерфейсы, где раковые клетки и дышат, и ферментируют, и более глубокие, слабо васкуляризованные ядра, которые сильнее полагаются на брожение. В метастазах колоректального рака в печени spFBA выделил резкие контрасты на границе между опухолью и стромой, где обращение глутамата и лактата меняло направление, что указывает на интенсивный обмен на инвазивном фронте. Во всех наборах данных предсказанные потоки, связанные с ростом, коррелировали с независимыми мерами пролиферации на основе генов, подтверждая биологическую правдоподобность модели. Что важно, тот же алгоритм предсказывал секрецию лактата в раке почки и поглощение лактата в колоректальном раке, что указывает на то, что наблюдаемые различия исходят из данных, а не из предвзятости модели.
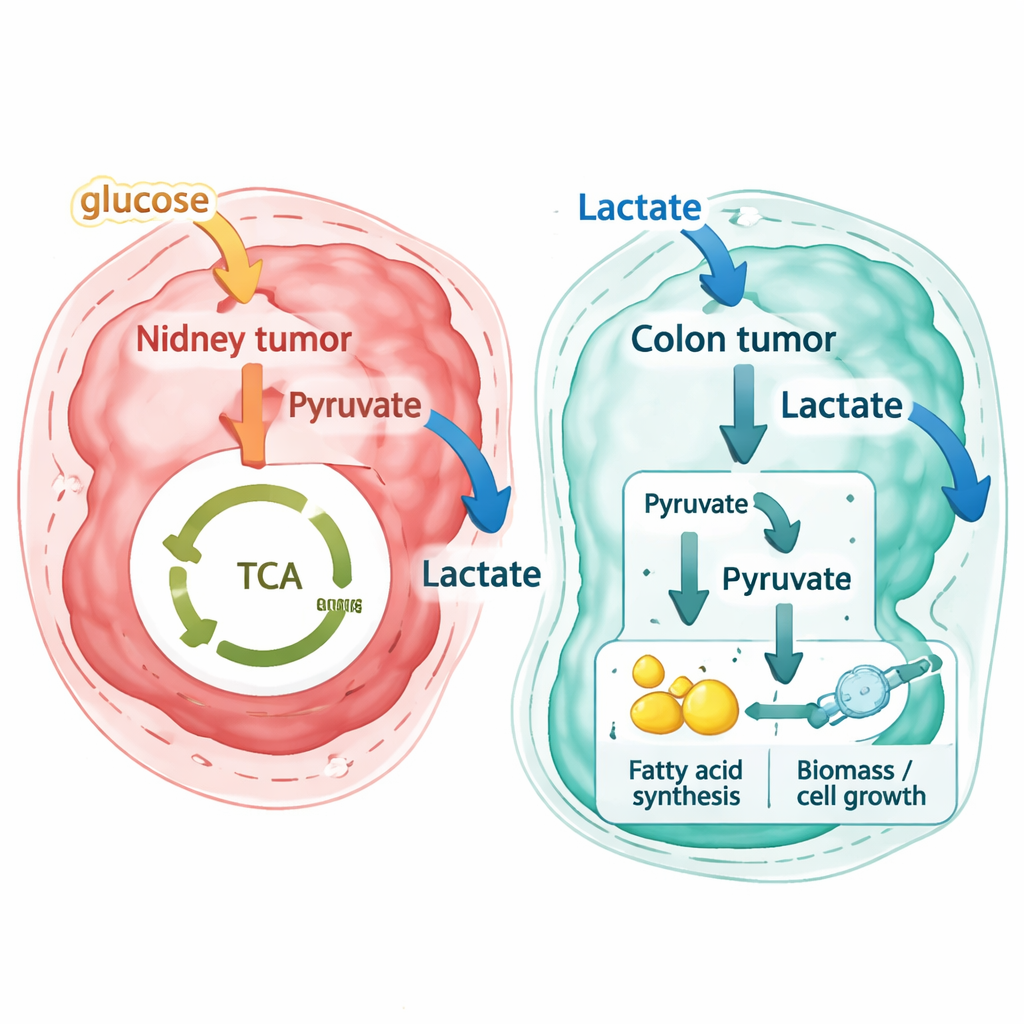
Что это значит для понимания и лечения рака
Для неспециалистов ключевая мысль такова: метаболизм рака не только аномален — он ещё и сильно локализован. Одна и та же опухоль может содержать несколько метаболических ниш, а опухоли, похожие по внешнему виду в разных органах, могут использовать одни и те же молекулы противоположным образом. Эта работа демонстрирует, что, наложив пространственную экспрессию генов на подробные метаболические модели, исследователи могут выяснить, где опухоли, вероятно, особенно нуждаются в конкретных питательных веществах, таких как лактат. В случае колоректального рака открытие того, что опухолевые клетки широко потребляют лактат и направляют его в процессы, связанные с ростом, ставит новые вопросы о том, как диета, кишечная микробиота и собственный метаболизм печени влияют на прогрессирование болезни, и можно ли усилив блокирование использования лактата сделать эти опухоли более уязвимыми для терапии.
Цитирование: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Ключевые слова: метаболизм рака, пространственная транскриптомика, лактат, эффект Варбруга, колоректальный рак