Clear Sky Science · ru
Анализ динамической сети выявляет дальнодействующие связи между остатками на интерфейсе pMHC, лежащие в основе повышенной иммуногенности
Как крошечные фрагменты вируса направляют нашу иммунную защиту
Наши киллерные Т‑клетки патрулируют организм в поисках признаков инфекции или рака. Они делают это, сканируя крошечные фрагменты белков — пептиды, — выставленные на поверхности клеток молекулами класса I MHC. В этом исследовании поставлен тонкий, но важный вопрос: как одна небольшая замена в пептиде может заставить Т‑клетки реагировать гораздо сильнее — или вообще не реагировать? Оказалось, что дело не только в статической структуре, но и в том, как весь молекулярный комплекс движется и деформируется со временем.
Замок, ключ и движущиеся части
Чтобы понять работу, полезно представить комплекс пептид–MHC (pMHC) как замок, а рецептор Т‑клетки (TCR) как ключ. Пептид располагается в желобке молекулы MHC, и вместе они образуют поверхность, которую исследует TCR. Предыдущие исследования показали, что и точная последовательность пептида, и конкретный вариант MHC существенно влияют на ответ Т‑клетки. Ученые также создавали «модифицированные пептидные лиганды» с небольшими изменениями для настройки иммунного ответа, в том числе в раковой иммунотерапии. Но если о статических формах этих комплексов известно много, то о том, как движения в одной точке пептида влияют на отдалённые участки интерфейса, где фактически связывается TCR, известно значительно меньше.
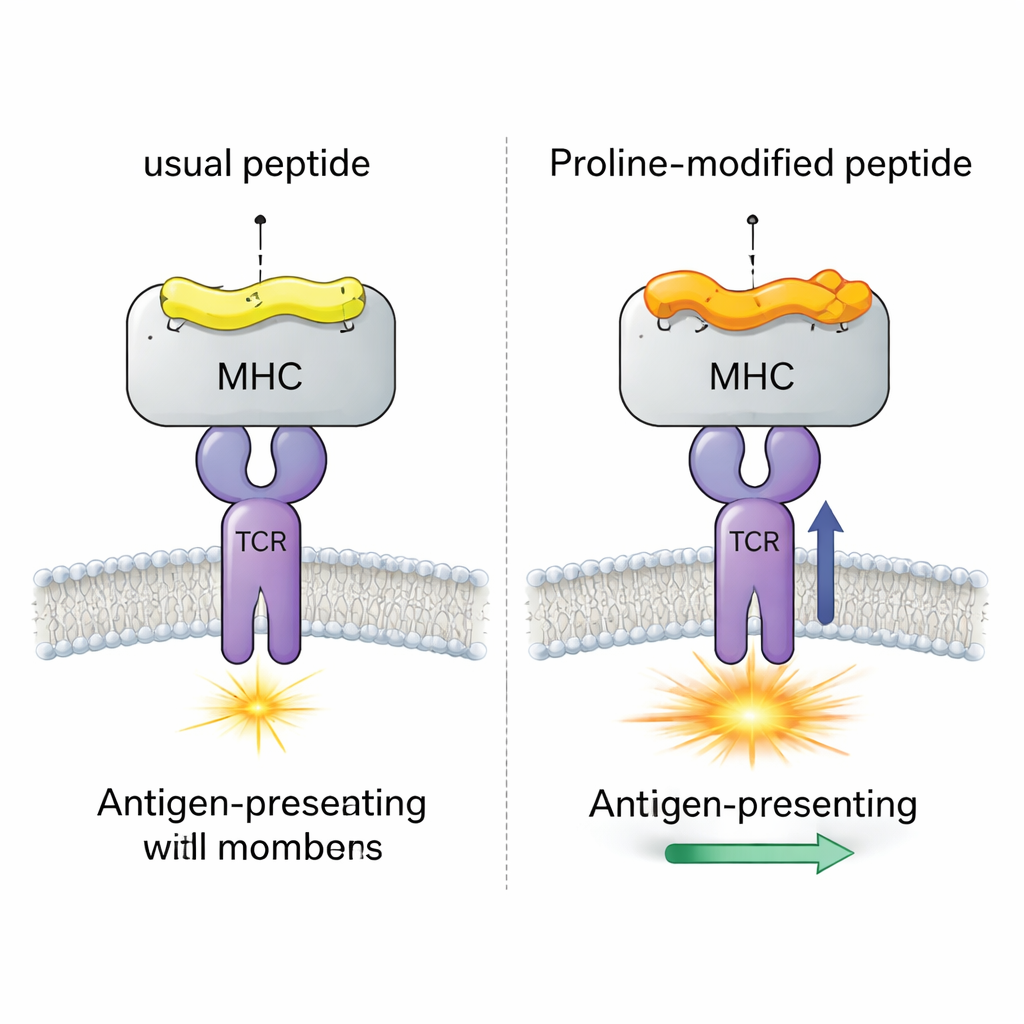
Вирусный пример с четырьмя практически идентичными пептидами
Авторы сосредоточились на хорошо изученной системе мышиного вируса (LCMV), включающей пептид gp33, который обычно вызывает сильные ответы CD8+ T‑клеток. Они сравнили четыре близкородственных варианта этого пептида, все связанные с той же молекулой MHC (H-2Db). Один вариант — оригинальный вирусный пептид; другой несёт мутацию выхода от иммунитета, которую Т‑клетки почти не распознают; и два — кандидатных вакцинных варианта с заменой на пролин в одной позиции близ начала пептида. Ранние эксперименты показали, что эта замена на пролин увеличивает прочность связывания пептид–MHC и усиливает отклик модельного TCR (называемого P14), но детальный механизм оставался неясным.
Наблюдая за дрожанием молекул: симуляции и кристаллография
Чтобы выяснить, что происходит, авторы объединили высокоразрешающую кристаллическую структуру с длительными покомпонентными компьютерными симуляциями каждого pMHC‑комплекса в движении. Они оценивали, насколько каждый аминокислотный остаток колеблется во времени и как эти колебания меняются при переводе третьей позиции пептида в пролин. Коррелируя закономерности движений в множестве парных симуляций, они построили «динамическую карту» остатков, которые двигаются согласованно, даже если находятся далеко друг от друга в пространстве. Затем эту карту превратили в сеть, где каждый остаток — это узел, а ребра отражают статистически связанные движения, и проанализировали сеть с помощью методов теории графов, схожих с теми, что применяются в анализе социальных сетей.
Дальнодействующая коммуникация внутри иммунного «замка»
Ключевое открытие состоит в том, что замена третьего остатка пептида на пролин делает не только локальную часть более жёсткой. Она меняет способ передачи движений вдоль одной из α‑спиралей MHC, примыкающей к желобку связывания пептида. Это, в свою очередь, влияет на поведение другого остатка пептида — позиции шесть, которая расположена прямо под пятном контакта TCR и критична для распознавания. В «хороших» вариантах с пролином этот остаток пробует более широкий набор конформаций, включая те, что оптимальны для связывания с TCR. В варианте с уходом от иммунитета без пролина этот остаток более закреплён и редко принимает ориентацию, благоприятную для TCR. Анализ сети показывает, что это влияние передаётся через специфические аминокислоты в желобке MHC, образуя цепочку динамически связанных остатков, связывающих место замены пролина с областью контакта TCR.
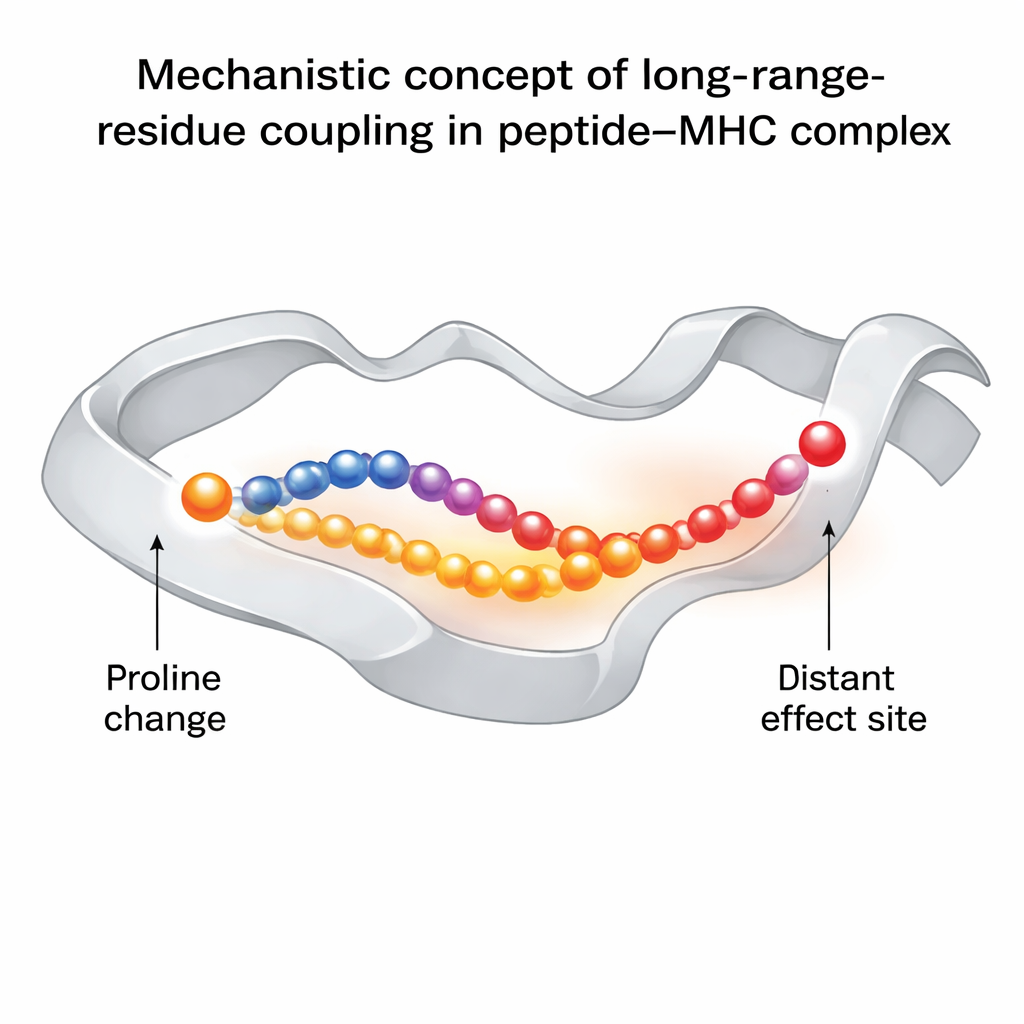
Почему это важно для вакцин и иммунотерапии
Эти результаты демонстрируют, что иммуногенность — степень, в которой пептид вызывает ответ Т‑клеток — зависит не только от того, подходят ли формы в конкретный момент, но и от того, как комплекс «дышит» и сгибается во времени. Тонкая замена в одной позиции может распространиться по молекулярной сети, делая ключевые контактные остатки более склонными к появлению в конформациях, совместимых с TCR. Вычислительный рабочий процесс авторов предоставляет способ систематически выявлять такие дальнодействующие связи, что может помочь в проектировании модифицированных пептидов для вакцин и раковой терапии. Проще говоря, они показывают, что, тщательно выбирая место для изменения пептида, можно подтолкнуть весь «замок» в более «готовое к открыванию» динамическое состояние для ключа иммунной системы.
Цитирование: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Ключевые слова: распознавание Т-клетками, пептид MHC, динамика белков, модифицированные пептидные лиганды, иммуногенность