Clear Sky Science · ru
Компьютерное моделирование дифференцировки передней кишки эндодермы в эпителиальные предшественники легких
Преобразование стволовых клеток в клетки, строящие легкие
Ученые изучают, как перенаправить собственные стволовые клетки пациента, чтобы получить заменительную ткань легкого, которая однажды сможет восстанавливать повреждения при таких заболеваниях, как ХОБЛ, фиброз или тяжелые инфекции. В этой статье рассматривается, как исследователи использовали компьютерное моделирование для картирования и тонкой настройки важного шага в этом процессе: превращения промежуточного типа клеток, называемого передней кишкой эндодермы, в ранние эпителиальные предшественники легких — стартовые клетки, которые в дальнейшем могут сформировать дыхательные пути и альвеолы легкого.
Почему важны стартовые клетки легкого
Человеческие индуцированные плюрипотентные стволовые клетки (iPSC) можно перепрограммировать из соматических тканей и направить к формированию разных органов. Чтобы создать ткань легкого, эти клетки проходят через несколько этапов развития. Один из них — передняя кишка эндодермы, слой, который в эмбриогенезе обычно дает начало частям дыхательной и пищеварительной систем. Дальше, при правильных химических сигналах, клетки могут становиться эпителиальными предшественниками легкого, несущими ранние маркеры легочной линии и способными впоследствии созревать в специализированные клетки дыхательных путей или альвеол. Поскольку для будущих клеточных терапий потребуется миллиарды таких клеток, исследователям нужны способы надежно повышать выход и адаптировать протоколы под разные клеточные линии пациентов без бесконечных проб и ошибок в лаборатории.
Создание виртуальной модели дифференцировки клеток
Команда расширила ранее предложенную математическую основу, чтобы построить, по их сведениям, первую на популяционном уровне модель этого конкретного перехода от эндодермы передней кишки к предшественникам легких. Они рассмотрели два способа представления клеток: простую версию, отслеживающую только общее число живых клеток, и более детальную, которая отдельно следует за клетками передней кишки и предшественниками легких. В обоих вариантах модель также отслеживает глюкозу и лактат в культуре, представляя собой питательные вещества и отходы. С использованием инструментов системной биологии исследователи составили множество кандидатных уравнений для описания роста, гибели и дифференцировки клеток, затем провели тесты идентифицируемости, чтобы отсеять модели, параметры которых нельзя было бы надежно оценить даже при идеальных данных.
Проектирование более разумных экспериментов с помощью модели
Вместо того чтобы подгонять модель к имеющимся случайным данным, исследователи позволили модели подсказывать, как следует проводить новые эксперименты. Они использовали смоделированные данные, чтобы выяснить, как часто нужно измерять число клеток и уровни питательных веществ, чтобы точно оценить параметры модели, балансируя статистическую точность и затраты труда при частом отборе проб. Это привело к практическому плану: ежедневные измерения глюкозы и лактата и подсчет клеток каждые один‑два дня при четырех условиях, различающихся степенью разведения культур на день 10 и тем, обновляли ли среду ежедневно. Затем они провели эти эксперименты, измеряя как общую популяцию клеток, так и, с помощью проточной цитометрии, доли клеток, оставшихся клетками передней кишки или ставших предшественниками легких.
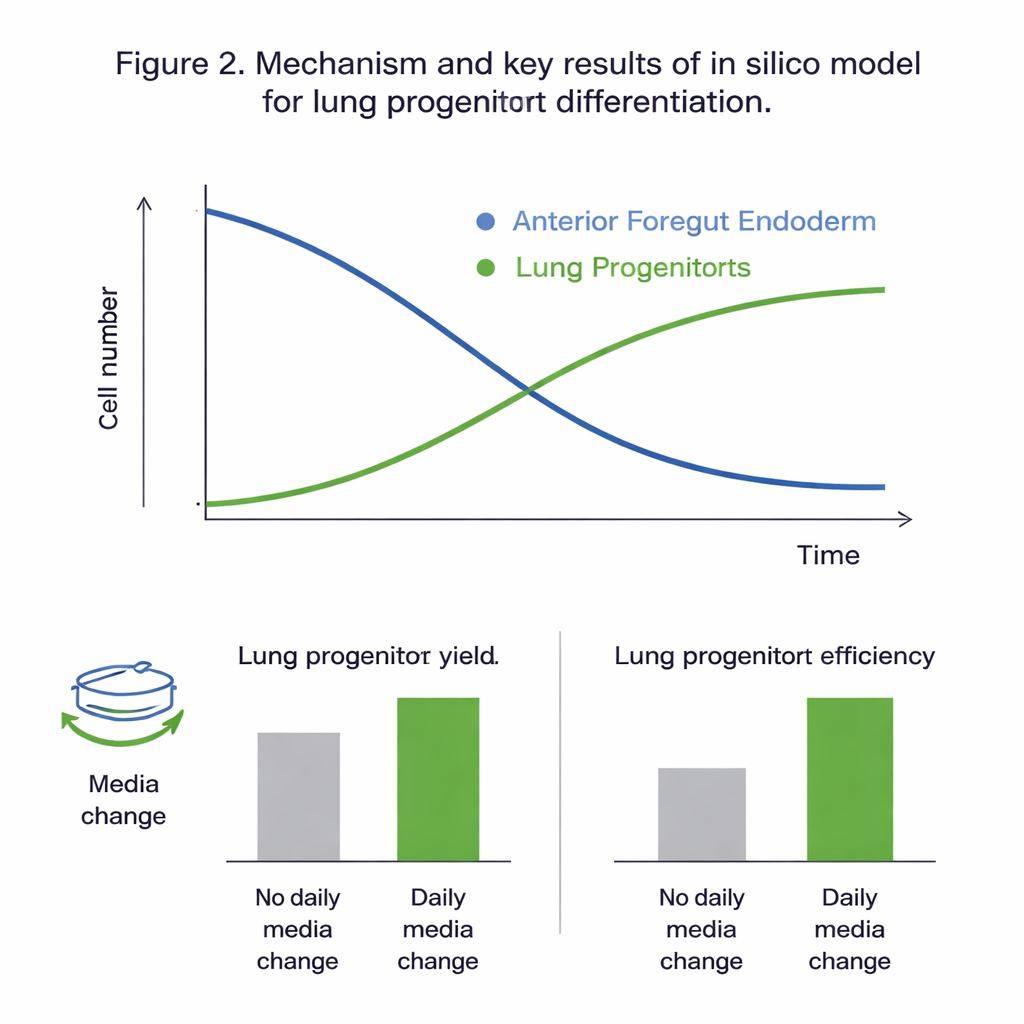
Что выявили виртуальные эксперименты
Подгонка всех кандидатных моделей к экспериментальным данным показала, что модель с двумя популяциями, отдельно отслеживающая клетки передней кишки и предшественников легких, может быть надежно калибрована и лучше всего описывает наблюдаемое поведение. Статистические проверки указали, что в изученный временной интервал (дни 11–15 протокола) динамика в основном определялась пролиферацией и дифференцировкой клеток передней кишки, тогда как пролиферация самих предшественников легких вносила небольшой вклад. Глобальный анализ чувствительности подтвердил эту картину, выделив скорости роста, гибели и дифференцировки клеток передней кишки — а также влияние глюкозы — как основные рычаги, контролирующие исход. Откалиброванная модель воспроизводила невидимые данные с ошибками, сопоставимыми с естественной вариабельностью экспериментов, что указывает на достаточную точность для исследования сценариев «что‑если» in silico.
Оптимизация смен среды и разведения клеток
Имея надежную виртуальную систему, команда протестировала, как два практичных параметра протокола влияют на результаты: насколько сильно развести культуру (коэффициент разделения) на день 10 и заменять ли ростовую среду ежедневно. Симуляции предсказали, что ежедневные смены среды почти удваивают число предшественников легких и выход на одну стартовую клетку, главным образом предотвращая истощение питательных веществ и накопление отходов и нестабильных сигнальных молекул. Эксперименты очень близко соответствовали этим прогнозам. Модель также показала, что использование более высоких коэффициентов разделения — более редкое размещение клеток на день 10 — повышает «выход на входную клетку» примерно на четверть, хотя при этом снижается абсолютное число клеток. В обоих случаях эти изменения мало влияли на конечную долю предшественников легких в культуре, в основном сдвигая количество клеток, которые можно произвести эффективно.
Что это значит для будущих терапий легких
Для неспециалиста главный вывод состоит в том, что авторы построили своего рода авиасимулятор для критического шага в выращивании клеток легкого из стволовых клеток. Сочетая продуманно спланированные эксперименты с строгим математическим моделированием, они показывают, как простые решения протокола — например, как часто менять среду и с какой плотностью сеять клетки — могут существенно влиять на количество получаемых клеток, строящих легкие, не изменяя их качества. Такой подход in silico может помочь оптимизировать будущие протоколы, сократить экспериментальные догадки и в конечном счете поддержать более надежное и масштабируемое производство предшественников легких для исследований, моделирования заболеваний и, в перспективе, регенеративных терапий.
Цитирование: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Ключевые слова: предшественники клеток легких, индуцированные плюрипотентные стволовые клетки, компьютерное моделирование, дифференцировка клеток, регенеративная медицина