Clear Sky Science · ru
Вывод параметров миграции клеток из моделирования в сложных пространственных средах
Как иммунные клетки находят путь через плотные ткани
Нашим иммунным клеткам часто приходится протискиваться через плотные, похожие на лабиринт ткани, чтобы добраться до очагов инфекции или лимфатических узлов. В этом исследовании поставлен на вид deceptively простой вопрос с большими последствиями: как эти клетки ориентируются в столь загромождённой среде и как можно надёжно восстановить их поведение по шумным данным микроскопа? Сочетая точно спроектированные лабораторные «лабиринты» с продвинутыми компьютерными симуляциями и современными инструментами машинного обучения, авторы показывают новый способ расшифровки правил, управляющих движением клеток в сложной обстановке.
Построение мини‑лабиринта для иммунных клеток
Чтобы изучить, как среда формирует движение, исследователи сосредоточились на дендритных клетках — иммунных стражах, которые должны передвигаться от периферических тканей к лимфатическим узлам, ориентируясь по химическим аттрактантам, называемым хемокинами. Они создали микрофабрикованный чип: плоский «лес столбиков» из регулярно расположенных опор из силиконовой резины (PDMS) с узкими зазорами около 10 микрометров, имитирующими тесные пространства в реальных тканях. С одной стороны чипа разместили десятки тысяч дендритных клеток; с противоположной стороны — источник хемокина CCL19, создающий стабильный градиент через столбики. С помощью тайм‑лапс‑микроскопии они отслеживали ядра отдельных клеток каждые 30 секунд, пока те пытались двигаться в сторону источника хемокина. 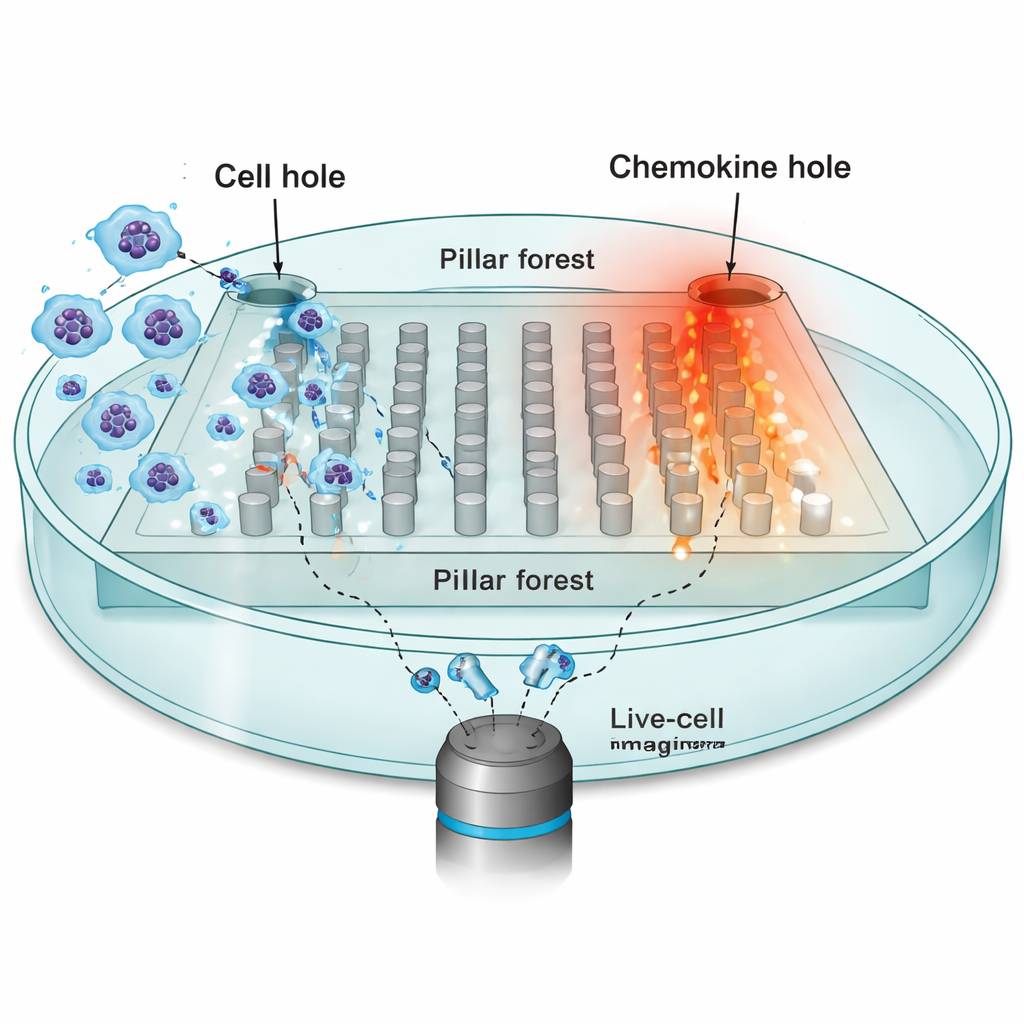
Преобразование биологии в виртуальный эксперимент
Чтобы разобраться в этом разнообразии, команда построила детальную вычислительную модель миграции клеток, используя подход, известный как модель Клеточного Поттса (Cellular Potts model). Вместо того чтобы рассматривать клетку как простую точку, этот подход представляет каждую клетку в виде протяжённого фрагмента на сетке, позволяя ей менять форму, сжиматься между столбиками и реагировать на химические сигналы. Модель включает четыре ключевых компонента: насколько сильно клетку тянет градиент хемокина (mdir), насколько она склонна сохранять текущее направление движения (mrand), как часто она переориентируется (здесь это описывается скоростью λ) и её эффективный размер (a). Настраивая эти параметры и запуская симуляции, модель порождает синтетические траектории, которые можно напрямую сравнивать с записанными путями клеток в «лесу» столбиков.
Почему выбранные вручную меры оказываются недостаточны
Традиционно исследователи сводят такие данные о движении к нескольким знакомым статистикам — насколько далеко клетка проходит (смещение), с какой скоростью она движется (скорость) и как изменяется её направление со временем (углы поворота). Авторы сначала использовали эти вручную разработанные меры в технике, называемой приближённой байесовской компьютацией (ABC), которая ищет наборы параметров, делающих симулированные траектории похожими на экспериментальные. Они обнаружили, что хотя эти сводки фиксируют общие тенденции, они упускают большую часть тонкой структуры в данных. В результате некоторые параметры модели, особенно отвечающие за случайную сохранность направления и частоту переориентаций, оставались слабо ограниченными или даже искаженными. Кроме того, ABC требовала сотен тысяч симуляций и многих часов вычислений, чтобы достигнуть приемлемого соответствия.
Дать нейросетям возможность узнать, что важно
Чтобы преодолеть эти ограничения, исследование обратилось к более новым методам, называемым оценкой апостериорного распределения нейросетью (neural posterior estimation, NPE). В этом подходе нейронная сеть обучается непосредственно на множестве пар «симулированные данные — соответствующие параметры». Одна часть сети автоматически учится извлекать компактный набор «характеристик‑сводок» из целых наборов траекторий; другая — учится отображать эти характеристики обратно в вероятные значения параметров. Важно, что эти извлекаемые признаки оптимизируются специально для точной инференции параметров, а не для удобства человеческого толкования. Авторы затем повторно использовали эти изученные сводки внутри фреймворка ABC, создав гибридный конвейер, который сочетает надёжность ABC с гибкостью нейросетей. 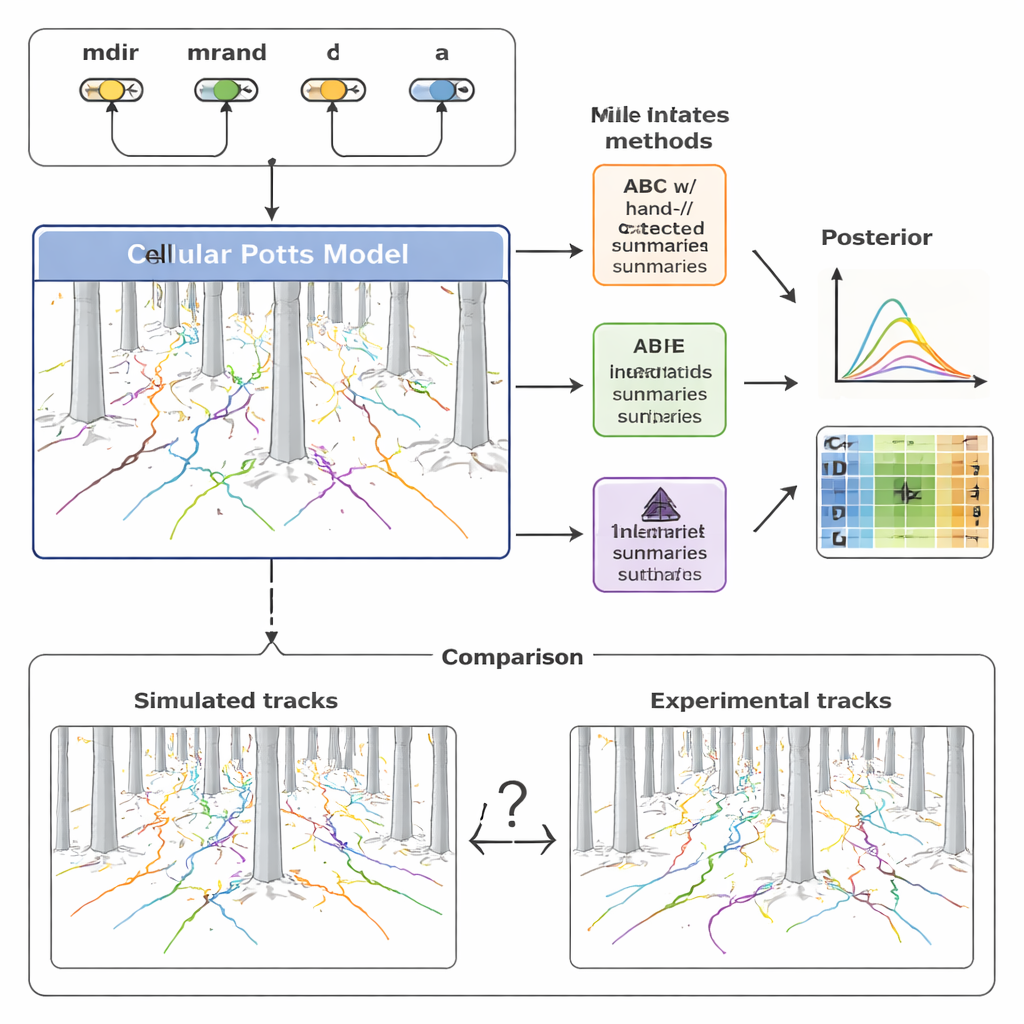
Что новый подход раскрывает о навигации клеток
Вооружившись откалиброванной моделью, исследователи изучили, как хемокиновые сигналы и физические препятствия совместно формируют миграцию. Выведенный эффективный размер клетки предположил, что дендритные клетки фактически уменьшаются и деформируются, чтобы пройти через зазоры в 10 микрометров, что соответствует их известной гибкости. Симуляции указали, что персистентное случайное движение является главным фактором того, насколько широко клетки распространяются, даже без хемокинового руководства, и что лес столбиков может захватывать клетки, когда сильные направленные сигналы и персистентность действуют совместно. Удивительно, но модель предсказывает, что кратковременный активный сигнал хемокина в начале может в некоторых случаях помочь большему числу клеток достичь цели, чем постоянный сигнал, потому что длительное притяжение может удерживать клетки, заставляя их кружить внутри препятствий, а не выходить из них.
Почему это важно для биологии и моделирования
Для неспециалистов ключевое сообщение двояко. Во‑первых, миграция иммунных клеток в тканях — это не просто следование химическому следу; она возникает из тонкого взаимодействия между направляющими сигналами, собственными тенденциями движения клеток и физической структурой их окружения. Во‑вторых, извлечение этих правил из изображений требует, чтобы компьютер сам научился, какие шаблоны в данных наиболее информативны, вместо того чтобы полагаться только на простые человеческие измерения. Интегрируя микроинженерные эксперименты, симуляции, учитывающие форму, и инференцию на базе нейронных сетей, эта работа предлагает мощный шаблон для изучения того, как клетки разных типов перемещаются в сложных средах, с потенциальными приложениями от понимания иммунного надзора до разработки более эффективных противоопухолевых терапий.
Цитирование: Arruda, J., Alamoudi, E., Mueller, R. et al. Simulation-based inference of cell migration dynamics in complex spatial environments. npj Syst Biol Appl 12, 20 (2026). https://doi.org/10.1038/s41540-026-00648-9
Ключевые слова: миграция клеток, дендритные клетки, градиенты хемокинов, инференция на основе моделирования, микрофлюидные «лесa» столбиков