Clear Sky Science · ru
Контроль роста оптической глиомы при астме через взаимодействие Т-клеток и микроглии: математическая модель
Когда проблемы с дыханием связаны с опухолями мозга
Астма и опухоли мозга кажутся совершенно разными явлениями: одна влияет на дыхание, другая — на зрение, мышление и движение. Тем не менее врачи заметили любопытный феномен — у детей с астмой вероятность развития некоторых опухолей зрительного нерва выглядит ниже. В этой статье рассматривается, как хроническое заболевание легких может неожиданно защищать мозг: авторы используют математическую модель, чтобы проследить скрытые «химические разговоры» между иммунными и опухолевыми клетками.
Медленно растущая опухоль с большими ставками
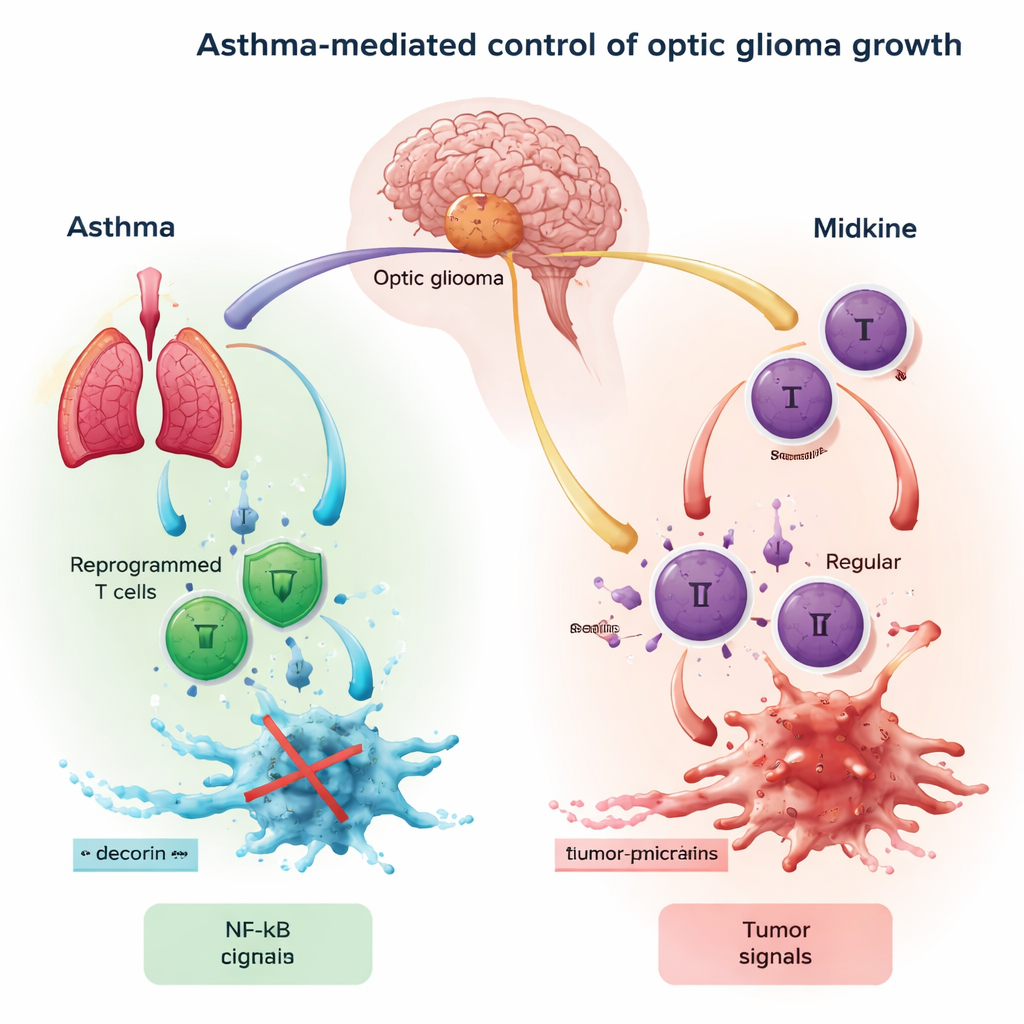
Оптические глиомы обычно растут медленно и образуются вдоль зрительного нерва, чаще всего у детей с наследственным заболеванием нейрофиброматозом 1 типа (NF1). Хотя эти опухоли считаются «низкой степени злокачественности», они все равно могут приводить к потере зрения и гормональным нарушениям. При NF1 дефект в гене вызывает гиперактивность сигнального белка RAS. Эта гиперактивность запускает производство другой молекулы, мидкина, который ведет себя как громкоговоритель в области зрительного нерва, привлекая иммунные клетки и перестраивая локальную среду так, что она чаще помогает опухоли, чем борется с ней.
Разговор между нервными и иммунными клетками, питающий опухоль
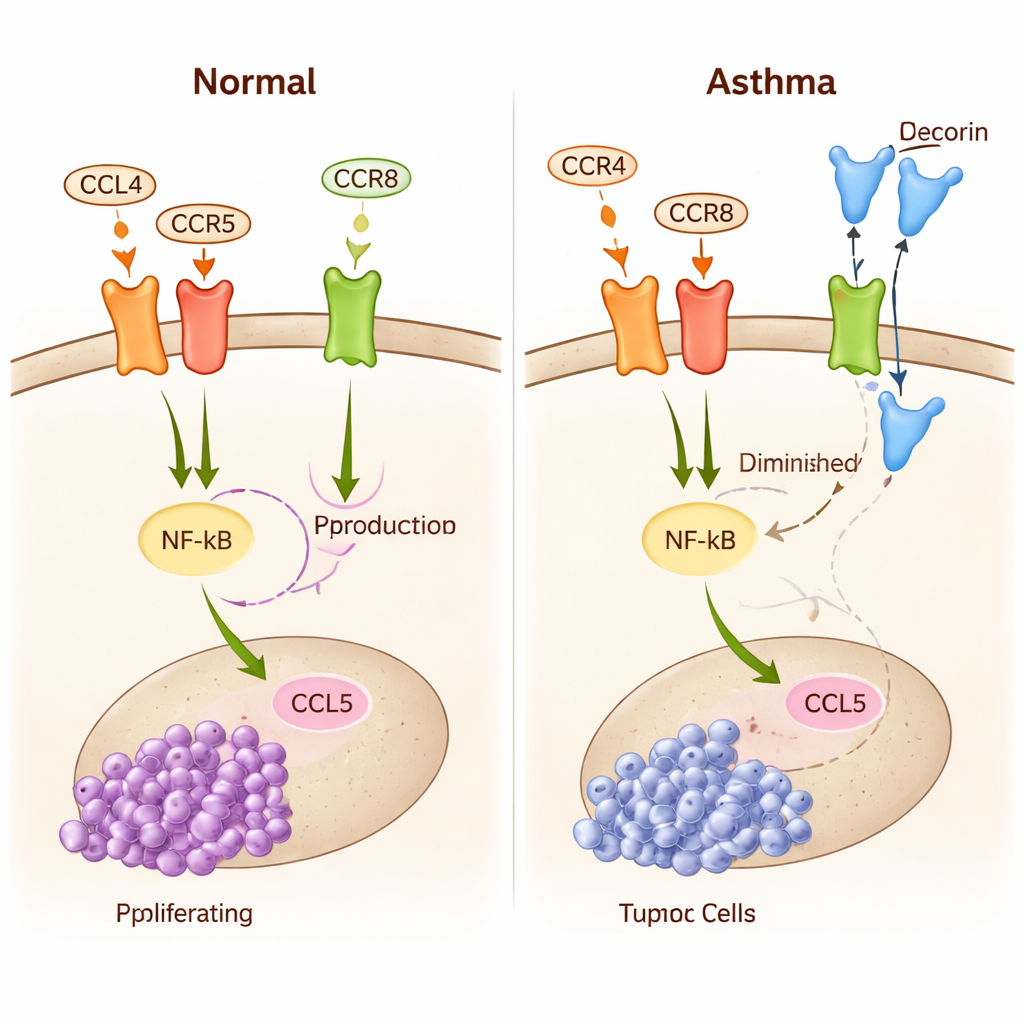
Авторы сосредотачиваются на цепочке событий, связывающих зрительный нерв, иммунные клетки и рост опухоли. Мидкин из зрительного нерва сначала активирует Т‑клетки — тип лейкоцитов — заставляя их выделять сигнал CCL4. Этот сигнал связывается с рецепторами (CCR5 и CCR8) на микроглии — тканевых иммунных клетках мозга. Когда достаточно много CCL4 прикрепляется к этим рецепторам, внутри микроглии включается главный транскрипционный фактор NF-κB. После активации NF-κB запускает выработку другого сигнала, CCL5, который стимулирует клетки оптической глиомы к росту, миграции и уклонению от иммунной атаки. Фактически ось мидкин–CCL4–NF-κB–CCL5 образует круговой «сигнал продолжать» для расширения опухоли.
Как астма перепрограммирует Т‑клетки в факторы сдерживания опухоли
Астма известна прежде всего как заболевание с хроническим воспалением дыхательных путей. Но у людей с астмой часть Т‑клеток «перепрограммируется» в другой функциональный тип: они теряют большую часть прямой цитотоксичности и вместо этого выделяют молекулы, меняющие микросреду. Одна из таких молекул — декорин, небольшой белок с известными противоопухолевыми свойствами. Ключевая идея этой работы в том, что Т‑клетки, «запрограммированные» астмой, могут мигрировать из легких в мозг и выделять декорин в окружении оптической глиомы. Декорин конкурирует с CCL4 за CCR8 на микроглии, фактически блокируя часть опухолепитающего разговора и ослабляя NF-κB и CCL5 в клетках иммунной системы мозга.
Использование математики для отслеживания невидимой сети
Поскольку эта сеть сигнальных взаимодействий слишком сложна, чтобы понять её интуитивно, исследователи создали подробную математическую модель на основе дифференциальных уравнений. Модель отслеживает уровни ключевых молекул (мидкин, CCL4, декорин, NF-κB, CCL5), активность рецепторов на микроглии и рост опухолевых клеток с течением времени. Они калибровали модель с помощью экспериментальных данных о силе каждого взаимодействия и затем смоделировали множество сценариев. Модель показывает, как небольшие изменения в сродстве связывания — то есть насколько легко CCL4 или декорин прикрепляются к рецепторам — могут переключать микроглию между двумя режимами: промотирующим опухоль состоянием с высоким NF-κB и CCL5 и подавляющим опухоль состоянием с доминированием декорина и слабыми сигналами CCL4. Простой индекс, основанный на соотношении числа рецепторов, связанных с декорином, к числу рецепторов, связанных с CCL4, надежно предсказывает, будет ли опухоль расти или останавливаться.
Проектирование более разумных иммунотерапий
Помимо объяснения, почему астма может защищать от оптической глиомы, модель используется для изучения терапевтических стратегий. Она показывает, что терапии, повышающие уровень декорина или ослабляющие связь CCL4 с его рецепторами, могли бы замедлить рост опухоли. Авторы в цифрах тестируют подходы, такие как многократное введение Т‑клеток, продуцирующих декорин, или использование иммунного мессенджера IL‑2 для расширения полезных клеток в организме. Любопытно, что симуляции показывают: важно не только суммарная доза, но и расписание введений — умеренные, хорошо распределенные по времени дозы могут удерживать микроглию в состоянии, подавляющем опухоль, так же эффективно, как большие и редкие введения, при потенциально меньших побочных эффектах.
Что это означает для пациентов и семей
Для неспециалистов главный посыл такой: хроническое воспаление при астме, обычно считающееся вредным, иногда может перестроить иммунную систему так, что она мешает развитию некоторых опухолей мозга. Превращая Т‑клетки в «фабрики» декорина, астма, по-видимому, смещает баланс в зрительном нерве от благоприятной для роста среды к более враждебной для рака. Никто, разумеется, не предлагает использовать астму как терапию, но выявленные механизмы могут вдохновить новые методы лечения, воспроизводящие её защитные аспекты — например, таргетированные Т‑клеточные терапии или препараты, имитирующие блокирующее действие декорина — для защиты детей, подверженных риску оптической глиомы.
Цитирование: Lee, D., Lawler, S. & Kim, Y. Asthma-mediated control of optic glioma growth via T cell-microglia interactions: A mathematical model. npj Syst Biol Appl 12, 26 (2026). https://doi.org/10.1038/s41540-026-00647-w
Ключевые слова: оптическая глиома, астма, декорин, Т-клетки, математическое моделирование