Clear Sky Science · ru
Ингибирование CDK8 восстанавливает нарушенное ишемией заживление переломов
Почему кровоток важен при переломах
Большинство переломов в конечном счёте заживают, но у миллионов людей каждый год этот процесс останавливается. Плохое кровоснабжение вокруг перелома — ишемия — резко повышает риск того, что перелом будет заживать медленно, ненадёжно или вовсе не заживет. В этом исследовании изучают, почему это происходит на клеточном уровне, и проверяют экспериментальную таблетку, которая, похоже, смещает восстановление организма от рубцовой заделки обратно к настоящей регенерации кости.
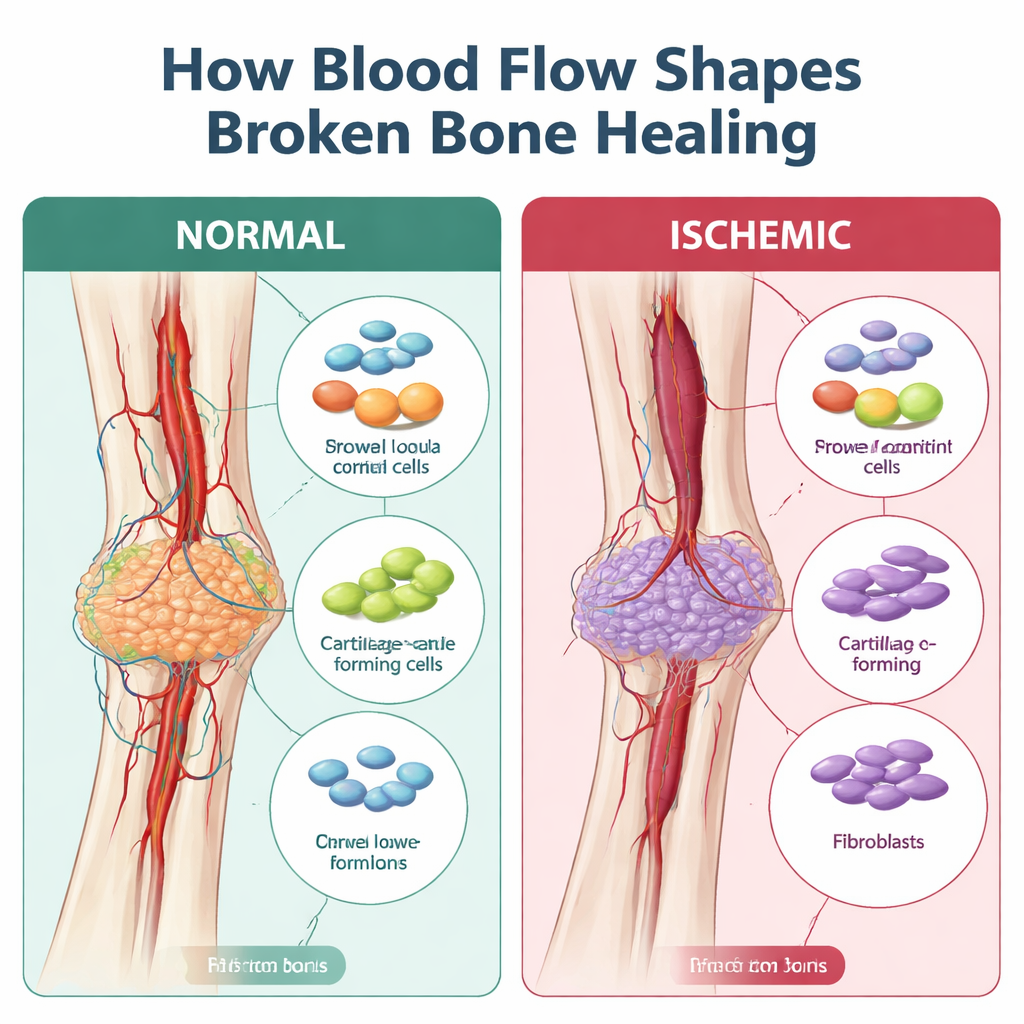
Когда заживление превращается в образование рубцовой ткани вместо восстановления
Обычно кость заживает путём образования мягкого хрящевого моста, который постепенно замещается твёрдой костью. Этот мост, называемый каллюсом, зависит от наличия стволоподобных поддерживающих клеток, иммунных клеток и кровеносных сосудов, согласующих ремонт. В ишемических переломах предыдущие работы показали, что каллюс обычно меньше, слабее и наполнен фиброзной тканью — скорее напоминает рубец, чем прочный участок новой кости. Не хватало подробной карты того, какие клетки дают сбой и когда именно во время этого отклонения от нормального заживления.
Одинарно-клеточные данные показывают ответвление в фиброз
Исследователи использовали модель на мышах, в которой артерия в ноге хирургически повреждается во время перелома, что точно имитирует потерю кровотока при тяжёлых травмах или у людей с сосудистыми заболеваниями или курящих. Затем они применили одноногие-РНК-секвенирование (single-cell RNA sequencing) — метод, считывающий активные гены в тысячах отдельных клеток — к каллюсам через четыре и семь дней после травмы. При хорошем кровоснабжении ранний каллюс был насыщен иммунными клетками, которые вскоре уступали место расширяющимся стромальным клеткам — поддерживающим клеткам, превращающимся в хрящ и кость. При ишемии же было значительно меньше клеток, образующих хрящ и кость, и гораздо больше фибробластов — клеток, откладывающих фиброзную ткань. Компьютерный анализ «траекторий» показал, что вместо плавного созревания от ранних предшественников в хрящ, стромальные клетки в ишемической кости часто отклонялись через состояние, похожее на фибробласты, что соответствует более рубцоподобному каллюсу, наблюдаемому под микроскопом.
Молекулярный «тормоз» на клетки, строящие кость
Изучая активность генов в этих клетках, команда обнаружила сильные признаки клеточного стресса в ишемических каллюсах, в том числе повышенные уровни белков теплового шока. Одним из самых заметных изменений было резкое повышение активности гена Cdk8, который кодирует регуляторный фермент, входящий в крупный транскрипционный комплекс и способный замедлять или перенастраивать ответ клеток на сигналы. Ранее Cdk8 уже отмечали как блокатор дифференцировки в других контекстах. Здесь он особенно усиливался в ранних стромальных предшественниках в ишемической кости. Человеческие мезенхимальные стромальные клетки, выращенные в условиях низкого содержания кислорода в лаборатории — имитируя плохое кровоснабжение — также увеличивали экспрессию CDK8, напрямую связывая недостаток кислорода с этим потенциальным «тормозом» на формирование хряща и кости.
Выключение CDK8 для восстановления заживления
Далее исследователи спросили, не позволит ли блокировка CDK8 стромальным клеткам вернуться к нормальному восстановлению. В клеточных культурах лечение мышиных и человеческих предшественников селективными ингибиторами CDK8 усиливало ключевые хрящевые гены и увеличивало синтез матрикса хряща, а также повышало минерализацию, когда те же клетки направляли в сторону образования кости. Затем команда протестировала перорально доступный ингибитор CDK8/19 под названием SNX631-6 на мышах с ишемическими переломами. При введении в ранний период образования хряща препарат увеличивал объём хряща в каллюсе. При продолжении лечения в более поздний период перехода от хряща к кости каллюсы демонстрировали больше общей кости, более высокое содержание минералов и больший общий объём на микро-КТ и тканевых срезах, что указывает на более надёжное структурное восстановление.
От лабораторного открытия к возможным новым терапиям
В целом результаты указывают на то, что ишемия направляет клетки заживления в состояние стресса и фибротического развития отчасти за счёт повышения активности CDK8, который сдерживает их способность становиться хрящом и костью. Блокировка этого фермента, по-видимому, снимает этот «тормоз», позволяя образовываться большему количеству хряща на раннем этапе и откладываться большему объёму кости позже, даже при нарушенном кровоснабжении. Поскольку ингибиторы CDK8 уже тестируются у онкологических пациентов, их в будущем могут перенаправить для помощи людям с высоким риском плохого заживления переломов — таким как пожилые, курящие или пациенты с сосудистыми заболеваниями — чтобы они восстанавливали прочную кость вместо хрупкой рубцовой ткани.
Цитирование: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Ключевые слова: заживление переломов кости, ишемия, ингибитор CDK8, мезенхимальные стромальные клетки, фиброз