Clear Sky Science · ru
Пересадка альвеолярных эпителиальных клеток II типа дикого типа у мышей с дефицитом белка сурфактанта C
Почему важно восстанавливать крошечные воздушные мешочки
Дыхание может казаться простым и незаметным, но оно зависит от тонкой пленки — сурфактанта, покрывающего миллионы крошечных воздушных мешочков в легких. Когда сурфактанта не хватает или он дефектен, как при некоторых редких детских болезнях легких, дети страдают от постоянных затруднений дыхания и образования рубцовой ткани. Сегодня единственное настоящее лечение — пересадка легких, что ограничено нехваткой доноров и серьезными рисками. В этом исследовании рассматривается другой подход: восстановление поврежденных легких путем пересадки здоровых клеток, производящих сурфактант, что потенциально открывает путь к более щадящим и таргетным методам лечения.
Когда «сторожевые» клетки легких дают сбой
Внутри каждого воздушного мешочка (альвеолы) находятся специализированные «сторожевые» клетки — альвеолярные клетки II типа. Они производят и рециркулируют сурфактант, который не дает альвеолам спадаться и облегчает дыхание. У некоторых детей мутации в генах, необходимых для синтеза сурфактанта, включая ген SFTPC, нарушают работу этих клеток. В результате развивается интерстициальное заболевание легких у детей (chILD), которое проявляется воспалением, утолщением легочной ткани, образованием рубцов и иногда дыхательной недостаточностью. Врачи могут лишь назначать симптоматические препараты и кислород; для наиболее тяжело пораженных последней инстанцией остается трансплантация легких. Авторы поставили задачу выяснить, может ли замена части дефектных «сторожевых» клеток на здоровые замедлить или обратить повреждение легких.
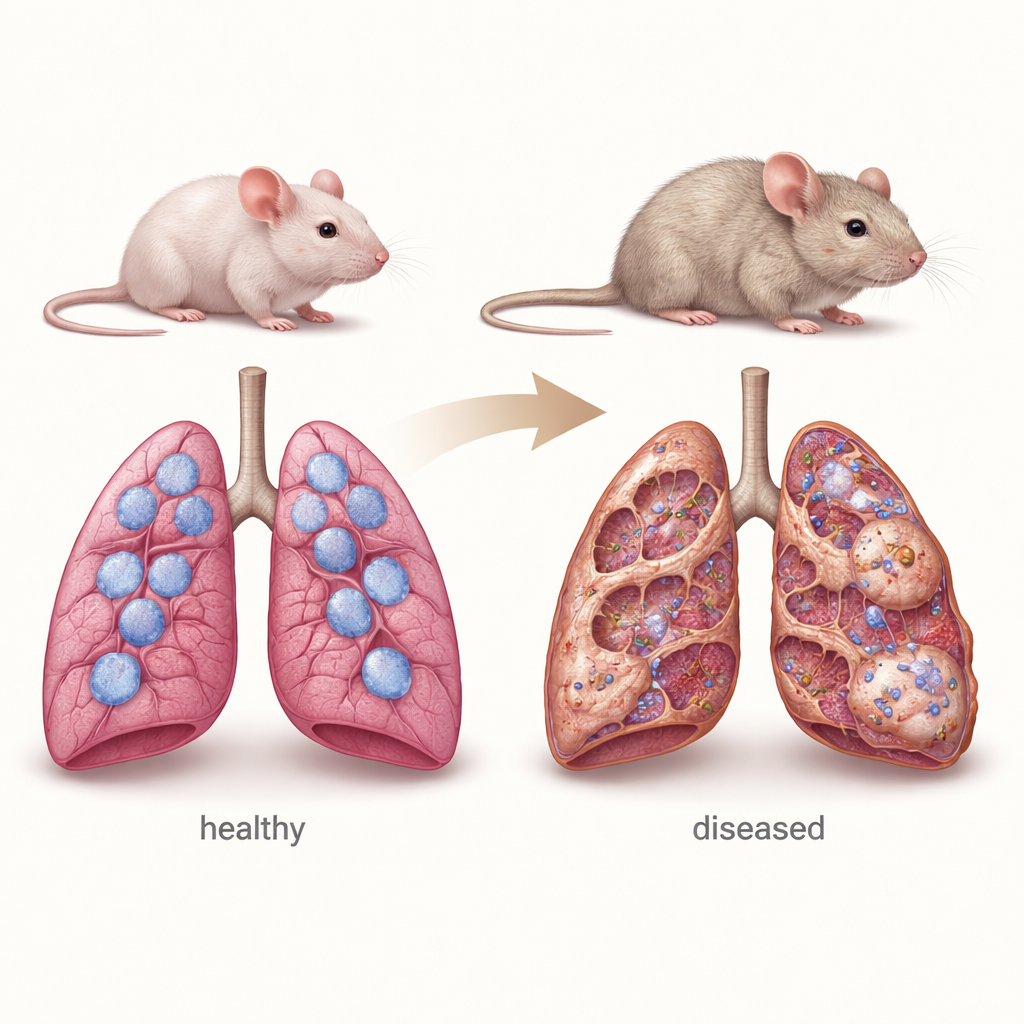
Мышиная модель детского заболевания легких
Чтобы воспроизвести ключевые черты chILD, исследователи использовали мышей с полным отсутствием гена Sftpc. Эти животные рождаются с внешне нормальными легкими, но с возрастом у них развиваются характерные черты хронического заболевания легких: утолщение стенок между альвеолами, избыток рубцовой ткани, богатой коллагеном, разрастание клеток II типа и скопление иммунных клеток. Подробные измерения показали, что архитектоника их легких постепенно ухудшается в период от 4 до 12 месяцев, напоминая медленное прогрессирование, наблюдаемое у многих пациентов. Команда также обнаружила, что эти мыши особенно чувствительны к химиотерапевтическому препарату блеомицину, который часто используют в лабораториях для индукции повреждения легких и фиброза, что дополнительно подчеркивает уязвимость их легких при дефиците сурфактанта.
Подготовка поврежденных легких к приему новых клеток
Успешная пересадка новых клеток в уже «переполненный» орган — нетривиальная задача. Авторы проверяли, может ли тщательно подобранная низкая доза блеомицина действовать как своего рода «кондиционирующая» обработка — повреждать часть дефектных туземных клеток и освобождать место для чужаков, не разрушая легкое. У мышей с дефицитом Sftpc даже небольшие дозы блеомицина усугубляли образование рубцов и снижали уровни нескольких ключевых маркеров клеток II типа, подтверждая повреждение. Тем не менее при самой низкой дозе ущерб был ограниченным, а собственный репаративный ответ легкого оставался активным. Этот баланс указывал на окно возможностей, в котором пересаженные клетки имели наилучшие шансы прижиться, выжить и внести вклад в восстановление.
Здоровые клетки сурфактанта заселяют легкое и начинают работать
Далее команда выделила здоровые клетки II типа из нормальных мышей и доставила миллион таких клеток непосредственно в дыхательные пути мышей с дефицитом Sftpc через десять дней после введения низкой дозы блеомицина. С помощью сочетания белкового окрашивания и генетических тестов они показали, что донорные клетки эффективно прижились, особенно у молодых животных. Пересаженные клетки синтезировали зрелый белок сурфактанта C — полностью отсутствовавший у хозяина — что свидетельствует о том, что они были не только присутствующими, но и функционально активными. Новые клетки сохранялись по крайней мере два месяца. Важно, что у мышей, получивших пересадку клеток, имело место меньше повреждений легких и меньше сильно пораженных участков по сравнению с мышами, которым вводили только блеомицин, что указывает на то, что даже частичная замена больных клеток может смягчить продолжающееся повреждение.
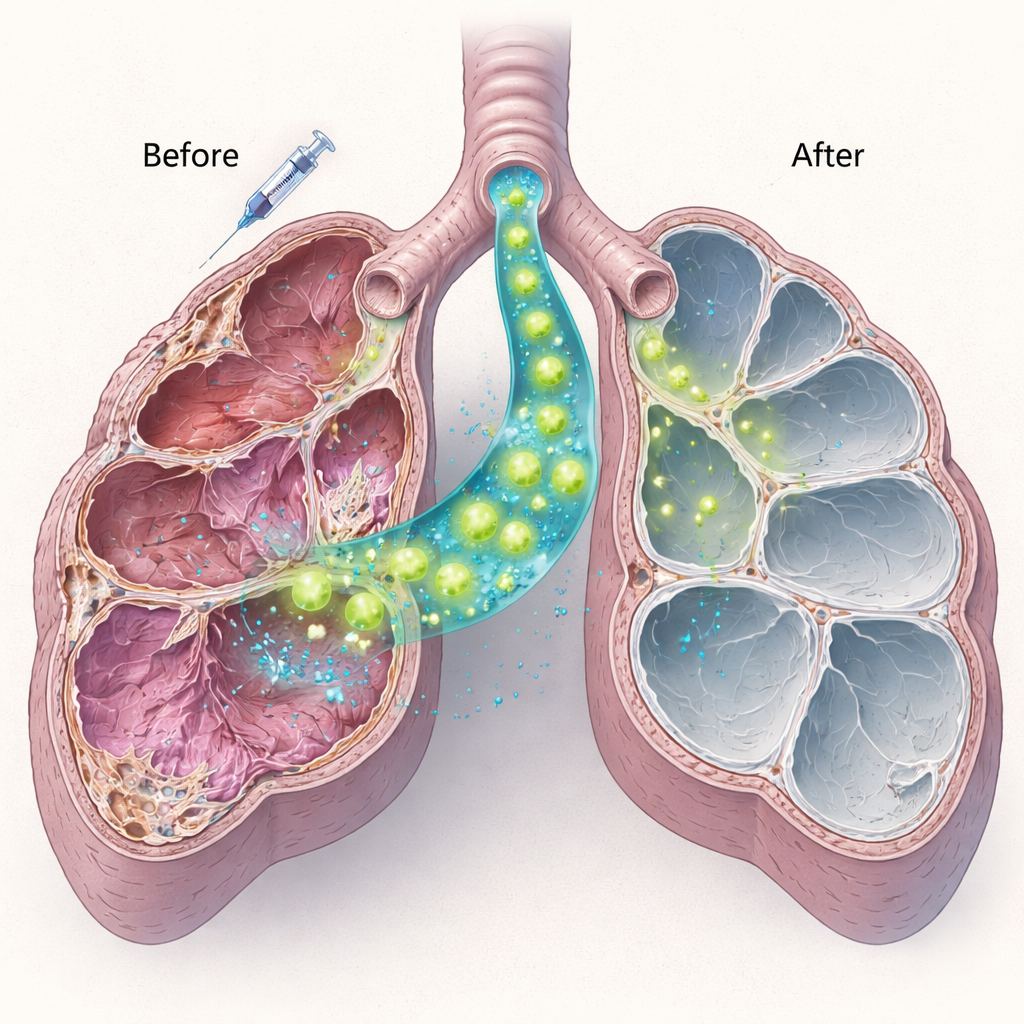
От доказательства концепции к будущим терапиям
Для неспециалистов главный вывод в том, что это исследование демонстрирует реалистичный путь к восстановлению, а не замене, легких при некоторых генетических детских заболеваниях. Показав, что скромное количество здоровых клеток, производящих сурфактант, может укорениться в хронически больном легком, восполнить отсутствующий белок и уменьшить повреждение, работа закладывает основу для будущих терапий на основе генокорректированных или полученных из стволовых клеток клеток легкого. Остается много препятствий, включая поиск более безопасных способов подготовки человеческих легких к такому лечению и обеспечение длительного эффекта. Тем не менее это исследование смещает обсуждение от управления симптомами в сторону потенциального восстановления собственных механизмов легких для здорового дыхания.
Цитирование: Predella, C., Lapsley, L., Ni, K. et al. Engraftment of wild-type alveolar type II epithelial cells in surfactant protein C deficient mice. npj Regen Med 11, 11 (2026). https://doi.org/10.1038/s41536-026-00455-0
Ключевые слова: интерстициальное заболевание легких у детей, белок сурфактанта C, альвеолярные клетки II типа, клеточная терапия, легочный фиброз