Clear Sky Science · ru
Мутация LRRK2R1627P усиливает хроническое воспаление, вызванное факторами окружающей среды, и агрегирование α-синуклеина в кишечнике крыс
Почему кишечник важен при заболевании мозга
Болезнь Паркинсона в первую очередь известна тремором и нарушениями движений, но накопляющиеся данные указывают на то, что её истоки могут начинаться далеко от мозга — глубоко в кишечнике. В этом исследовании изучается, как конкретное генетическое изменение, связанное с Паркинсоном в азиатских популяциях, вместе со старением и воздействием токсинов может постепенно повреждать кишечник крыс. Наблюдая за тем, что происходит в кишечнике на протяжении жизни животных, исследователи прослеживают, как повседневные иммунные реакции могут перейти в хроническое воспаление, создавая условия для накопления белков, связанных с болезнью, что в конечном итоге может угрожать мозгу.
Рискованный ген в пищеварительном тракте
Ученые сосредоточились на варианте гена LRRK2, давно связанном с болезнью Паркинсона и некоторыми воспалительными заболеваниями кишечника. Они создали крыс с аналогичной мутацией, названной LRRK2R1627P, и сравнили их с нормальными животными на протяжении жизни. Хотя уровень мРНК LRRK2 в кишечнике не изменился, общий уровень белка LRRK2 и одного из ключевых маркеров его активности снизились, что указывает на ослабление нормальной функции этого белка в кишечнике. Это тонкое молекулярное изменение не вызывало драматического раннего повреждения, но незаметно изменяло способы обновления и организации кишечных клеток по мере старения животных.
Стареющий кишечник под медленным, постоянным напряжением
С течением месяцев у крыс с мутацией появились явные признаки нарушения структуры кишечника. Их тонкая кишка стала короче, а тонкие ворсинки и крипты, поглощающие питательные вещества, уменьшились. Число некоторых специализированных клеток эпителия, вырабатывающих защитную слизь и антимикробные вещества — бокаловидных клеток и панетовских клеток — сократилось, а белки, обеспечивающие плотные, непроницаемые контакты между соседними клетками, тоже уменьшились. Под микроскопом эти контакты стали короче или шире, что указывает на ослабление барьера. Важно, что общая архитектура не разрушилась; скорее, кишечник демонстрировал более коварную картину сниженного обновления и защиты, что делает его более уязвимым к раздражению и инфекции. 
Иммунная система на взводе
Чтобы понять, почему кишечник терял равновесие, команда изучила активность генов и иммунные клетки в стенке кишечника. Они обнаружили, что пути, связанные с сенсором TLR4 и его партнером NF-κB, были сверхактивны у старых животных с мутацией. Эти сенсоры обычно помогают организму обнаруживать вредные микроорганизмы, но здесь они способствовали накоплению «атакующих в первую очередь» иммунных клеток, известных как макрофаги M1. Эти клетки выделяли провоспалительные молекулы, превращая кишечник в хронически раздраженную среду. Поразительно, что белок, связанный с Паркинсоном, α-синуклеин в своей фосфорилированной, связанной с болезнью форме, начал накапливаться не в нейронах кишечника, а внутри этих активированных макрофагов в тонкой кишке, особенно у старых животных.
Повышенная чувствительность к внешним воздействиям
Генетическая мутация сама по себе не объясняла всю картину. Когда молодых крыс кратко подвергали воздействию бактериального токсина (LPS), который стимулирует TLR4, животные с мутацией LRRK2 развивали гораздо более выраженное воспаление кишечника, чем их нормальные собратья. У них сильнее отслаивался эпителий, белки барьера падали еще сильнее, и количество провоспалительных макрофагов резко увеличивалось, вновь сопровождаясь накоплением аномального α-синуклеина. Это говорит о том, что люди с похожими мутациями могут быть особенно чувствительны к внешним факторам, нарушающим кишечник — таким как некоторые инфекции или токсины — что усиливает их долгосрочный риск.
Ослабление сигнала тревоги
Поскольку TLR4 оказался в центре этой воспалительной бури, команда протестировала препарат TAK-242, который специфически подавляет сигнализацию TLR4. Прием препарата в течение нескольких месяцев взрослеющими крысами в основном восстановил длину тонкой кишки, размеры ворсинок и крипт, количество клеток, продуцирующих слизь, и белков барьера. Он снизил активность макрофагов, уменьшил уровень воспалительных молекул и резко сократил накопление аномального α-синуклеина в кишечнике. Одновременно препарат нормализовал состав микробного сообщества: увеличилось разнообразие, избыточный рост Lactobacillus снизился, несколько полезных групп бактерий восстановились, а прогнозируемые функции микробиоты сместились в сторону менее ассоциированных с заболеванием паттернов. 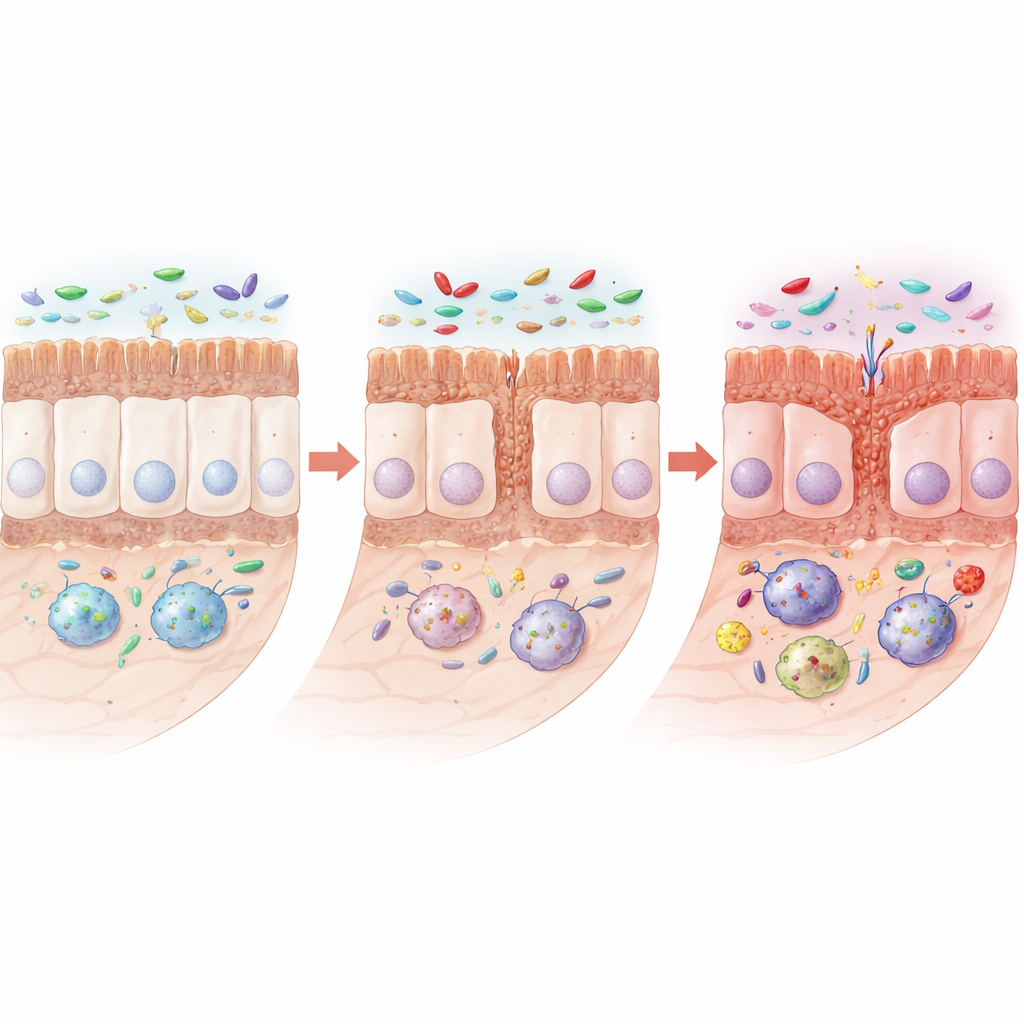
Что это значит для риска развития Паркинсона
Для неспециалиста смысл в том, что «ген Паркинсона» может тихо перестраивать иммунную защиту кишечника с течением времени, особенно на фоне старения и внешнего стресса. У этих крыс результат — хроническое, низкоуровневое воспаление, которое ослабляет кишечный барьер, нарушает состав местной микробиоты и приводит к накоплению белка, связанного с Паркинсоном, в иммунных клетках — не полноценный Паркинсон, но биологическая обстановка, которая может способствовать развитию болезни в мозге позже. Показав, что блокирование одного кишечного иммунного пути может обратить многие из этих изменений, исследование подчеркивает кишечник как практическую раннюю мишень: защита здоровья кишечника и подавление кишечного воспаления могут помочь отложить или предотвратить развитие Паркинсона у людей с генетическим риском.
Цитирование: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Ключевые слова: Болезнь Паркинсона, воспаление кишечника, мутация LRRK2, микробиом, врожденный иммунитет