Clear Sky Science · ru
Систематическая оценка регуляторов морфологии митохондрий для улучшения нейрональной α‑синуклеинопатии
Почему крошечные электростанции важны при заболеваниях мозга
Митохондрии, «электростанции» клетки, жизненно необходимы для выживания нейронов и поддержания их связей. При заболеваниях мозга, таких как болезнь Паркинсона, эти крошечные структуры часто выглядят повреждёнными или фрагментированными, однако долгое время было сложно понять, какие изменения вредны, а какие переключатели можно безопасно задействовать для их защиты. В этом исследовании систематически тестируют ключевые «регуляторы формы» митохондрий в лабораторной модели, имитирующей накопление белка, связанное с Паркинсоном, используя инструмент искусственного интеллекта для измерения формы митохондрий в разных частях нейронов. Работа указывает на один конкретный регулятор, называемый Fis1, как на перспективную мишень для сохранения митохондрий — и синапсов — здоровыми без появления новых побочных эффектов.
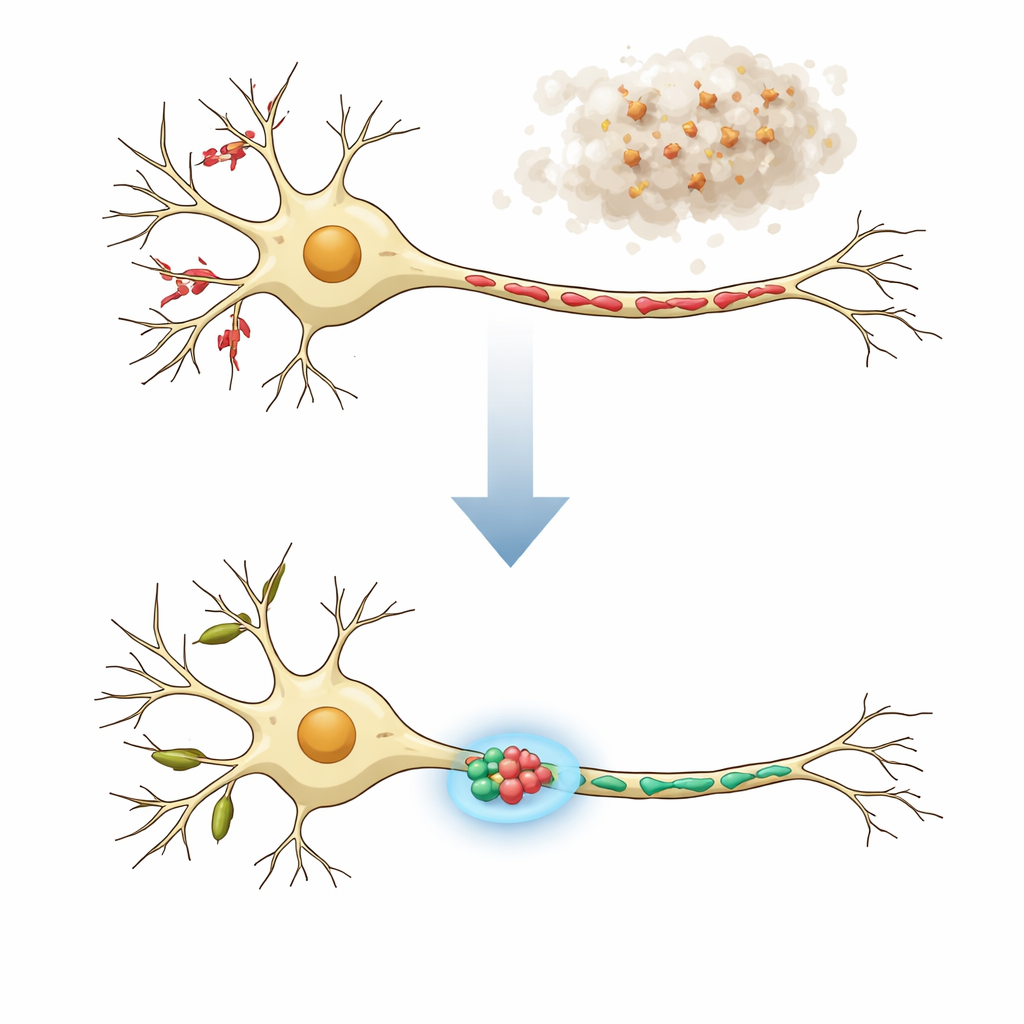
Два «района» одного нейрона
Нейроны неоднородны: их ветвистые отростки (дендриты) и длинные «кабели» (аксон) выполняют разные функции и содержат митохондрии с весьма отличающейся формой. В здоровых клетках в дендритах обычно присутствуют длинные трубчатые митохондрии, которые поддерживают локальную синтезу белка и гибкую коммуникацию в местах приёма — дендритных шипиках. Аксон, ответственный за передачу сигналов, вместо этого содержит множество коротких митохондрий, обеспечивающих энергию и помогая регулировать уровень кальция в пресинаптических терминалях. При нейродегенеративных заболеваниях и функция, и структура этих митохондрий могут нарушаться, проявляясь в виде фрагментации, вздутых форм или «бусообразных» нитей. Авторы исходили из того, что по-настоящему эффективные стратегии лечения должны восстанавливать митохондрии в дендритах и аксонах до их нормальных, специфичных для компартмента форм.
Создание стресс‑теста, похожего на болезнь Паркинсона
Чтобы смоделировать ключевую особенность болезни Паркинсона и родственных расстройств, исследователи подвергли культивируемые корковые нейроны мыши воздействию предварительно сформированных фибрилл альфа‑синуклеина — белка, который может образовывать вредные агрегаты. В течение нескольких дней эти фибриллы вызывали аномальное накопление альфа‑синуклеина в клетках и приводили к выраженной фрагментации митохондрий как в дендритах, так и в аксонах. С помощью MitoVis, системы глубокого обучения для анализа изображений, команда автоматически разделяла дендриты и аксоны на микроскопических снимках и измеряла длину, площадь и форму сотен митохондрий на изображение примерно в десять раз быстрее, чем при ручной трассировке. Этот высокопроизводительный подход подтвердил, что при болезненном состоянии митохондрии укорачиваются и становятся более округлыми, что согласуется с данными из модельных животных и тканей пациентов.
Тестирование «переключателей» формы митохондрий
Далее команда проверила, можно ли предотвратить это повреждение, смещая баланс конкретных белков слияния и деления митохондрий. Усиление двух белков слияния (Mfn1 и Mfn2) или подавление белка деления (Mff) действительно защищало дендритные митохондрии от укорачивания, вызванного альфа‑синуклеином, и также предотвращало потерю дендритных шипиков. Однако те же манипуляции делали аксональные митохондрии чрезмерно длинными, что в предыдущих работах связывали с проблемами высвобождения сигнала и ветвления аксона. В отличие от этого, снижение другого белка деления, Fis1, восстановило длину митохондрий в дендритах и аксонах до почти нормальных значений без чрезмерного удлинения. Важно, что в этой настройке уменьшение Fis1 не вызывало гибели нейронов и, подобно другим вмешательствам, сохраняло плотность дендритных шипиков, которые в противном случае уменьшались бы под стрессом от альфа‑синуклеина.
Сохранение баланса кальция
Поскольку митохондрии в аксонах помогают буферизовать кальций во время электрической активности, исследователи проверили, влияет ли изменение их формы на этот тонкий баланс. Они использовали флуоресцентный кальциевый датчик, направленный в митохондрии пресинаптических бантонов, и стимулировали аксоны короткими вспышками потенциалов действия. В состоянии с альфа‑синуклеином обработка кальция в слегка укороченных аксональных митохондриях выглядела похожей на нормальную. Но когда аксональные митохондрии становились чрезмерно длинными из‑за сверхэкспрессии Mfn1 или подавления Mff, они поглощали больше кальция, чем обычно, после стимуляции. Это усиленное поглощение могло нарушать пресинаптическую функцию. Напротив, снижение Fis1, которое нормализовало, но не приводило к избыточной длине митохондрий, сохраняло митохондриальные кальциевые ответы, близкие к контролю, что указывает на меньшее количество скрытых компромиссов.
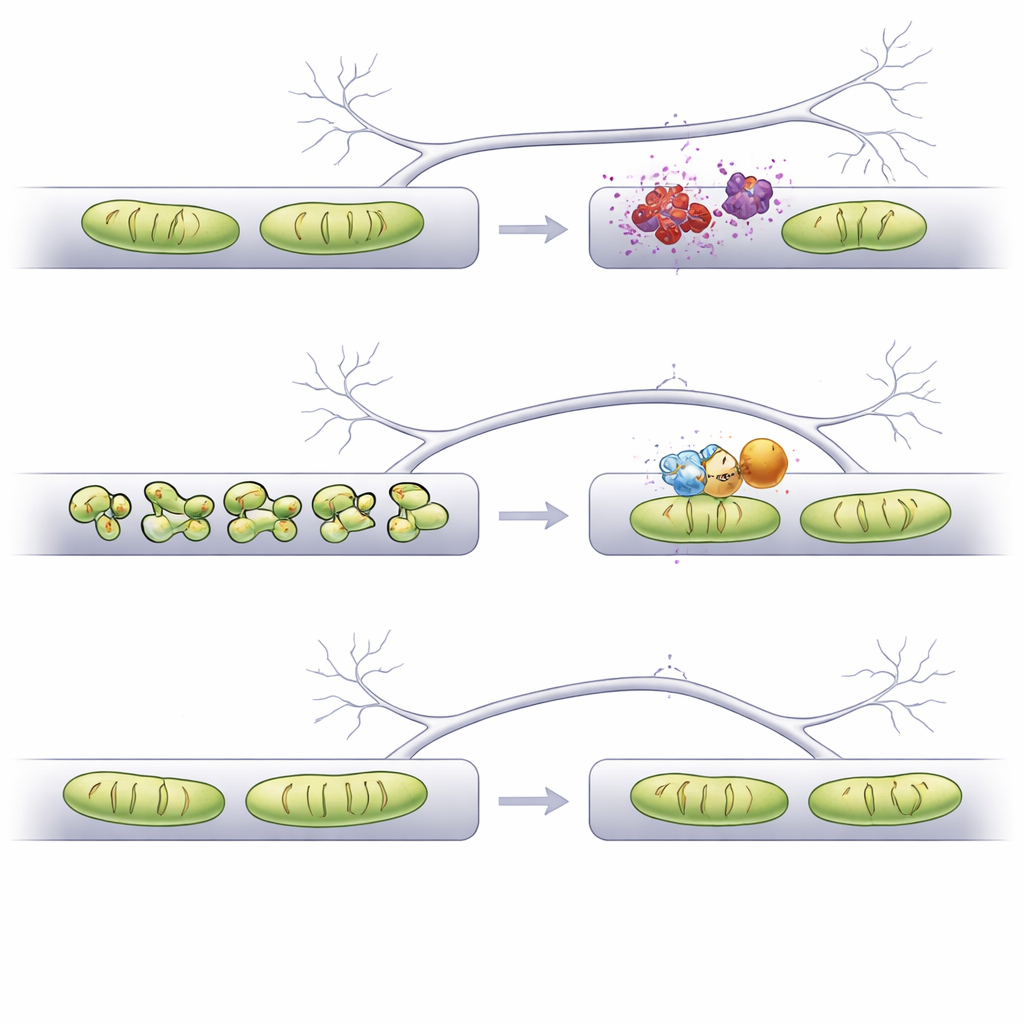
Что это может означать для будущих терапий
В совокупности исследование показывает, что простое удлинение митохондрий недостаточно — важно восстановить их форму до правильного размера в нужном компартменте. С помощью AI‑помощника для анализа изображений авторы выделяют Fis1 как особенно привлекательную мишень: его подавление стабилизирует структуру митохондрий в дендритах и аксонах, предотвращает потерю дендритных шипиков и избегает аномальной обработки кальция в пресинаптических терминалях. Эти результаты поддерживают идею о том, что тонкая настройка формы митохондрий, потенциально с помощью лекарств или антисмысловых молекул, направленных на Fis1, может помочь защитить уязвимые синапсы при альфа‑синуклеинопатии, связанной с Паркинсоном, и, возможно, при других заболеваниях мозга, где митохондрии выходят из строя.
Цитирование: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
Ключевые слова: Болезнь Паркинсона, митохондрии, альфа‑синуклеин, синаптическая дисфункция, нейродегенерация