Clear Sky Science · ru
Клиническая польза вызванных потенциалов для настройки глубокой стимуляции субталамического ядра при болезни Паркинсона
Почему эта история про «мозговой кардиостимулятор» важна
У многих людей с болезнью Паркинсона со временем медикаменты перестают работать гладко. Симптомы могут колебаться между скованностью и неконтролируемыми движениями, а доведение лечения до оптимума превращается в изнурительный цикл визитов в клинику. В этом обзорном материале рассматривается, как врачи могут использовать собственные электрические «эхо» мозга — так называемые вызванные потенциалы — для более быстрого и объективного программирования глубокой стимуляции мозга (DBS). По сути, статья задаёт вопрос, можно ли превратить подбор параметров DBS из аккуратного предположения в более основанный на данных, персонализированный «мозговой кардиостимулятор».
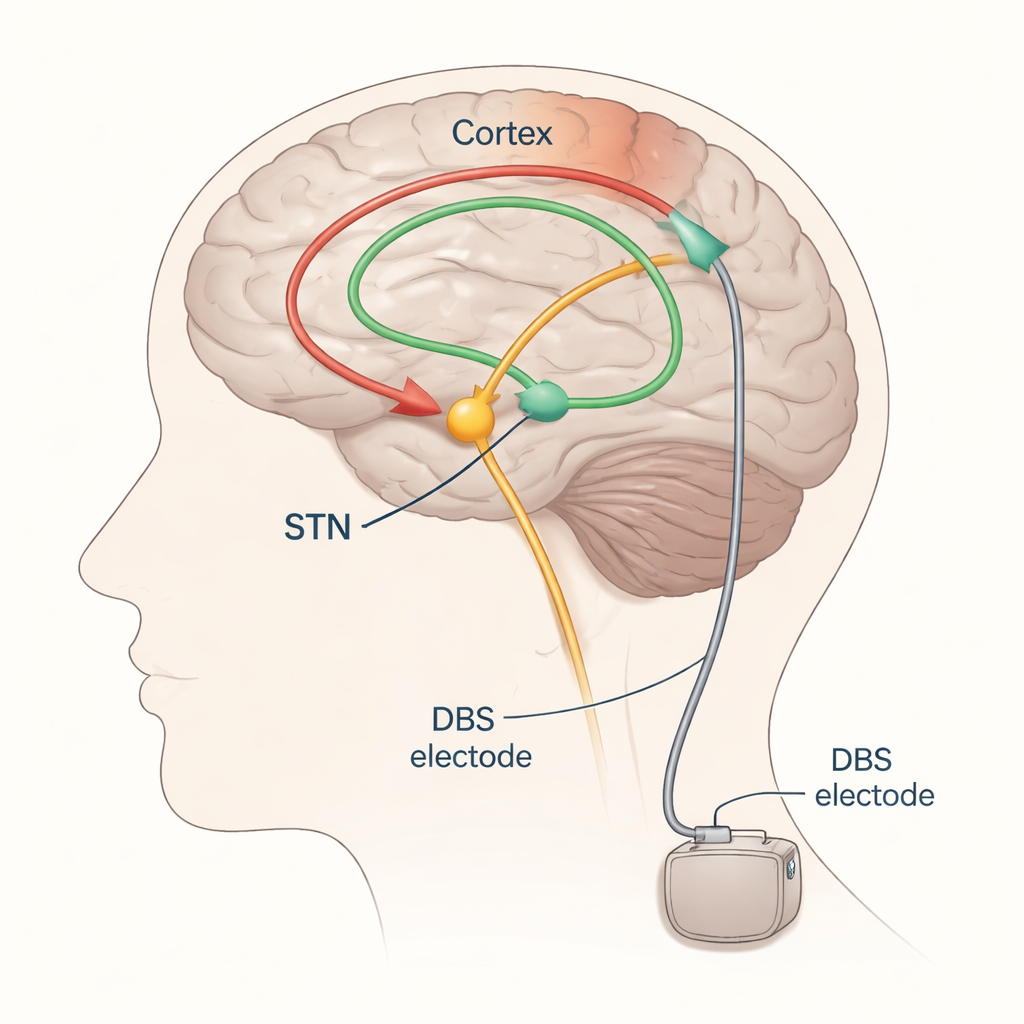
От метода проб и ошибок к направленной настройке
DBS при болезни Паркинсона чаще всего нацелена на небольшую глубокую структуру мозга — субталамическое ядро (СТН). В это ядро имплантируются электроды, подключённые к генератору импульсов под кожей грудной клетки. При правильной настройке стимуляция СТН может смягчать тремор, брадикинезию и ригидность, но если электрическое поле распространяется слишком широко, оно может случайно возбуждать соседние пути, контролирующие мышцы или чувствительность, вызывая побочные эффекты вроде судорожных тянущих сокращений или покалываний. Сегодня неврологи обычно настраивают DBS, постепенно меняя параметры и наблюдая за движениями пациента и побочными эффектами — подход, требующий много времени, зависящий от самочувствия пациента в конкретный день и часто требующий нескольких контрольных визитов.
Слушая электрические «эхо» мозга
Авторы сосредоточены на вызванных потенциалах — крошечных, синхронизированных по времени электрических ответах в мозге или мышцах после стимуляции — как на потенциальных ориентирах для хороших и плохих настроек DBS. При стимуляции СТН волны активности распространяются по нервным путям и могут регистрироваться на коже головы с помощью ЭЭГ, в мышечной активности с помощью ЭМГ или иногда с помощью регистрирующих полосок, размещённых прямо на поверхности мозга. Повторяя стимуляцию на низкой частоте и усредняя ответы, исследователи устойчиво обнаруживают отдельные волны, появляющиеся с разной задержкой (в миллисекундах) после каждого импульса. Ранние волны, приходящие примерно в пределах двух тысячных секунды, в основном отражают активацию быстрых моторных путей, пролегающих рядом с электродом. Немного более поздние волны, около трёх миллисекунд (часто называемые компонентом «P3»), считаются возникающими из прямой связи между лобной корой и СТН — так называемого гиперпрямого пути. Ещё более поздние волны, скорее всего, идут по более длинным, петляющим цепям, включающим таламус и другие глубокие ядра.
Нахождение «сладкого места» и избежание проблем
Во многих исследованиях складывается последовательная картина: контакты на электроде DBS, которые дают выраженный коротколатентный P3, как правило, находятся в наиболее полезной части СТН и связаны с лучшим улучшением моторных симптомов паркинсонизма и более широким «терапевтическим окном» до появления побочных эффектов. Напротив, очень ранние волны, связанные с моторными путями, и определённые ответы на 8–10 миллисекунд часто указывают на то, что стимуляция распространяется в соседние структуры, повышая риск мышечных сокращений или других нежелательных эффектов. Отдельные замеры моторных вызванных потенциалов (ЭМГ-ответы в мышцах лица и конечностей) и соматосенсорных вызванных потенциалов (ЭЭГ-узоры, связанные с тактильными путями) могут выявить тонкую активацию внутренней капсулы или медиальной лемнискуса — пучков волокон, которые проводят моторные команды и сенсорную информацию. Раннее обнаружение таких изменений позволяет клиницистам отвести ток от рискованных зон, выбирая другие контакты или корректируя форму и полярность импульса.
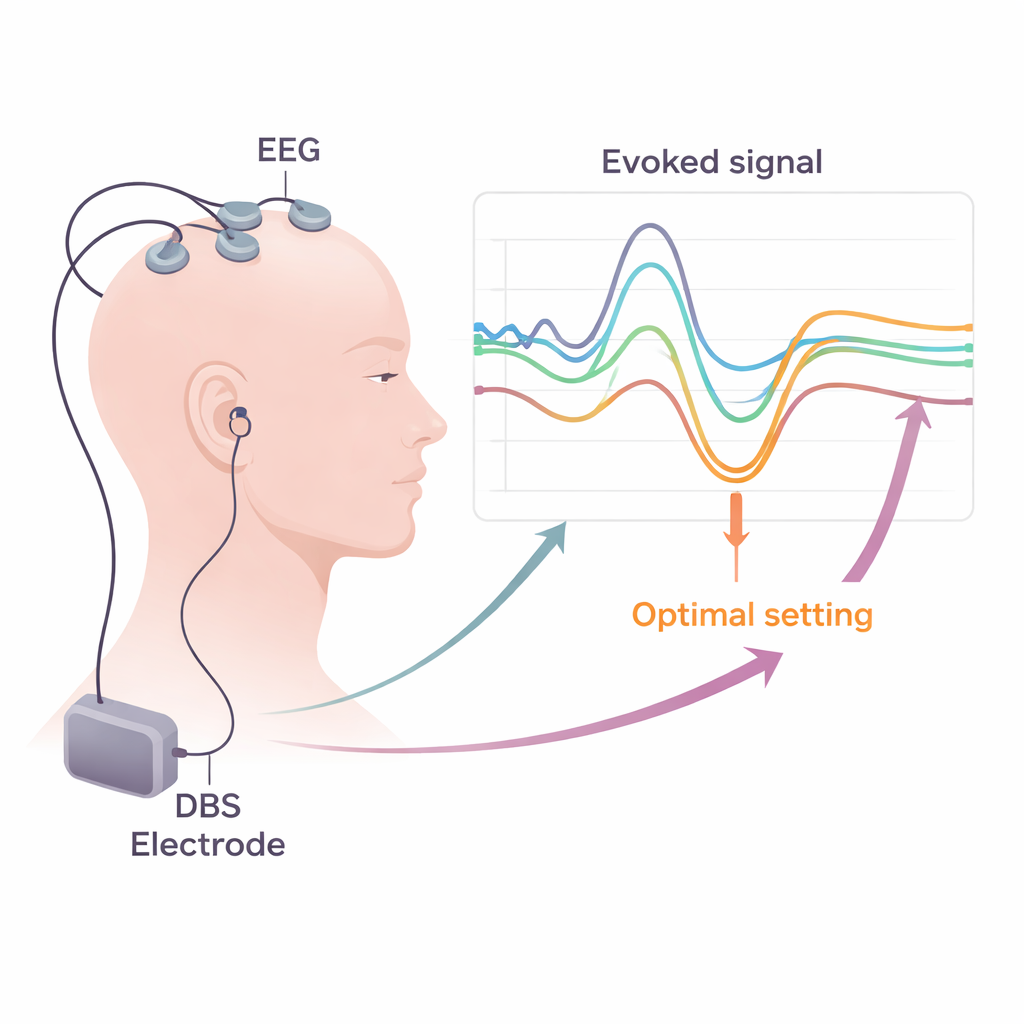
Как сделать лабораторные инструменты практичными в клинике
Перенести эти идеи в рутинную практику требуют практических решений. Обзор объясняет, как стандартные больничные системы ЭЭГ и ЭМГ уже способны записывать большинство необходимых сигналов при условии использования высокой частоты дискретизации и аккуратных методов удаления электрических «шумов» от импульсов DBS. Авторы обсуждают стратегии снижения артефактов, такие как удачное ререферирование, вычитание шаблонов и современные компьютерные алгоритмы, отделяющие истинную мозговую активность от остатков стимуляции. Они предлагают, что короткие, структурированные тестовые сессии — сочетание кратковременной низкочастотной DBS, записи с кожи головы и мониторинга мышц в покое и при лёгком напряжении — можно встроить в обычную неделю постоперационного программирования. Карты вызванных потенциалов для каждого контакта затем могут комбинироваться с визуализацией и другими биомаркерами, чтобы ориентироваться, какие контакты и параметры использовать в долгосрочной перспективе.
Что это значит для людей с болезнью Паркинсона
В статье делается вывод, что вызванные потенциалы являются перспективными кандидатами для того, чтобы сделать настройку DBS более точной, эффективной и предсказуемой. В частности, коротколатентная волна P3 выглядит сильным маркером того, что стимуляция достигает нужной цепи для облегчения моторных симптомов Паркинсона, тогда как моторные и сенсорные вызванные ответы могут сигнализировать о вытекании тока в пути, вызывающие побочные эффекты. Хотя требуется дополнительная работа по стандартизации методов и доказательству пользы в повседневной практике, этот подход нацелен на будущее, в котором врачи смогут «слушать» мозг во время программирования, быстро находить индивидуальное «сладкое место» и снижать бремя метода проб и ошибок для людей, живущих с болезнью Паркинсона.
Цитирование: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Ключевые слова: Болезнь Паркинсона, глубокая стимуляция мозга, вызванные потенциалы, картирование мозга, нейрофизиология