Clear Sky Science · ru
Ингибирование de novo синтеза церамидов ослабляет патологию альфа‑синуклеина в модели болезни Паркинсона на мышах
Почему жиры в мозге важны при болезни Паркинсона
Болезнь Паркинсона известна прежде всего дрожанием рук и замедленностью движений, но глубоко в мозге развивается более тихая драма. Нервные клетки, контролирующие движение, постепенно погибают, когда белок альфа‑синуклеин сворачивается в липкие агрегаты. В этом исследовании показано, что особая группа жиров — церамиды — способствует этому повреждению, и что блокирование их синтеза может защитить клетки мозга у мышей и в моделях на человеческих клетках. Работа указывает на неожиданный, доступный для лекарственной модуляции путь, который однажды может замедлить или предотвратить болезнь Паркинсона, а не просто облегчать её симптомы.
Подсказки из посмертных анализов мозга
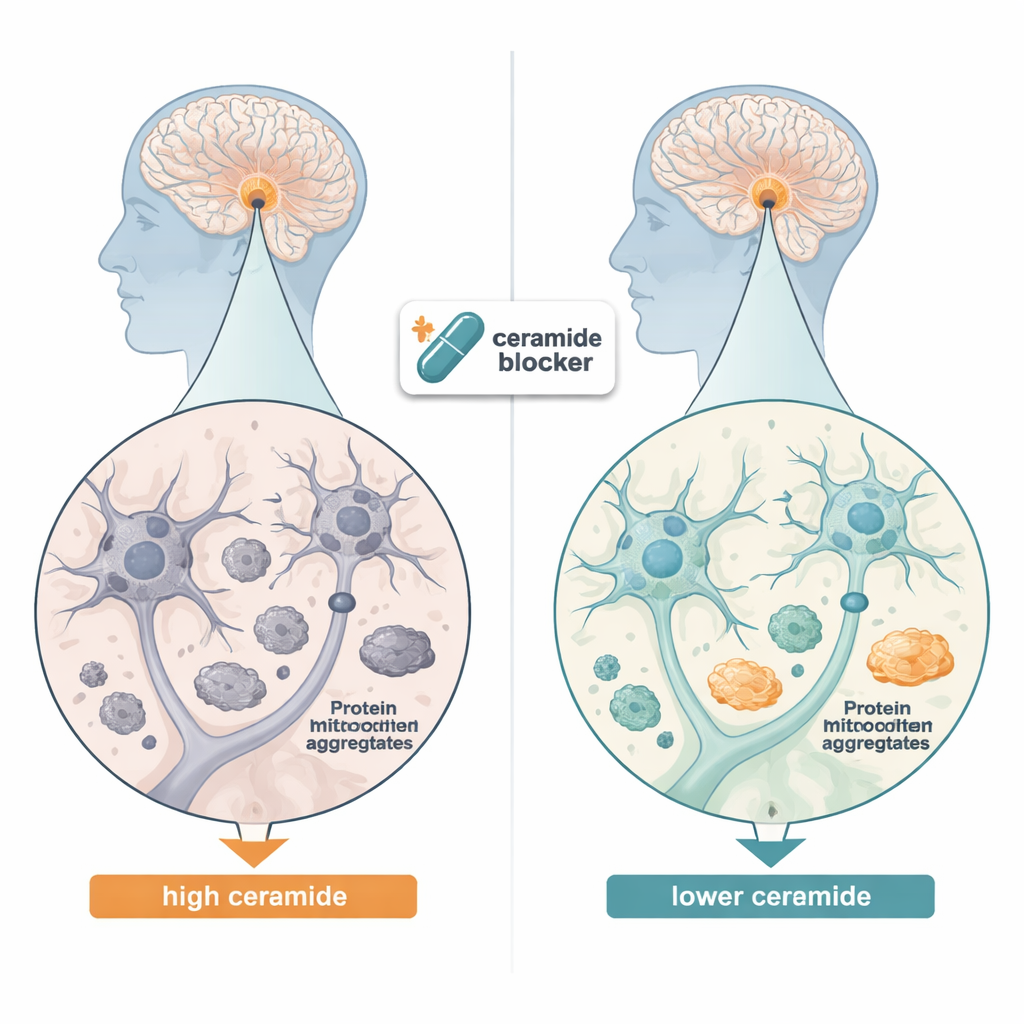
Чтобы понять, вовлечены ли церамиды в болезнь Паркинсона и родственные состояния, исследователи сначала изучили посмертную ткань мозга людей с деменцией с тельцами Леви — заболеванием, в котором появляются те же токсические белковые включения, что и при Паркинсоне. При помощи чувствительных химических измерений они обнаружили, что многие виды церамидов были значительно повышены в среднем мозге по сравнению со здоровыми образцами, особенно формы с длинными жирными хвостами. Затем они повторно проанализировали крупные генетические наборы данных из человеческих клеток мозга и выявили, что гены, ответственные за синтез и переработку церамидов, были более активны в дофамин-продуцирующих нейронах пациентов с Паркинсоном, а также в некоторых вспомогательных клетках, таких как астроциты и олигодендроциты. В совокупности эти результаты указывают на нарушение баланса церамидов в нескольких типах клеток в поражённом мозге.
Уборка белковых сгустков в клетках
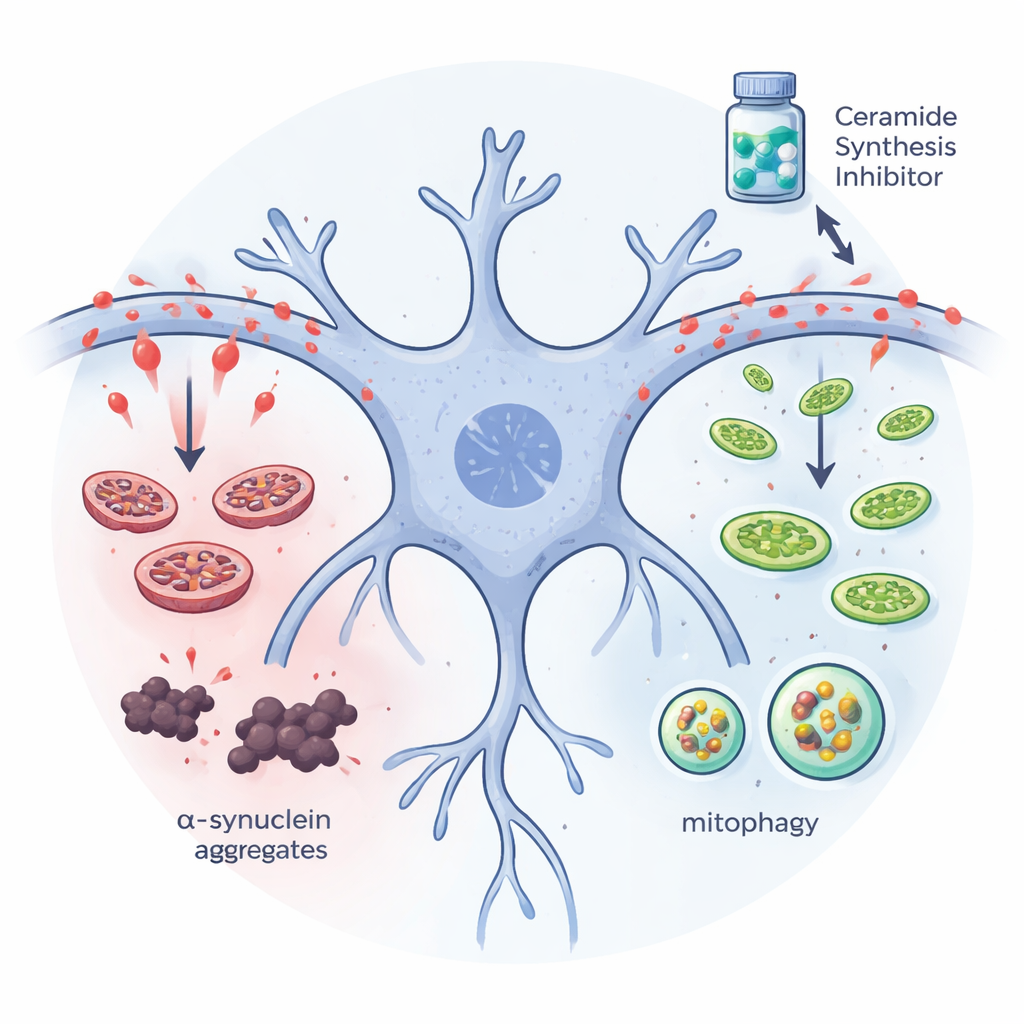
Далее команда спросила, может ли снижение уровня церамидов уменьшить накопление белка в клетках, похожих на нервные, выращенных в лаборатории. Они использовали человеческие нейробластомные клетки, модифицированные для перепроизводства мутантной формы альфа‑синуклеина, склонной к агрегации. Когда они блокировали первый шаг синтеза церамидов — либо заглушая ген ключевого фермента, либо добавляя препарат мириоцин — количество нерастворимых агрегатов альфа‑синуклеина резко снизилось. Одновременно увеличились маркёры митофагии, специализированной системы клетки по выявлению и переработке повреждённых митохондрий, и активизировался механизм пометки нежелательных белков для утилизации. Эти сдвиги предполагают, что избыток церамидов обычно мешает клеточным «бригадам по уборке», и что удаление этого липидного груза позволяет клетке эффективнее очищать дефектные митохондрии и белковые агрегаты.
Защита функции мозга у мышей
Ключевой проверкой было, помогает ли эта стратегия в живом мозге. Исследователи лечили хорошо изученную мышиную модель, перепроизводящую мутантный человеческий альфа‑синуклеин и постепенно развивающую двигательные нарушения и проблемы с памятью. Начиная с середины жизни, некоторым мышам несколько месяцев вводили мириоцин, а другим — безвредный носитель. Мириоцин явно снижал уровни церамидов в крови и среднем мозге животных. Поведенческие тесты показали, что обработанные мыши проходили больше расстояния и лучше справлялись с простым лабиринтом, требующим пространственной рабочей памяти. Срезы мозга этих животных продемонстрировали, что больше дофамин‑продуцирующих нейронов выжило в ключевых областях, а количество фосфорилированного, склонного к агрегации альфа‑синуклеина уменьшилось. Масштабный анализ экспрессии генов среднего мозга дополнительно показал, что мириоцин подавлял воспалительные пути и восстанавливал гены, связанные с синаптической передачей и поддержанием здоровых митохондрий.
Человеческие нейроны и мини‑мозги подтверждают выводы
Чтобы приблизить результаты к пациентам, команда использовала нейроны и трёхмерные органоиды среднего мозга, выращенные из индуцированных плюрипотентных стволовых клеток, полученных от людей с болезнью Паркинсона. В нейронах, полученных от пациентов и несущих флуоресцентный датчик митофагии, лечение мириоценом усиливало сигнал, отмечающий доставку повреждённых митохондрий в перерабатывающие центры клетки, и улучшало архитектуру митохондриальной сети. В органоидах среднего мозга мириоцин сохранял дофамин‑продуцирующие клетки и снижал вредные агрегаты альфа‑синуклеина. Когда исследователи добавляли в эти мини‑мозги дополнительные церамиды, наблюдалось обратное: формировалось больше белковых сгустков и гибло больше дофаминовых нейронов, особенно в органоидах от доноров с Паркинсоном. Эти эксперименты подтверждают непосредственную разрушительную роль накопления церамидов в тканях, релевантных для человека.
Что это может значить для будущих терапий
Для неспециалистов основная мысль проста: в нескольких моделях болезни Паркинсона избыток определённого жира в мозге, по-видимому, отравляет клетки, способствуя образованию белковых агрегатов, дефектных митохондрий и хронического воспаления. Блокирование основной пути синтеза этих липидов с помощью экспериментального препарата мириоцина смягчало эти проблемы, сохраняло уязвимые нейроны и улучшало поведение мышей, а также спасало человеческие нейроны в культуре. Авторы подчёркивают, что долгосрочная безопасность и режимы дозирования у людей неизвестны, и что причины Паркинсона многочисленны и выходят за рамки роли церамидов. Тем не менее работа открывает новую стратегию: помимо поддержки падающего дофаминового сигнала, будущие терапии могут также нормализовать липидный метаболизм и клеточную «уборку», давая клеткам мозга лучший шанс сопротивляться медленному прогрессированию нейродегенерации.
Цитирование: Lee, E., Park, My., Park, M. et al. Inhibition of de novo ceramide synthesis mitigates alpha-synuclein pathology in a Parkinson’s disease mouse model. npj Parkinsons Dis. 12, 49 (2026). https://doi.org/10.1038/s41531-026-01263-5
Ключевые слова: болезнь Паркинсона, церамид, альфа‑синуклеин, митофагия, нейродегенерация