Clear Sky Science · ru
Ингибирование питтинговой коррозии нержавеющей стали с помощью NaNO3: механистические выводы о растворении сульфидов, депассивации и активном растворении
Почему маленькие пятна ржавчины важны
От мостов и небоскрёбов до автомобилей и химических заводов нержавеющую сталь выбирают за её способность сопротивляться ржавчине. Однако при определённых условиях на её поверхности могут внезапно появиться крошечные, но глубокие отверстия — питты, которые со временем вырастают в опасные трещины. В этом исследовании задаётся практический вопрос для промышленности: может ли распространённое, относительно безопасное вещество — нитрат натрия — помешать началу этих питтов и если да, то как именно? Ответ может помочь дольше сохранять безопасность критической инфраструктуры, используя доступные и менее вредные для окружающей среды добавки. 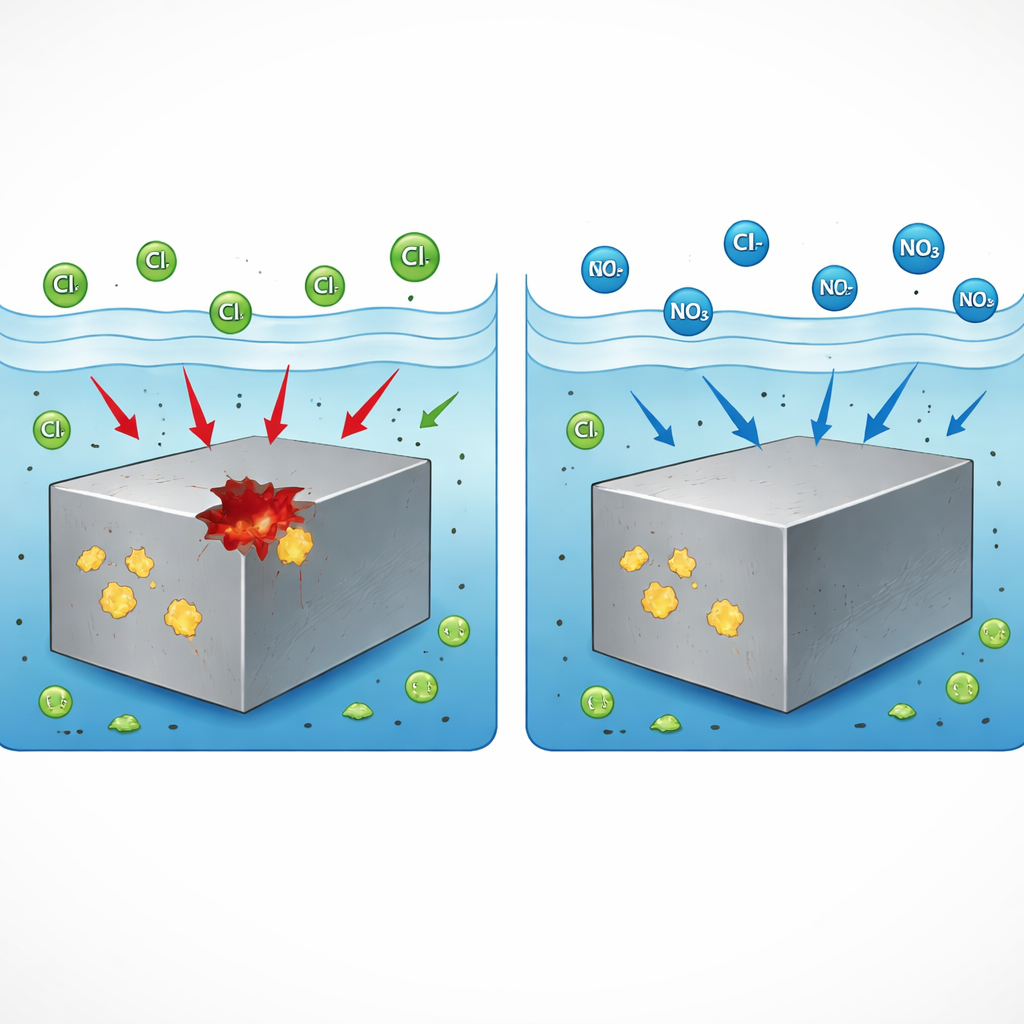
Скрытые слабые места в нержавеющей стали
Даже лучшие марки нержавеющей стали не являются полностью однородными. В материале встречаются микроскопические частицы, богатые серой, — сульфидные включения. Два важных типа основаны на марганце (MnS) и кальции (CaS). Эти включения ведут себя как встроенные слабые места, где питты предпочитают зарождаться при контакте с водой, содержащей хлориды, например с солёными брызгами или охлаждающей водой. Предыдущие работы показали, что образование питтов следует устойчивому сценарию: сульфидная частица начинает растворяться, защитная плёнка на соседней стали разрушается, и затем окружающий металл быстро растворяется, образуя питт. Настоящее исследование сравнивает две коммерческие стали типа 304 — одну с преобладанием включений MnS и другую с включениями на основе CaS — чтобы понять, может ли нитрат прервать этот сценарий у одного или обоих типов слабых мест.
Испытание распространённых добавок в солёной воде
Исследователи погружали образцы стали в простой солевой раствор и постепенно переводили металл в более коррозионно агрессивные условия, наблюдая, когда образуются устойчивые питты. Они сравнили три добавки в реалистичных концентрациях: аммоний, нитрит и нитрат, все в виде натриевых или аммониевых солей. Лишь нитрат дал заметный эффект. В сталях как с преобладанием MnS, так и с преобладанием CaS добавление умеренного количества нитрата натрия полностью предотвратило образование устойчивых питтов в исследованном диапазоне, тогда как две другие добавки не давали улучшения. Микроскопия подтвердила, что без нитрата питты действительно начинались в сульфидных включениях, тогда как при добавлении нитрата эти включения больше не вызывали повреждающих отверстий. Это показало, что нитрат является широко эффективным ингибитором питтинга для разных типов сульфидов, а не только частным случаем. 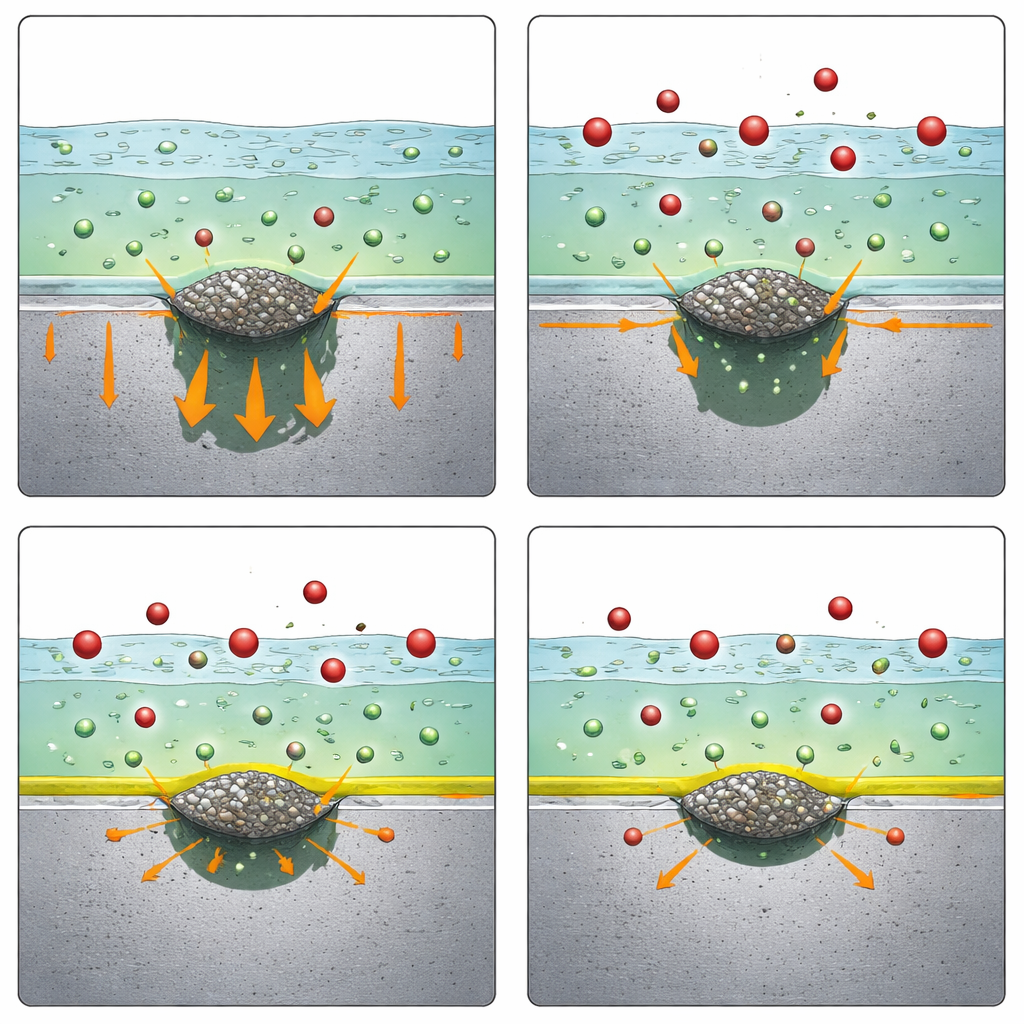
Тщательный взгляд на то, что нитрат меняет — и чего не меняет
Чтобы уточнить механизм действия нитрата, команда внимательно изучила ранние стадии формирования питта вокруг одиночных частиц MnS с помощью микроэлектродов и высокоразрешающей визуализации. Они увидели, что нитрат не препятствует самому растворению частиц MnS и не меняет мелкие бороздки, образующиеся на границе включения и окружающей стали. Нитрат также не сдвигал уровень кислотности, при котором защитная плёнка стали перестаёт работать в хлоридном растворе. Всё это указывает на то, что первые шаги инициации питта — ослабление и нарушение вокруг включения — по существу проходят в присутствии нитрата так же, как и без него.
Замедление финального резкого вымывания металла
Ключевое различие обнаружилось, когда исследователи воссоздали суровую среду внутри уже сформировавшегося питта: очень кислые, обогащённые хлоридами условия. Используя сильные кислоты, имитирующие химию глубоко внутри питтов, они обнаружили, что сталь обычно демонстрирует два отдельных всплеска быстрого растворения металла по мере повышения напряжения. Добавление нитрата последовательно уменьшало первый всплеск растворения как в чистой кислоте, так и в кислоте, содержащей серные виды, похожие на те, что выделяются при растворении MnS. Наблюдения поверхности показали равномерное поражение, но с явно меньшей скоростью. Дополнительные тесты с вариациями кислотности и концентрации хлоридов показали, что эффект нитрата не объясняется просто разбавлением кислотности, вытеснением хлоридов или стабилизацией солевых корок. Вместо этого результаты указывают на то, что нитрат способствует образованию хромсодержащего стабилизирующего поверхностного слоя в сплаве, что, в свою очередь, замедляет раннюю, самую критичную фазу активного вымывания металла.
Что это значит для реальных сталей
Проще говоря, нитрат не предотвращает первые химические «укусы» по крошечным сульфидным частицам внутри нержавеющей стали, но замедляет финальную, неконтролируемую фазу, когда безобидный дефект превращается в опасный питт. Погасив этот всплеск потери металла в кислых, солёных микроокружениях, нитрат натрия помогает стали оставаться ближе к пассивному, самозащитному состоянию, даже когда присутствуют сульфидные включения и ионы хлорида. Поскольку нитрат относительно недорог, менее токсичен по сравнению со многими альтернативами и уже применяется в промышленных оборотных водах, понимание этого механизма усиливает аргументы в пользу его целенаправленного применения как добавки для контроля коррозии с целью продления срока службы конструкций и оборудования из нержавеющей стали.
Цитирование: Amatsuka, S., Nishimoto, M. & Muto, I. Pitting-corrosion inhibition in stainless steel by NaNO3: mechanistic insights on sulfide dissolution, depassivation, and active dissolution. npj Mater Degrad 10, 40 (2026). https://doi.org/10.1038/s41529-026-00753-4
Ключевые слова: коррозия нержавеющей стали, ингибирование питтинга, нитрат натрия, сульфидные включения, хлоридные растворы