Clear Sky Science · ru
Влияние электрохимических методов обработки воды на коррозию углеродистой стали в городской системе водоснабжения
Почему важны трубы вашего крана
Электрохимические системы обработки воды становятся всё более распространёнными в городах, поскольку они эффективно удаляют загрязнения, смягчают воду и уничтожают микробов. Но те же электрические реакции, которые очищают воду, могут тихо разъедать металлические трубы, по которым вода поступает в наши дома. В этом исследовании рассматривается, как такая обработка влияет на углеродистую сталь — распространённый материал труб — и объясняется, почему коррозия может резко ускоряться при взаимодействии электрики и обычной химии водопроводной воды.
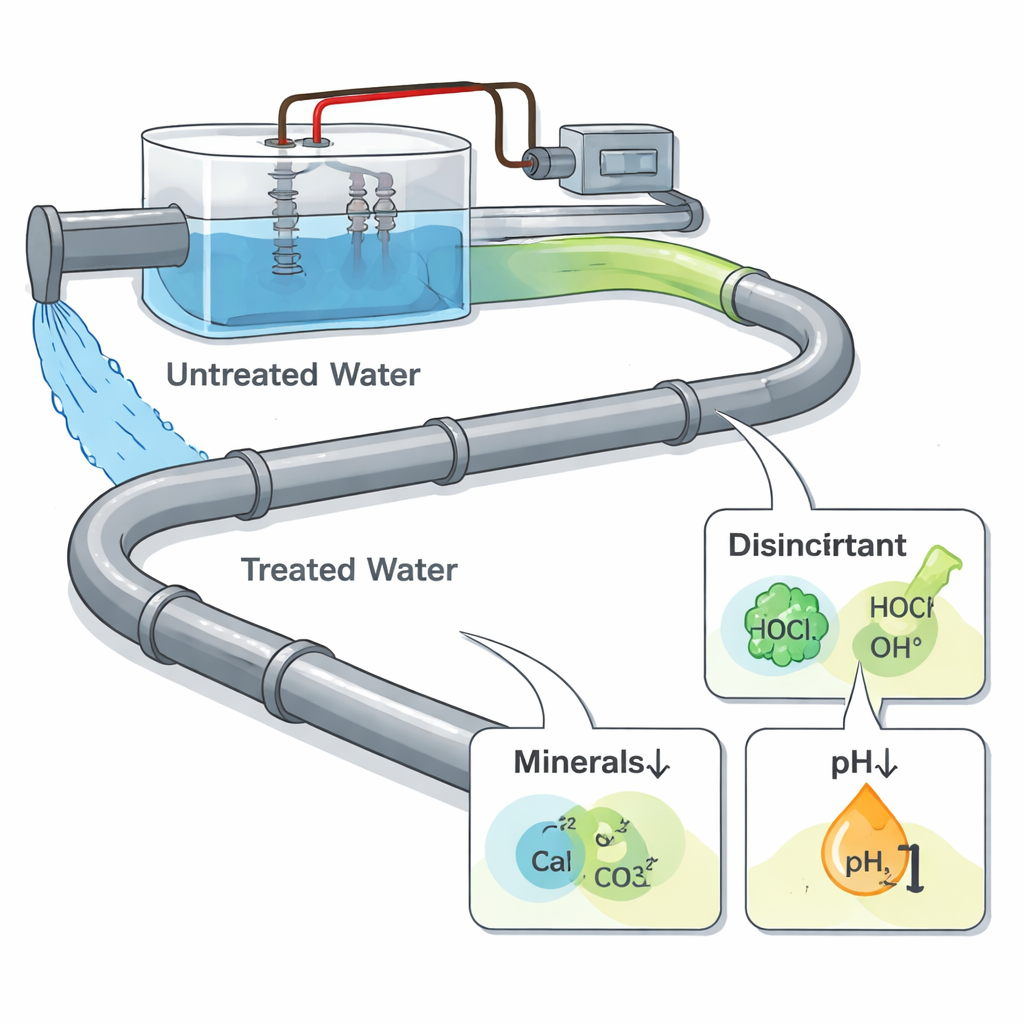
Очистка воды с помощью электричества
Электрохимическая обработка воды пропускает электрический ток через воду с использованием металлических пластин — электродов. Это позволяет удалять нежелательные ионы, разрушать органические загрязнения и генерировать дезинфицирующие вещества, что делает метод привлекательным для городских и промышленных систем. В отличие от традиционной очистки, сами трубы обычно не подключены к электричеству — они лишь получают обработанную воду, выходящую из установки. Это значит, что дополнительная коррозия вызывается не прямым воздействием тока на трубу, а изменениями в химии воды: появлением новых окисляющих веществ для дезинфекции, сдвигами кислотности и перемещением минеральных ионов, которые обычно помогают формировать защитные слои внутри труб.
Ускоренная потеря металла и более глубокие скрытые повреждения
Исследователи провели 90‑дневный эксперимент с реальной городской водой, подвергая образцы углеродистой стали разным напряжениям от 0 до 9 вольт и отслеживая потерю веса, повреждения поверхности и электрохимическое поведение. Они обнаружили, что уже в первые три дня включение электролиза увеличивало коррозию, а более высокое напряжение неизменно означало больше повреждений. При 9 вольтах скорость общей коррозии возросла более чем в 25 раз по сравнению с водой, не прошедшей электрическую обработку. С помощью 3D‑сканирования поверхности также показали, что мелкие ямки в металле становились значительно глубже с ростом напряжения. При наивысшем напряжении глубина крупнейших ямок была почти в пять раз больше, чем в необработанной воде, что резко сокращало ожидаемый срок службы стали, даже если средняя потеря металла не казалась экстремальной.
Почему защитные слои не выдерживают
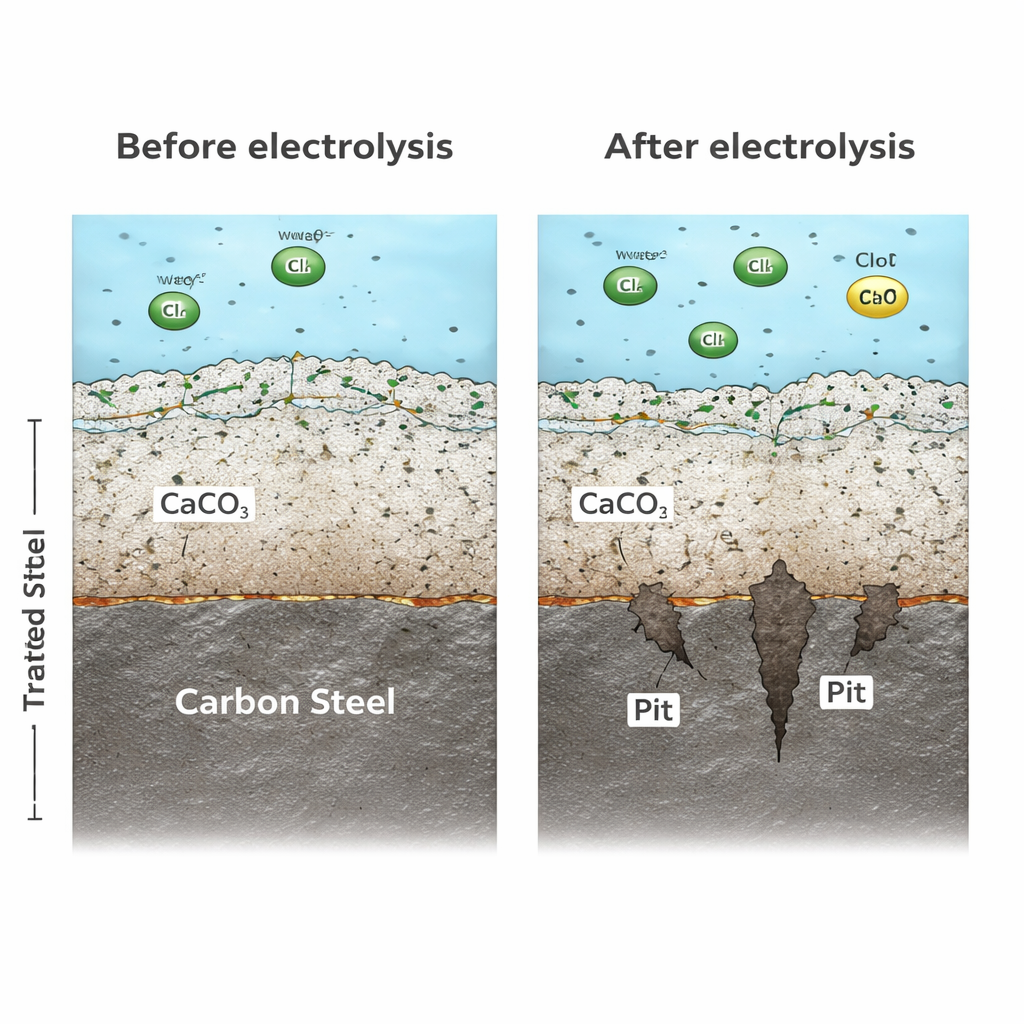
Внутри многих водопроводных труб минералы из воды естественным образом наращивают тонкий плотный слой, который помогает защищать металл. В необработанной воде эту роль обычно выполняет карбонат кальция. В электрохимически обработанной воде эта минеральная защита в значительной степени исчезала. Поскольку катод в установке для обработки привлекает ионы кальция и карбоната и поощряет их отложение на себе, меньше этих ионов остаётся для формирования прочного покрытия на стенках труб. Микроскопия и дифракционные тесты показали, что вместо плотного обогащённого минералами барьера сталь в обработанной воде покрывалась рыхлым пористым ржавым слоем с мелкими, нестабильными кристаллами. Такое слабое покрытие позволяло коррозионным веществам и электронам легко проникать, поэтому коррозия оставалась быстрой вместо того, чтобы замедляться со временем.
Усиленная химическая атака в воде
Чтобы выяснить, что именно усиливает коррозию, команда выделила различные факторы. Когда они проводили электролиз в сульфатном растворе без хлорида, побочные продукты расщепления воды — такие как кислород, водород и краткоживущие радикалы — едва меняли коррозионное поведение стали. Но при наличии хлорида, того же иона, что входит в состав обычной соли и встречается во многих водопроводных водах, картина менялась. При электролизе часть хлорида превращалась в гипохлорит, более реактивный дезинфектант. Электрохимические испытания показали, что по мере увеличения тока сталь становилась гораздо более подверженной коррозии в хлоридных растворах. Компьютерные моделирования подтвердили это: гипохлорит снижал энергетический барьер для выхода атомов железа с поверхности металла, что облегчало протекание коррозии по сравнению с одним только хлоридом. Одновременно быстрое образование продуктов ржавления потребляло гидроксид‑ионы, сдвигая воду в сторону более низкого pH, то есть более кислой среды, что дополнительно способствовало коррозии.
Что это значит для водных систем
Для неспециалистов вывод таков: очистка и дезинфекция воды с помощью электричества не обязательно безвредна для труб, по которым течёт эта вода. В системах, где вода содержит хлорид, электрохимическая обработка может превращать часть этого хлорида в более сильный, более агрессивный дезинфектант и одновременно удалять минеральные компоненты, необходимые для формирования естественной защиты. В результате металл тонет быстрее, образуются более глубокие ямки, что может сократить срок службы труб и повысить риск утечек или загрязнений. Авторы предлагают, чтобы проектировщики и операторы таких систем рассматривали коррозию как центральную проблему проектирования — ограничивая напряжение, снижая содержание хлора до обработки, выбирая электроды, формирующие меньше агрессивных побочных продуктов, и мониторя питтинговую коррозию и химический состав воды в долгосрочной перспективе — чтобы более чистая вода не стоила разрушенной инфраструктуры.
Цитирование: Zhao, S., Jing, Y., He, X. et al. Effect of electrochemical water treatment processes on carbon steel corrosion in urban water supply system. npj Mater Degrad 10, 23 (2026). https://doi.org/10.1038/s41529-026-00736-5
Ключевые слова: электрохимическая обработка воды, коррозия углеродистой стали, городские водопроводы, хлорид и гипохлорит, долговечность водной инфраструктуры