Clear Sky Science · ru
Система тетраэдра 4A: синергетическая рамочная модель для панваскулярного вмешательства, усиленного гибкой электроникой
Переосмысление ухода за нашими сосудами
Панваскулярные заболевания — поражение сосудов по всему телу — ныне являются ведущей причиной смертности в мире. Они могут поразить сердце, мозг, почки и конечности, часто без явных предвестников. В этой статье изложен смелый новый план борьбы с этими расстройствами с помощью ультратонкой, гибкой электроники и искусственного интеллекта. Вместо того чтобы рассматривать каждую процедуру как разовый случай, авторы предлагают пожизненное, основанное на данных партнерство между пациентом и устройством — от диагностики до операции и долгосрочного последующего наблюдения.
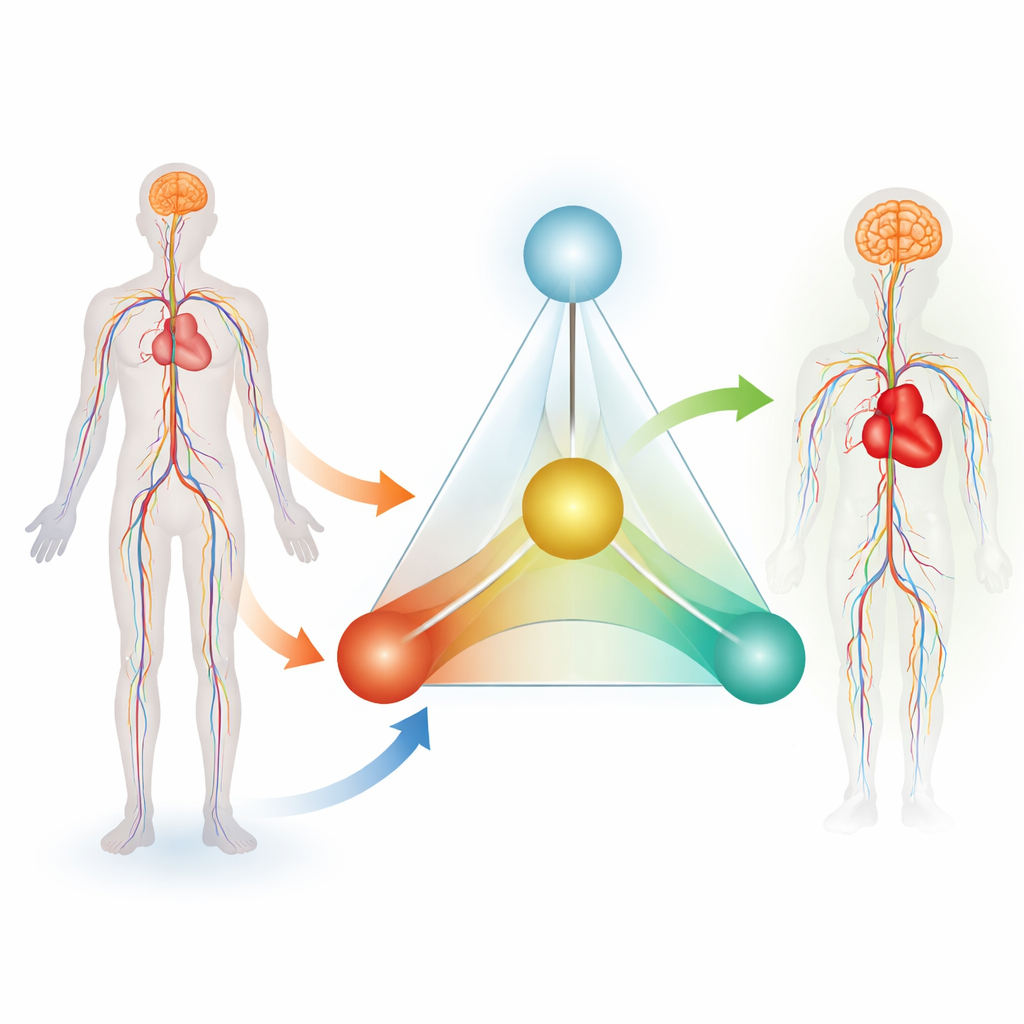
Большая идея, построенная на четырёх столпах
Авторы предлагают то, что они называют «Система тетраэдра 4A» — четырёхкомпонентную рамочную модель управления сосудистыми заболеваниями как непрерывным процессом. Четыре «А» — это Assessment (оценка), Assistance (помощь), Aftercare (послеоперационный уход) и AI‑retrofit (ИИ‑обновление). Assessment охватывает способы, которыми врачи оценивают пациента и инструменты перед процедурой. Assistance сосредоточена на безопасном проведении инструментов через извилистые артерии и вены во время операции. Aftercare касается мониторинга пациента после вмешательства, в идеале — круглосуточного. Связующим звеном этих трёх элементов является AI‑retrofit, при котором искусственный интеллект учится на всех собранных данных и возвращает выводы для улучшения будущих устройств и клинических решений. Вместе эти четыре элемента изображены как трёхгранное основание (Assessment, Assistance, Aftercare), поддерживающее вершину (ИИ), образуя тетраэдр, который символизирует замкнутый, самоусовершенствующийся цикл ухода.
Мягкие тесты и более умные имплантаты
На этапе Assessment авторы выделяют гибкие пластины с микроскопическими иглами, которые лишь слегка проникают в кожу, чтобы взять пробу межклеточной жидкости. Эта жидкость тесно отражает состав крови, но доступ к ней можно получить почти безболезненно. Встроенные сенсоры в этих крошечных иглах могут отслеживать маркеры воспаления, функцию почек, уровень сахара и другие показатели, по сути перенося часть лаборатории на пластырь, носимый на коже. Одновременно в обзоре описывается, как традиционные имплантаты — такие как стенты, искусственные клапаны и заглушки дефектов сердца — можно модернизировать с помощью ультратонких датчиков давления, химического состава и деформации. Эти «умные» устройства не только открывали бы закупоренные сосуды; они бы непрерывно измеряли механические силы, поведение клеток и химическую среду в месте имплантации, показывая, действительно ли сосуд заживает или тихо склоняется к осложнениям.
Ведение инструментов извне внутрь
Этап Assistance решает распространённую проблему современных вмешательств: навигацию проводников и катетеров через сложную сеть сосудов при минимизации облучения рентгеном и использования контрастных веществ. Авторы указывают на появляющиеся гибкие ультразвуковые пластины и фотоакустические зонды, которые могут давать снимки сосудов в реальном времени без радиации. Они также описывают магнитно управляемые мягкие проводники и микрокатетеры, кончики которых можно отклонять внешними магнитными полями и приводить в движение роботизированными манипуляторами. В паре с гибкими сенсорами и умной визуализацией эти системы нацелены на то, чтобы протаскивать устройства через волосковидные или резко изгибающиеся сосуды с субмиллиметровой точностью, снижая риски разрывов сосудов, инсультов или неудачных процедур.
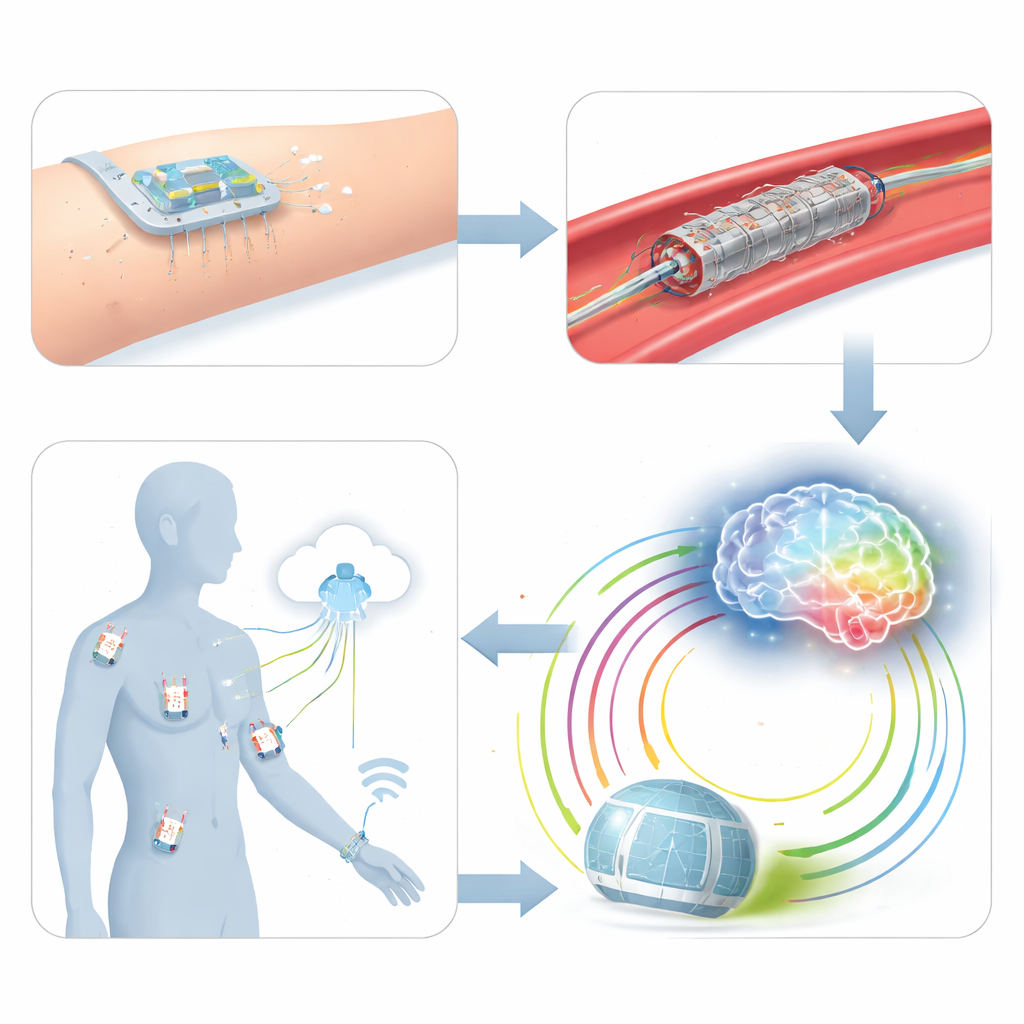
Жизнь с сетью молчаливых стражей
После процедуры многие пациенты сегодня возвращаются к разрозненным визитам в клинику и кратким осмотрам, которые легко пропускают бессимптомную рестенозу или образование тромбов. На этапе Aftercare авторы предсказывают «Интернет медицинских вещей»: сеть носимых, полупогружённых и полностью имплантируемых гибких сенсоров, расположенных по органам и на разных глубинах тканей. Пластыри на коже могут отслеживать ритм сердца и дыхание, микроскопические иглы — уровень глюкозы и маркеры воспаления, а имплантированные сенсоры на стентах или артериях — локальное давление и поток. Всё это будет через беспроводную передачу отправлять данные в облачные системы, создавая «беспроводную медицинскую сенсорную сеть», которая держит врачей виртуально у постели больного и фиксирует, как болезнь развивается по всему телу, а не только в одном пролеченном участке.
Позволяя алгоритмам замкнуть цикл
На вершине тетраэдра находится AI‑retrofit, где алгоритмы превращают сырые потоки данных от сенсоров в улучшенный уход. Модели машинного обучения могут помочь проектировать более надёжные микрошприцы и умные стенты, распознавать рискованные паттерны в химических и давленческих данных до появления симптомов и направлять хирургических роботов по более безопасным траекториям. Глубокое обучение с подкреплением — программное обеспечение, которое учится методом проб и ошибок на исторических данных — могло бы предлагать, как корректировать лекарства или когда повторно вмешиваться для каждого конкретного пациента. Крупные языковые модели однажды смогут связывать показания сенсоров, снимки и медицинские записи в понятные сводки для клиницистов и доступные объяснения для пациентов. В этой картине каждая процедура возвращает информацию в систему, оттачивая будущие решения.
От концепта к повседневной практике
Для неспециалиста основная мысль такова: уход за сосудистыми заболеваниями может сместиться от изолированных реактивных вмешательств к интеллектуальному непрерывному партнерству между организмом, гибкой электроникой и ИИ. Пластыри с микрошприцами делают тестирование мягче, умные имплантаты присматривают за уязвимыми участками изнутри, носимые и имплантируемые датчики отслеживают состояние всего тела, а обучающиеся алгоритмы связывают данные воедино в течение месяцев и лет. Остаётся множество препятствий — от долгосрочной безопасности и энергоснабжения до защиты данных и регулирования — но авторы утверждают, что в следующем десятилетии подход Системы тетраэдра 4A может превратить сегодняшние одноразовые сосудистые процедуры в развивающуюся, персонализированную систему защиты от группы заболеваний, отнимающих больше всего жизней в мире.
Цитирование: You, L., Qu, Y., Chen, Y. et al. 4A tetrahedron system: a synergistic framework for panvascular intervention empowered by flexible electronics. npj Flex Electron 10, 35 (2026). https://doi.org/10.1038/s41528-026-00537-5
Ключевые слова: гибкая электроника, заболевания сосудов, умные имплантаты, носимые датчики, медицинский ИИ