Clear Sky Science · ru
Гибкие фероэлектрические биоматериалы для регенерации кожи, нервной и опорно-двигательной тканей
Умные материалы, которые помогают организму заживать самостоятельно
Когда мы ломаем кость, рвём сухожилие, повреждаем нерв или сталкиваемся с упорной кожной раной, врачи часто могут стабилизировать повреждение — но заставить организм полностью восстановить здоровую ткань по‑прежнему трудно. В этой статье рассматривают новый класс «умных» материалов, которые гибко сочетаются с телом и превращают повседневные движения в крошечные электрические сигналы. Эти сигналы имитируют собственный биоэлектрический язык организма и мягко подталкивают клетки к росту, реорганизации и восстановлению повреждённой кожи, нервов, мышц, хряща и кости.
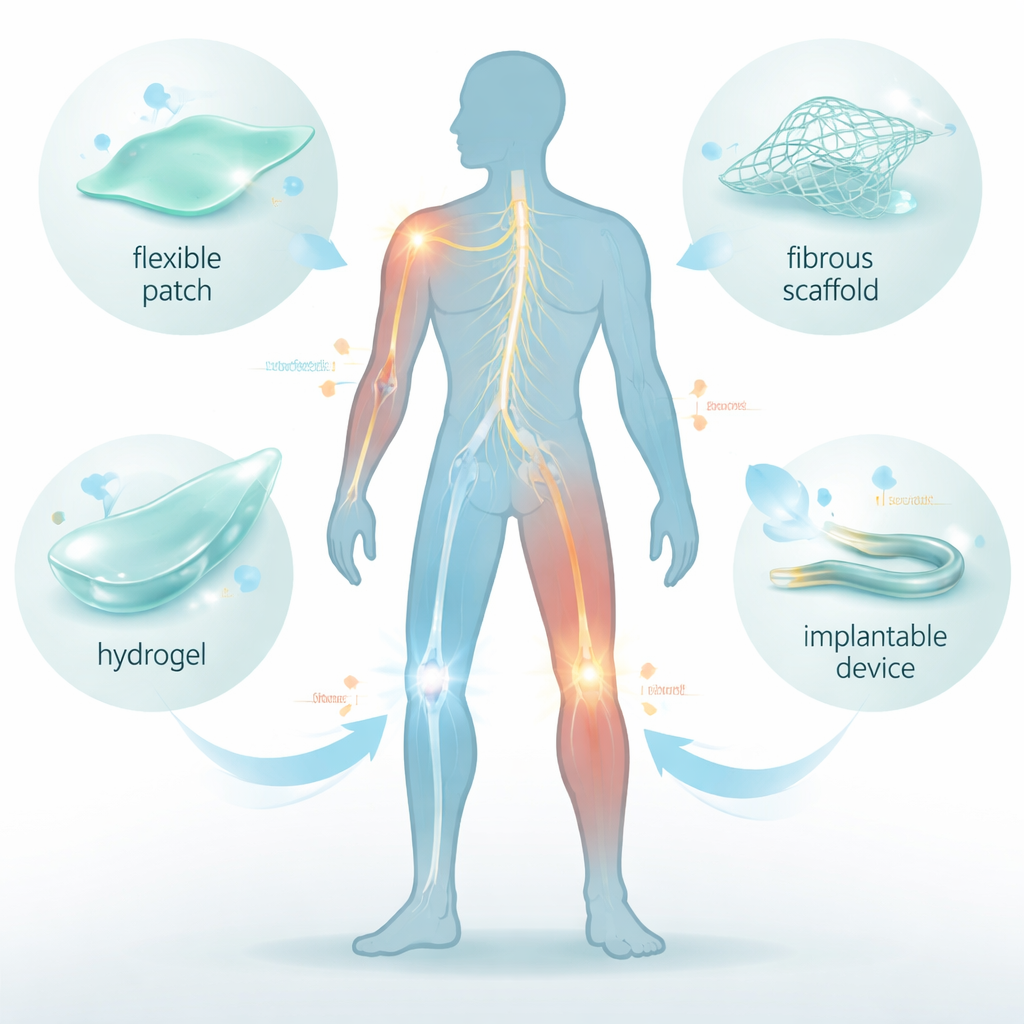
Почему электричество важно для заживления
Каждая живая ткань несёт тонкие электрические паттерны. Нервы генерируют импульсы напряжения, кости создают небольшие заряды при ходьбе, а вокруг ран в коже формируются естественные электрические поля. Эти сигналы направляют клетки — говоря им, когда перемещаться, делиться и специализироваться. Травма или хроническое воспаление могут исказить эту электрическую «карту», замедляя или неверно направляя восстановление. Обзор объясняет, как гибкие фероэлектрические биоматериалы проектируют для восстановления или усиления этих сигналов. Они реагируют на сгибание, растяжение или изменение температуры, генерируя крошечные локальные напряжения и, по сути, переводя механическое движение в собственные электрические «подсказки» организма для заживления.
Из чего состоят эти умные материалы
Авторы сосредотачиваются на нескольких классах фероэлектрических материалов, которые можно сделать мягкими и совместимыми с телом. Полимеры, такие как PVDF, его кополимер P(VDF‑TrFE) и PLLA, — это пластики, которые при правильной обработке ведут себя как мини‑генераторы: при движении они создают заряд. Керамические частицы, такие как титанат бария (BaTiO₃), феррит висмута (BiFeO₃) и ниобат калия‑натрия (KNN), дают сильный электрический отклик, но сами по себе хрупки, поэтому их вводят в гибкие полимеры. Настраивая кристаллическую структуру, выравнивание волокон и пористость, исследователи могут получать тонкие плёнки, нанофибровые сети, 3D‑печатаемые каркасы и инъецируемые гидрогели, которые повторяют формы тела и при этом вырабатывают уровни электрической стимуляции, значимые для биологии.
Как сигналы от движения «общаются» с клетками
Когда эти материалы сжимаются, растягиваются или возбуждаются ультразвуком, они посылают крошечные электрические импульсы в близлежащие клетки. В мембране клетки имеются ионные каналы, которые открываются в ответ на электрические или механические сигналы, позволяя ионам кальция проникать внутрь. Этот кратковременный всплеск кальция действует как главный переключатель, включая сети, контролирующие выживание клеток, миграцию, рост и специализацию в кости, хрящ, нерв или мышцу. Электрические сигналы также перестраивают поверхностные рецепторы, влияют на адгезию клеток к окружению, изменяют энергетический обмен в митохондриях и даже направляют иммунные клетки от затяжного воспаления к поведению, способствующему заживлению. Таким образом, простой механический шаг — например, ходьба после операции — через эти материалы может превратиться в значимые биологические инструкции.
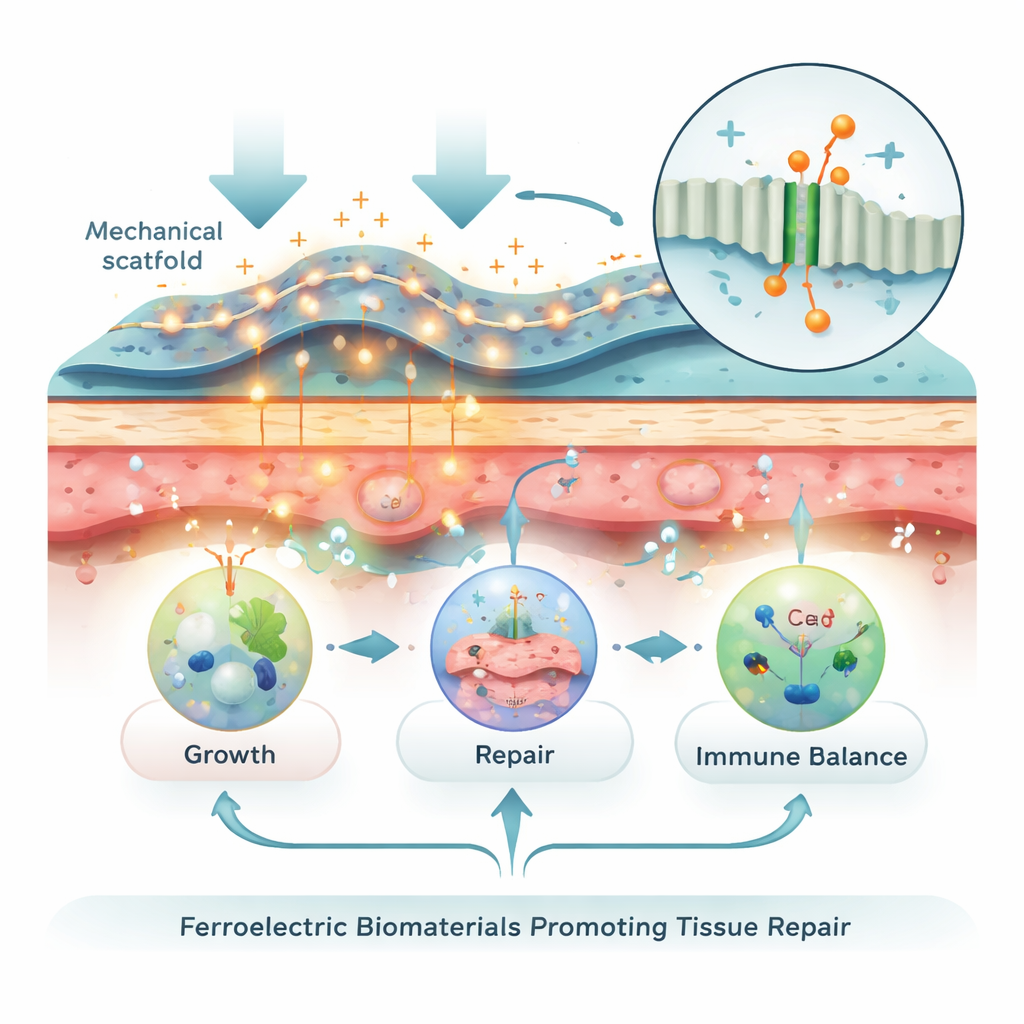
Реальные применения для кости, нервов, кожи и прочего
Обзор охватывает быстрый прогресс во многих тканях. В кости и хряще фероэлектрические каркасы и гидрогели, помещённые в дефекты, при обычной подвижности суставов или при целенаправленном ультразвуке генерируют небольшие напряжения, усиливающие экспрессию генов, ответственных за формирование кости, и способствующие качественному восстановлению хряща. В периферических нервах гибкие направляющие из пьезоэлектрических волокон направляют отрастающие аксоны и при активации движением или звуковыми волнами обеспечивают мягкую непрерывную стимуляцию, сравнимую по эффекту с нервными трансплантатами. Для кожи автономные повязки и 3D‑напечатанные пластыри усиливают собственные токи раны, ускоряя закрытие, рост кровеносных сосудов, контроль инфекции и даже снижая образование рубцов. Подобные подходы помогают выравниванию и созреванию мышечных волокон и улучшают прикрепление сухожилия к кости после травм ротаторной манжеты или связок.
От лабораторных обещаний к повседневной терапии
Несмотря на воодушевление, авторы подчёркивают, что большинство этих технологий ещё находятся на ранних стадиях — в экспериментах на животных или лабораторных исследованиях. Надёжное масштабное производство таких сложных многослойных материалов, их выживаемость после стерилизации и в долгосрочном пребывании в теле, а также согласование скорости их разложения с темпом заживления тканей остаются открытыми задачами. Некоторые широко используемые полимеры, например PVDF, почти не разлагаются в организме, что ставит вопросы о их долгосрочной судьбе. В будущем потребуются более совершенные системы управления — возможно, с применением ИИ — для регулирования стимуляции в реальном времени, а также новые фероэлектрические материалы, которые были бы одновременно эффективны и действительно биоразлагаемы. Если эти препятствия удастся преодолеть, гибкие фероэлектрические биоматериалы могут привести к созданию имплантатов, перевязок и мягких электронных «кож», которые тихо используют наши движения для точного и персонализированного восстановления кожи, нервов, мышц и всей опорно‑двигательной системы.
Цитирование: Sheng, N., Wang, Y., Luo, X. et al. Flexible ferroelectric biomaterials for skin, neural, and musculoskeletal tissue repair. npj Flex Electron 10, 29 (2026). https://doi.org/10.1038/s41528-026-00532-w
Ключевые слова: гибкие биоматериалы, электростимуляция, регенерация тканей, пьезоэлектрические полимеры, заживление ран