Clear Sky Science · ru
Умный фотокапацитивный гибкий биоинтерфейс на основе квантовых точек Cu2SnS3 для ретиноподобной фотоэлектрической стимуляции
Новые подходы к восстановлению ухудшающегося зрения
Миллионы людей теряют зрение, когда светочувствительные клетки глаза постепенно погибают — состояние, известное как дегенерация сетчатки. Когда эти клетки исчезают, глаз уже не способен преобразовывать свет в электрические сигналы, которые мозг использует для построения изображений. В этом исследовании изучается новый вид ультратонкой гибкой пленки, которую можно разместить там, где раньше работали поврежденные клетки, и которая превращает мягкие вспышки света в безопасные электрические сигналы для нервных клеток — предлагая потенциальный путь к будущим «питаемым от солнца» зрительным имплантатам.
Создание крошечного искусственного фрагмента сетчатки
Вместо громоздкой электроники и проводов исследователи создали многослойную структуру светочувствительных материалов толщиной всего в несколько микрометров. В ее основе — квантовые точки сульфида меди‑олова (Cu2SnS3) — нанокристаллы размером меньше десяти миллиардных долей метра — в сочетании с мягкой пластиковой смесью, часто используемой в органических солнечных элементах. Этот гибридный слой лежит на прозрачной гибкой подложке и погружен в солевой раствор, похожий на жидкость внутри и вокруг мозга. Когда на пленку попадает свет, она ведет себя одновременно как миниатюрный солнечный элемент и как крошечный конденсатор: превращает свет в электрический заряд и временно хранит этот заряд на своей поверхности, именно там, где его могут ощущать нервные клетки. 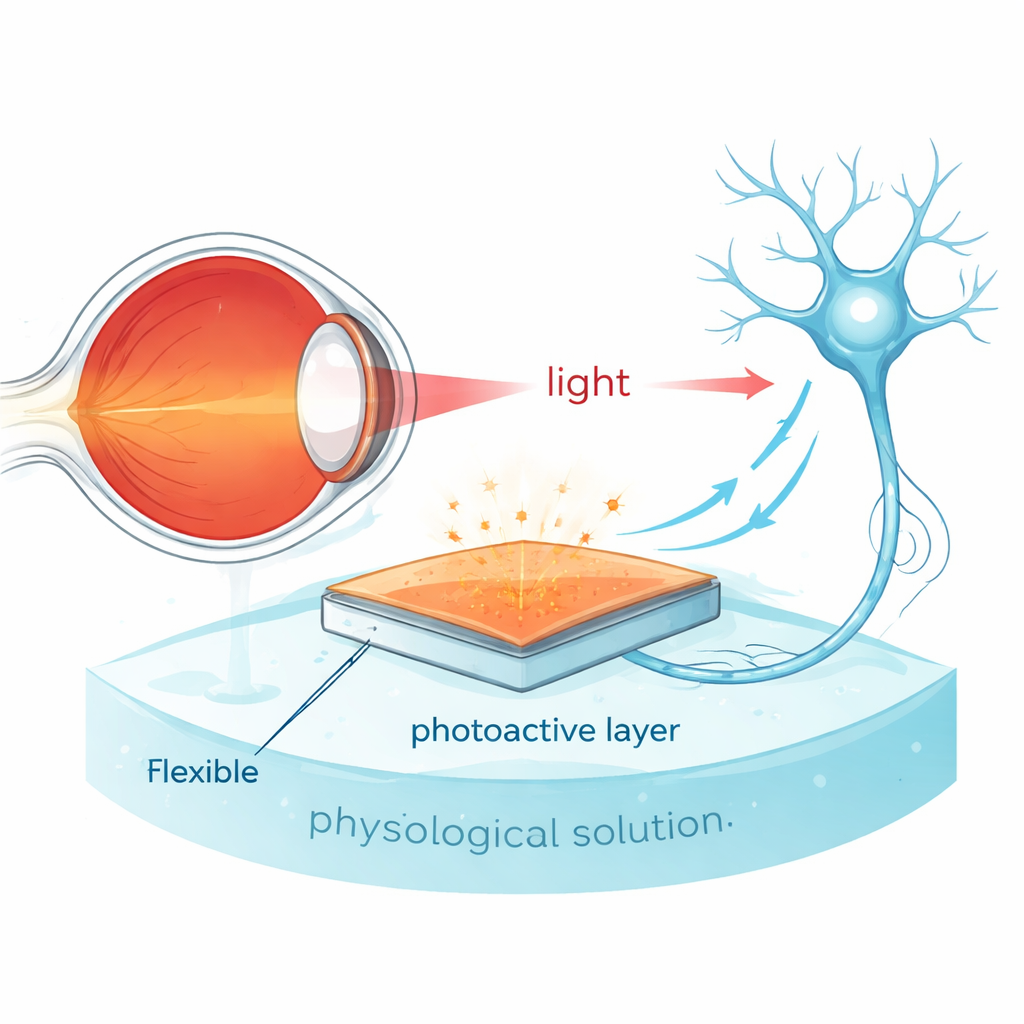
Интеллектуальная реакция на цвета света
Команда сначала точно настроила квантовые точки так, чтобы они эффективно поглощали видимый и ближний инфракрасный свет, с выраженным смещением в сторону красного света — похожим на то, как некоторые клетки сетчатки более чувствительны к более длинным длинам волн. Затем они измерили, как емкостные свойства пленки меняются при освещении разными цветами. Красный свет вызывал повышение емкости примерно в семь раз по сравнению с темнотой, тогда как синий свет практически не влиял на нее. При этом электрическое сопротивление пленки падало под воздействием света, что подтверждает высвобождение зарядов, которые перемещаются к поверхности и участвуют в обратимых реакциях с окружающей жидкостью. Это зависящее от длины волны, саморегулируемое поведение перекликается с тем, как биологические фоторецепторы изменяют мембранный потенциал при изменениях интенсивности и цвета света.
От световых импульсов к электрическим «подталкиваниям»
Далее исследователи проверили, можно ли использовать эти светогенерируемые заряды без жесткой проводки, как это потребовал бы будущий имплантат. Они разместили гибкую пленку в искусственной церебральной жидкости и опустили микроэлектрод для записи в раствор над ней. Короткие вспышки красного света вызывали резкие всплески тока — достигая пиков примерно 4,5 миллиардных долей ампера при умеренных уровнях света — состоящие в основном из быстрых емкостных импульсов, а не медленных химически обусловленных токов. Заряд, доставляемый за импульс, превышал то, что обычно требуется для воздействия на нервные ткани, при этом оставался безопасно ниже порогов, связанных с повреждением или нагревом. Компьютерные модели, трактующие мембрану нервной клетки как маленькую электрическую цепь, показали, что такие импульсы могут кратковременно сдвигать потенциал клетки на десятки милливольт — достаточно, чтобы вызвать возбуждение, сохраняясь в пределах биологически приемлемых значений. 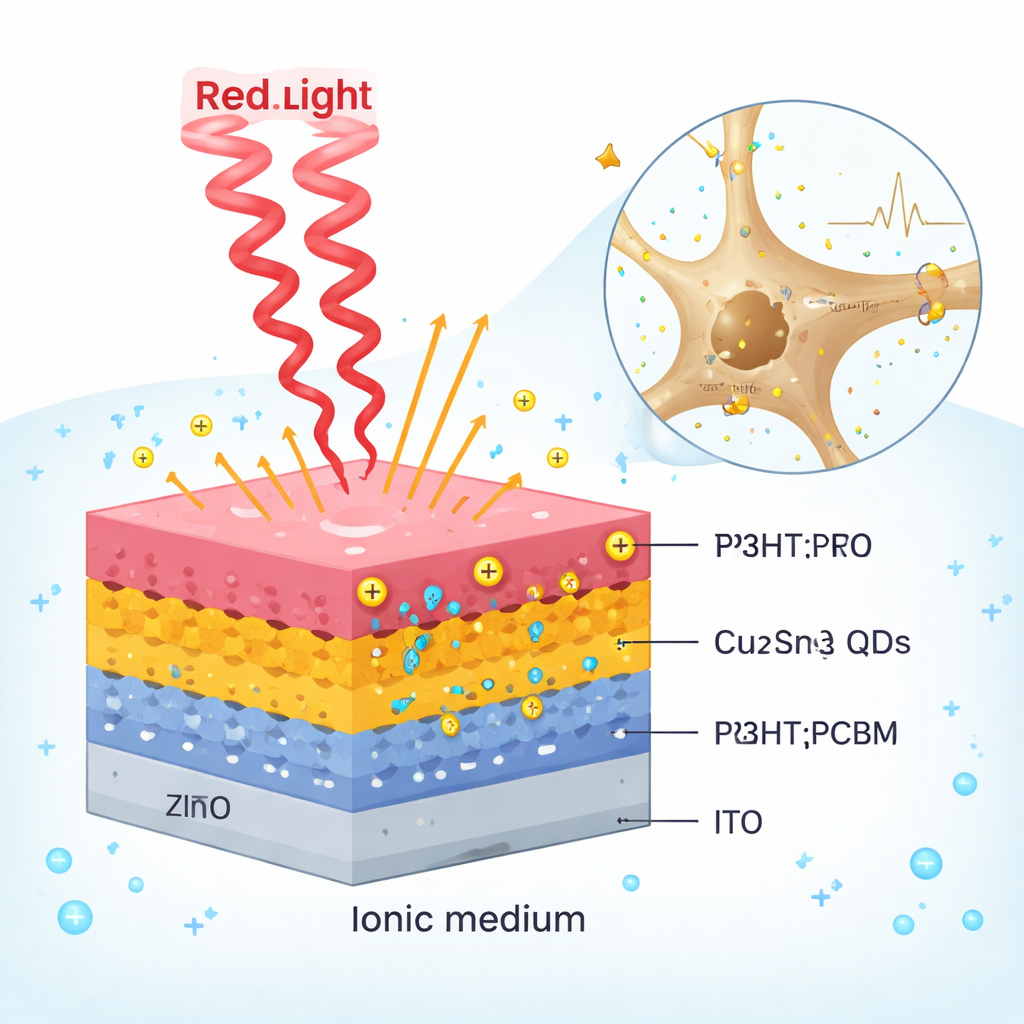
Наблюдение за зажиганием нейронов
Чтобы проверить, ответят ли настоящие нервные клетки, команда вырастила первичные гиппокампальные нейроны — клетки, участвующие в памяти и передаче сигналов — прямо на гибких пленках. С помощью стандартного лабораторного теста они подтвердили, что около 80 процентов клеток выживают, что указывает на низкую токсичность. Нейроны затем загрузили флуоресцентным красителем, который светится ярче при входе ионов кальция в клетки — маркере электрической активации. Когда исследователи применяли короткие импульсы красного или желтого света, пленки возбуждали лежащие под ними нейроны: в течение одной–двух секунд после каждого светового импульса флуоресценция во многих клетках увеличивалась примерно на 10 процентов, затем медленно возвращалась к исходному уровню. Временные характеристики и форма этих сигналов показывали, что попадание света на пленку надежно переводилось в изменения внутренней химии и электрического состояния нейронов.
В направлении беспроводных средств помощи зрению будущего
Проще говоря, эта работа демонстрирует мягкую, гибкую «фото‑батарею», которая может находиться в биологической жидкости, заряжаться при помощи красного света и разряжаться, выдавая мягкие электрические импульсы для нервных клеток. Объединив концепции солнечных элементов и суперконденсаторов в одной нетоксичной пленке с квантовыми точками, исследователи создали платформу, работающую при безопасных уровнях света, генерирующую быстрые обратимые сигналы и хорошо взаимодействующую с живыми нейронами. Хотя предстоит много инженерной работы — например, повышение чувствительности, оптимизация конструкции слоев и адаптация технологии специально для ганглионарных клеток сетчатки — исследование приближает нас к беспроводным, лишенным батарей имплантатам, которые однажды могли бы помочь восстановить полезное зрение или обеспечить новые типы светозависимой терапии в мозге и за его пределами.
Цитирование: Vanalakar, S.A., Qureshi, M.H., Mohammadiaria, M. et al. Smart photocapacitive Cu2SnS3 quantum dots-based flexible biointerface for retinal-inspired photoelectrical stimulation. npj Flex Electron 10, 28 (2026). https://doi.org/10.1038/s41528-026-00531-x
Ключевые слова: ретинальный протез, фотокаpacитор, квантовые точки, невромодуляция, гибкая биоэлектроника