Clear Sky Science · ru
Транскриптомный анализ механизмов радиочувствительности AR-позитивных тройных отрицательных раков молочной железы при ингибировании AR
Почему это исследование важно для людей, сталкивающихся с раком молочной железы
Лучевая терапия является основным методом лечения при многих агрессивных формах рака молочной железы, но некоторые опухоли по своей природе хуже поддаются облучению. В этом исследовании поставлен практический вопрос с реальными клиническими последствиями: может ли класс препаратов, блокирующих мужские гормональные сигналы и уже применяющихся при раке предстательной железы, сделать подтип тройных отрицательных раков молочной железы более уязвимыми к радиации — и почему это работает в одних случаях, но не в других?
Трудно лечимая форма рака молочной железы
Тройные отрицательные раки молочной железы лишены трех распространенных молекулярных мишеней — рецепторов эстрогена, прогестерона и HER2 — поэтому пациентам часто приходится полагаться только на операцию, химиотерапию и радиацию. Однако часть этих опухолей экспрессирует андрогенный рецептор, белок, реагирующий на гормоны, подобные тестостерону, и способный стимулировать рост опухоли. Предыдущие работы показали, что блокада этого рецептора может замедлять развитие таких опухолей и усиливать эффект радиации, но было неясно, как именно это происходит и какие препараты и опухоли получают наибольшую выгоду.
Испытание современных блокаторов гормонов вместе с радиацией
Исследователи изучали несколько лабораторных моделей клеток тройного отрицательного рака молочной железы, которые в основном различались по уровню экспрессии андрогенного рецептора. Они сосредоточились на двух новых антиандрогенах — апалутамиде и даролутамиде — и комбинировали короткие воздействия этих препаратов со стандартными дозами рентгеновского излучения. В клетках с высоким уровнем андрогенного рецептора апалутамид явно усиливал радиационное повреждение, оставляя меньше клеток, способных образовать новые колонии. Даролутамид, напротив, мало или вовсе не влиял на радиочувствительность в тех же клетках, и ни один из препаратов не помогал в клетках с очень низким уровнем рецептора. Эти результаты показывают, что не все антиандрогены действуют одинаково при раке молочной железы и что для эффективности комбинации опухоли должны сильно зависеть от этого рецептора.
Наблюдение перемещения ключевого белка внутри клетки
Чтобы понять, что происходит внутри раковых клеток после гормональных сигналов или облучения, команда отслеживала локализацию самого андрогенного рецептора. При воздействии синтетического андрогена рецептор перемещался в ядро — центр управления, где включаются и выключаются гены. Само по себе облучение не выводило рецептор из ядра; на самом деле он оставался там после лечения, готовый влиять на активность генов. Однако когда клетки получали антиандроген энзалутамид перед облучением, уровни рецептора в ядре падали, и больше его оставалось в цитоплазме. Это поддерживает идею, что блокада ядерной транслокации рецептора мешает ему запускать защитную генную программу после радиации.
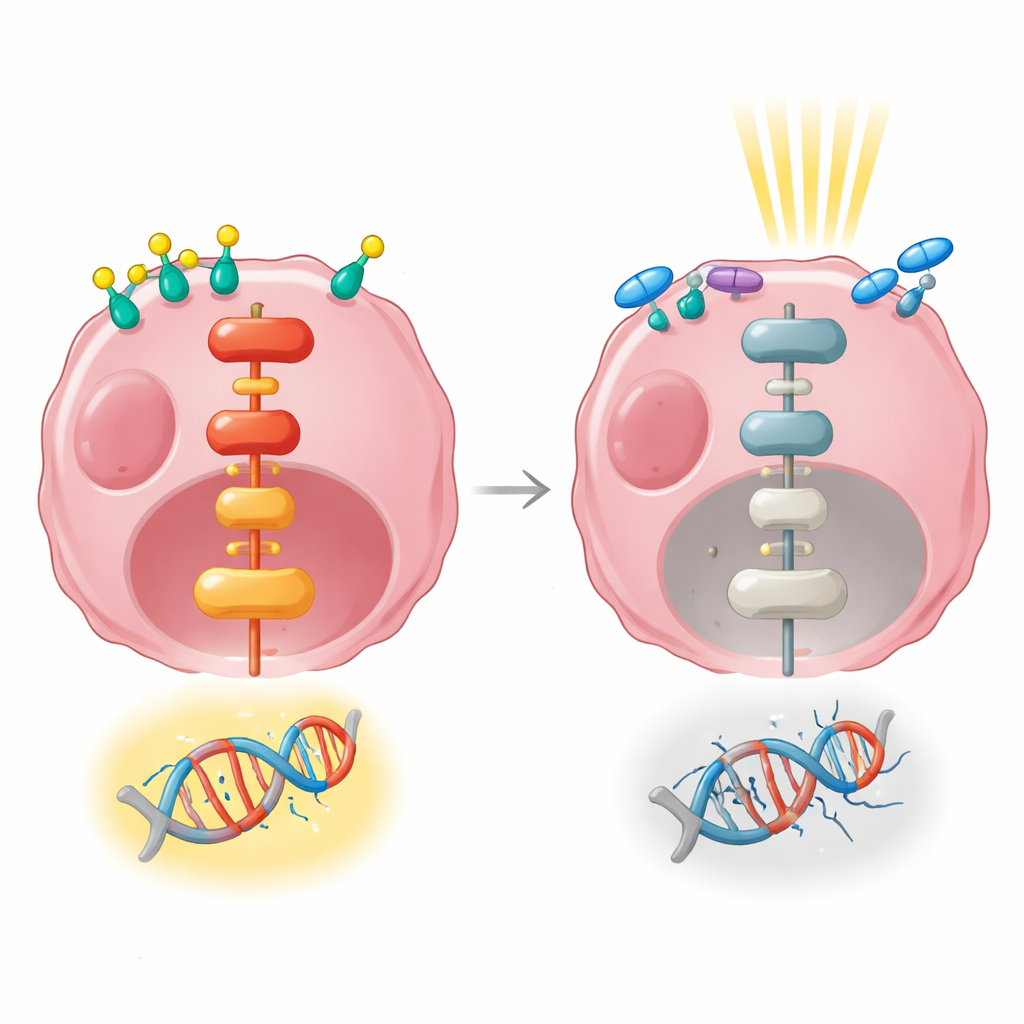
Генные сигналы, связывающие гормоны с радиорезистентностью
Затем исследователи использовали секвенирование РНК, чтобы получить широкий снимок того, какие гены активируются или подавляются после гормональной стимуляции, облучения или их сочетания. Самостоятельная гормональная обработка изменила активность сотен генов и сильно затронула пути, контролирующие рост клеток, прикрепление и взаимодействие с окружением. Облучение, примененное само по себе на раннем временном отрезке, изменяло гораздо меньше генов. Когда гормональная стимуляция и облучение сочетались, многие те же пути, связанные с ростом, активировались, включая важный сигнальный маршрут MAPK/ERK, который передает сигналы от поверхности клетки в ядро. Известно, что этот путь помогает клеткам выживать и ремонтировать повреждения ДНК.
Проверка пути выживания, защищающего ДНК
Поскольку в анализах постоянно всплывал сигнальный путь MAPK/ERK, исследователи проверили, может ли усиление этого пути отменить эффект блокады андрогенов при облучении. Они модифицировали клетки, чтобы те чрезмерно производили постоянно активную форму ERK — ключевой компонент пути, — и затем повторили комбинированное лечение облучением и апалутамидом. В таких условиях апалутамид больше не повышал чувствительность клеток к радиации: усиленный сигнал ERK, по-видимому, защищал их. Вместе с белковыми измерениями эти результаты указывают на сигнальный путь MAPK/ERK как критическую связь между активностью андрогенного рецептора и способностью клетки восстанавливать разрывы ДНК, вызванные радиацией.
Что это значит для будущего лечения рака молочной железы
Проще говоря, эта работа показывает, что некоторые тройные отрицательные раки молочной железы выживают после облучения, используя андрогенные сигналы для включения внутренней цепи выживания, которая помогает им ремонтировать поврежденную ДНК. Такие препараты, как апалутамид и энзалутамид, могут прерывать эту цепь в опухолях, сильно зависящих от андрогенного рецептора, делая радиацию более эффективной, тогда как опухоли с низким уровнем рецептора или с альтернативными путями выживания могут не получить выгоды. Карта вовлеченных генетических путей — особенно маршрута MAPK/ERK — закладывает основу для более точных комбинаций гормональных блокаторов, ингибиторов путей и радиации, которые могли бы улучшить прогноз у пациентов с этой трудно поддающейся лечению формой рака молочной железы.
Цитирование: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
Ключевые слова: тройной отрицательный рак молочной железы, андрогенный рецептор, радиотерапия, радиочувствительность, сигнальный путь MAPK ERK