Clear Sky Science · ru
Программируемая локальная иммунохимиотерапия для тройного-негативного рака молочной железы с пространственно-временным управлением высвобождения CpG олигодезоксинуклеотидов, гемцитабина и паклитаксела
Преобразование трудного типа рака молочной железы в локальную цель
Тройной-негативный рак молочной железы — одна из наиболее трудно поддающихся лечению форм, поскольку он лишён обычных молекулярных «переключателей», на которые ориентируются многие современные препараты. Пациентам часто приходится полагаться на мощную химиотерапию, воздействующую на весь организм, что вызывает серьёзные побочные эффекты и нередко не обеспечивает длительного контроля болезни. В этом исследовании рассматривается иная идея: вместо того чтобы заливать организм лекарствами, можно ли поместить крошечный программируемый депо лекарства рядом с опухолью, которое в тщательно выстроенной последовательности будет высвобождать химиопрепараты и иммуностимуляторы прямо там, где они наиболее нужны?
Маленькое депо с большими амбициями
Исследователи создали то, что они называют платформой программируемой локальной иммунохимиотерапии (PLICT). Представьте мягкую инъецируемую бусинку, которая располагается рядом с опухолью молочной железы и постепенно выделяет лечение в течение недель. Бусинка объединяет гидрофильный гель, который быстро высвобождает иммунный стимулятор и один химиопрепарат — гемцитабин, — и микроскопические полимерные шарики, которые медленно выделяют второй препарат — паклитаксел. Иммунный стимулятор, короткая цепочка ДНК CpG, призван активировать местные иммунные клетки, тогда как сочетание химиотерапевтических средств непосредственно атакует опухолевые клетки и перестраивает опухолевую среду, чтобы иммунные клетки могли проникнуть внутрь и выполнить свою работу.
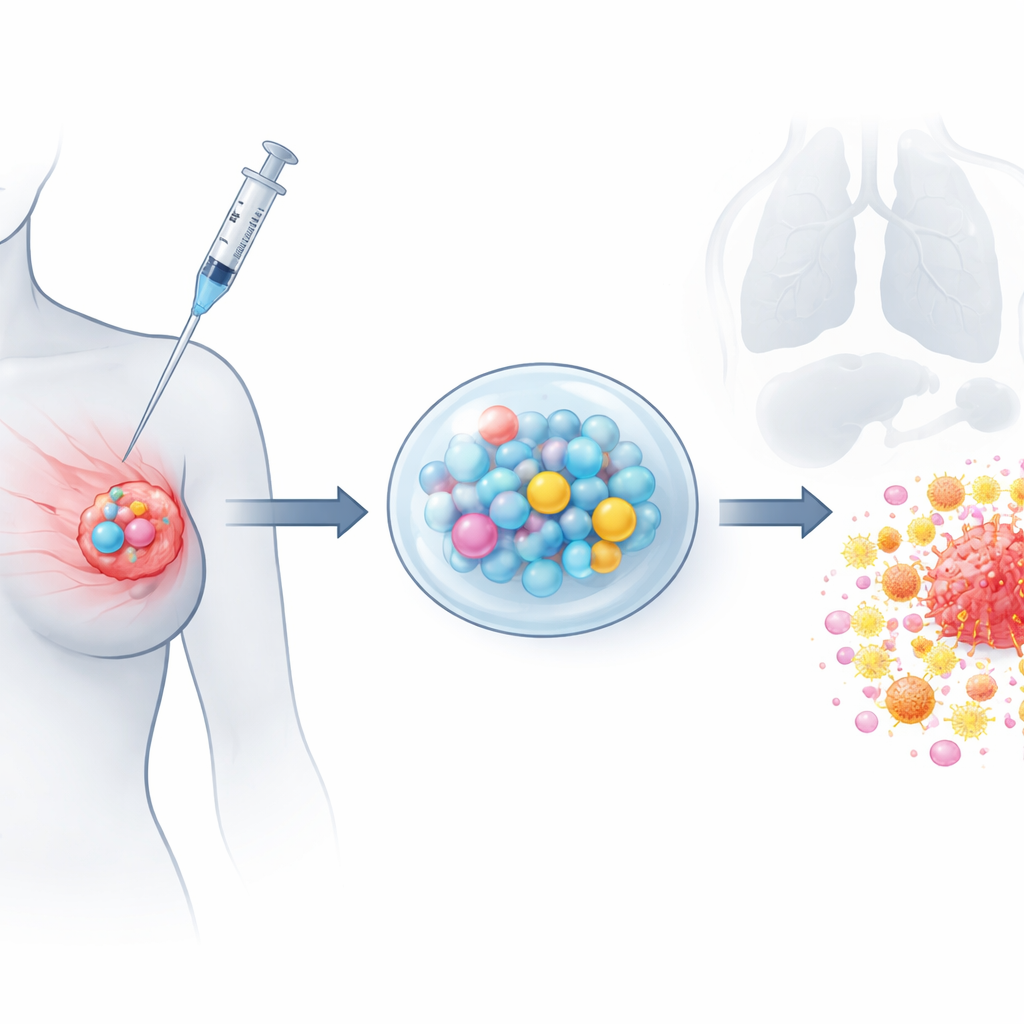
Создание отсроченной по времени атаки на рак
Для создания системы команда использовала метод «электропрыска» с высоким напряжением для формирования однородных микросфер, нагруженных паклитакселом, из биоразлагаемого полимера. Визуализация показала гладкие сферические частицы примерно одной десятой ширины человеческого волоса, а лабораторные тесты подтвердили, что паклитаксел выделяется равномерно как минимум в течение месяца без раннего резкого выброса. Отдельно гемцитабин и CpG были внедрены в термочувствительный гель, который жидкий при охлаждении и становится полутвёрдым при температуре тела. Химическое профилирование подтвердило, что оба препарата сохраняют целостность внутри своих носителей. В сочетании гель обеспечивает быстрый ранний выброс гемцитабина и CpG, а микросферы дают продолжительный подсос паклитаксела, имитируя преимущества длительной низкодозной химиотерапии после однократного локального введения.
Проверка локальной стратегии на мышах
Далее команда испытала PLICT на модели тройного-негативного рака молочной железы у мышей. У мышей сначала развивались небольшие опухоли, затем они получали либо стандартные инъекции только паклитаксела, паклитаксел в сочетании с гемцитабином, либо одно локальное имплантированное депо PLICT рядом с опухолью. В течение четырёх недель опухоли в контрольной группе быстро росли, при стандартной химиотерапии рост был замедлен, но в опухолях, леченных PLICT, размер и масса были заметно меньше. Визуализация всего животного и удалённых органов показала, что PLICT также эффективнее уменьшал метастазирование в отдалённые органы, в особенности в лёгкие, по сравнению с обычными введениями препаратов. Измерения уровней препаратов объяснили причину: паклитаксел концентрировался в опухолях после PLICT, но был низким в отдалённой жировой ткани и сопоставим в крови, что указывает на сильное локальное удержание с меньшим количеством побочных воздействий вне цели.
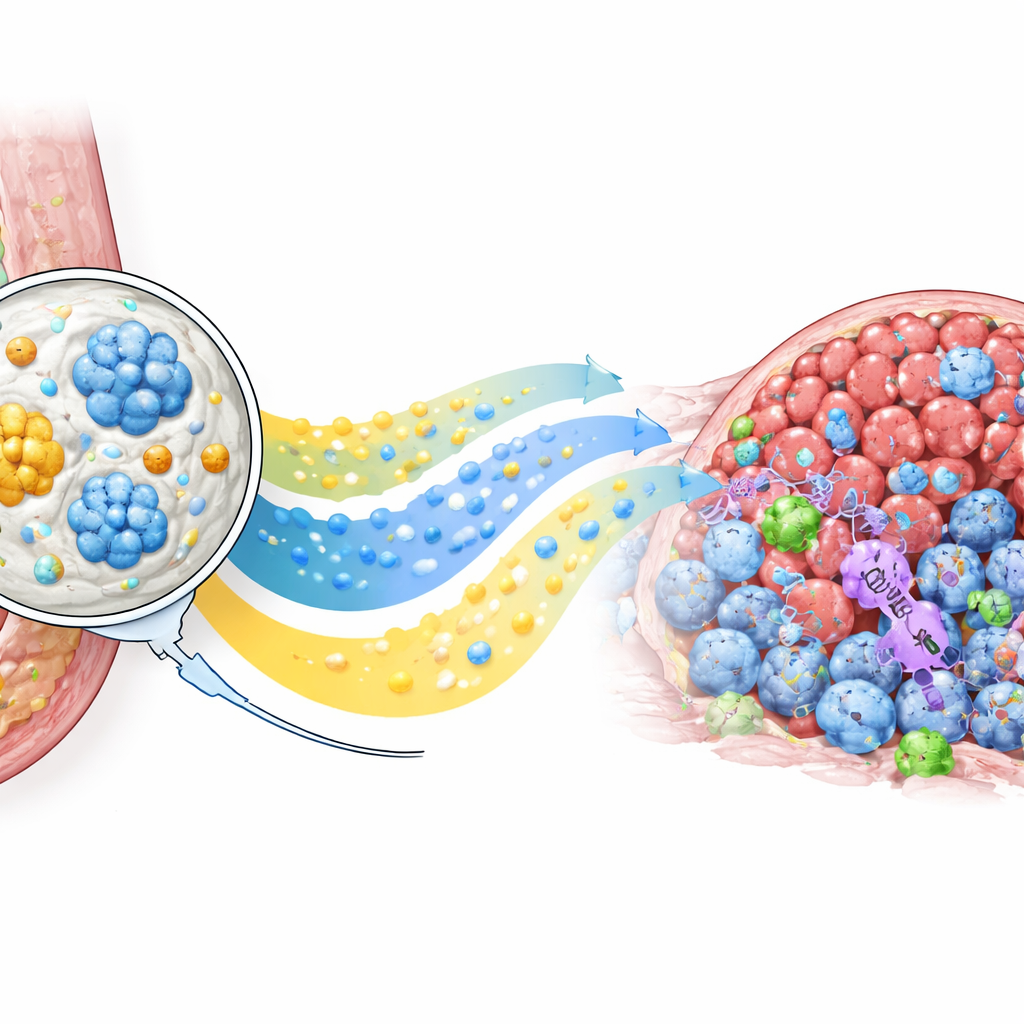
Призыв собственных защитников организма
Кроме уменьшения размеров опухолей, PLICT изменял иммунную среду внутри них. Детальный анализ клеток показал резкое увеличение цитотоксических CD8 Т-клеток в опухолях, обработанных PLICT, по сравнению со всеми другими группами, а также снижение определённых регуляторных Т-клеток, которые обычно подавляют иммунные атаки. Окраска тканей для маркера CD69, свидетельствующего о недавней активации Т-клеток, подтвердила, что многие из этих проникающих клеток были включены и готовы действовать. Одновременно стандартная химиотерапия вызывала заметные повреждения печёночной ткани, тогда как органы мышей в группе PLICT при микроскопическом исследовании выглядели почти нормально. В совокупности эти результаты указывают на то, что локальное депо не только усиливает прямое воздействие препаратов в опухоли, но и запускает более благоприятный, менее подавленный иммунный ответ, не создавая дополнительной нагрузки для жизненно важных органов.
Что это может означать для будущего лечения рака
Для неспециалистов вывод прост: превратив химиотерапию и иммунную стимуляцию в медленную, точно этапированную подачу непосредственно рядом с опухолью, этот подход в экспериментах на животных обеспечил более мощный контроль опухоли и меньше системных побочных эффектов, чем стандартные инъекции. Работа пока находится на доклинической стадии, и остаются вопросы о том, как такая система поведёт себя у людей или в иных клинических условиях. Тем не менее концепция инъецируемого, программируемого «депо лекарства», которое незаметно высвобождает несколько агентов по очереди, может открыть новые пути лечения агрессивных опухолей, таких как тройной-негативный рак молочной железы — фокусируя удар там, где это важнее всего, и щадя остальной организм.
Цитирование: Hsieh, CH., Hsu, MY., Lin, CF. et al. Programmable local immunochemotherapy for triple-negative breast cancer via spatiotemporally controlled release of CpG oligodeoxynucleotides, gemcitabine, and paclitaxel. npj Breast Cancer 12, 45 (2026). https://doi.org/10.1038/s41523-026-00910-7
Ключевые слова: тройной-негативный рак молочной железы, локальная доставка препаратов, иммунотерапия, контролируемое высвобождение, гидрогелевые микросферы