Clear Sky Science · ru
Ось CXCL10/CXCR3 необходима для поддержания иммунологической дремоты при тройном негативном раке молочной железы
Почему некоторые раки «спят», а не распространяются
Рак молочной железы иногда ведёт себя как «спящий агент». После начального лечения несколько раковых клеток могут скрываться в организме годами, не растя настолько, чтобы их было видно на сканах — но при этом оставаясь способными проснуться позже и вызвать жизнеугрожающие метастазы. В этой статье исследуют, почему такое состояние «сна», называемое дремотой, возникает при особенно агрессивной форме заболевания — тройном негативном раке молочной железы — и выявляют химический сигнал, который помогает иммунной системе держать эти клетки под контролем.
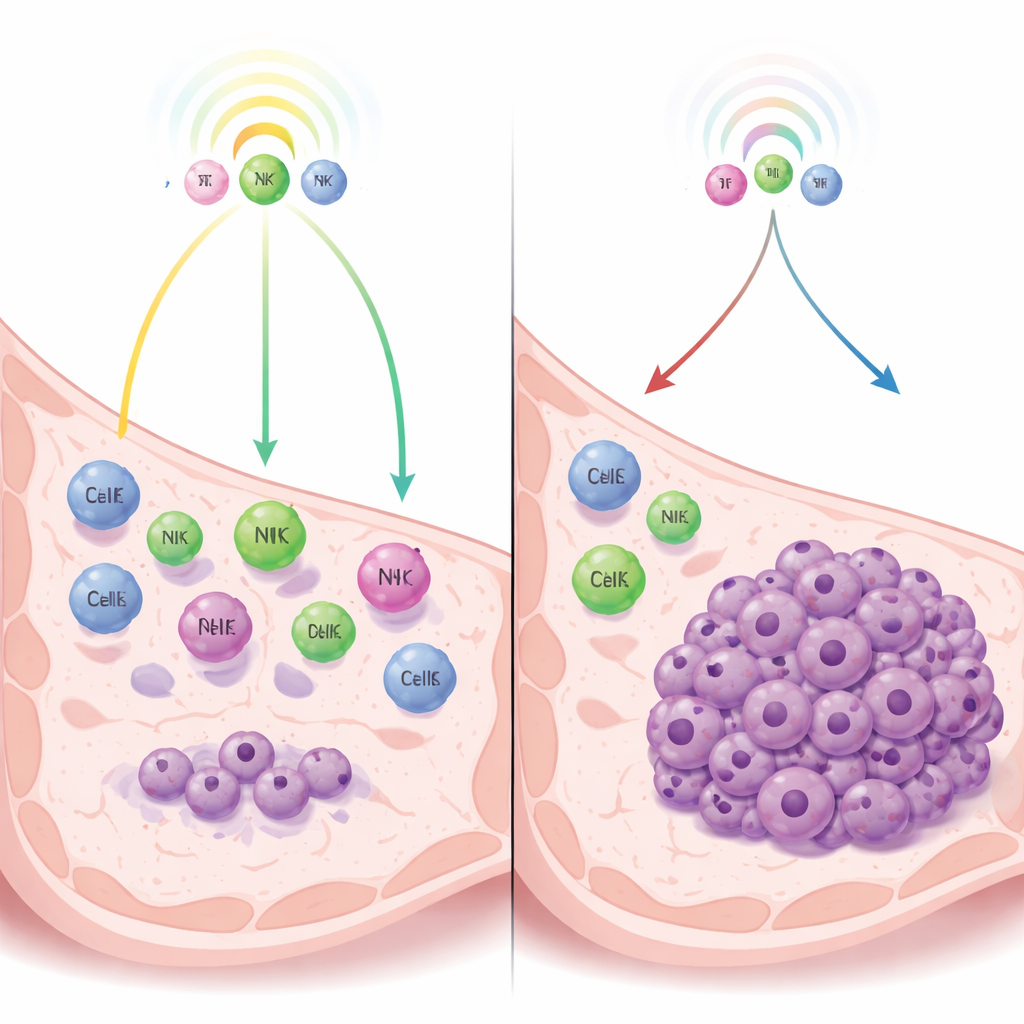
Перетягивание каната между раком и иммунной системой
Авторы сосредотачиваются на виде дремоты, контролируемом не нехваткой кровоснабжения и не внутриклеточными тормозами роста, а иммунным надзором — постоянным наблюдением иммунных клеток, которые могут сдерживать опухоль, не уничтожая её полностью. На моделях тройного негативного рака молочной железы у мышей они сравнивают опухолевые клетки, которые естественно остаются в дремоте, с близкородственными клетками, дающими быстрорастущие опухоли. Анализируя, какие гены активируются, исследователи обнаруживают, что у дремлющих клеток сильно включены интерфероновые пути — сигнальные системы тревоги иммунитета, стимулирующие выделение молекул‑медиаторов, привлекающих иммунные клетки в область опухоли.
Ключевой химический медиатор, который удерживает опухоли в тишине
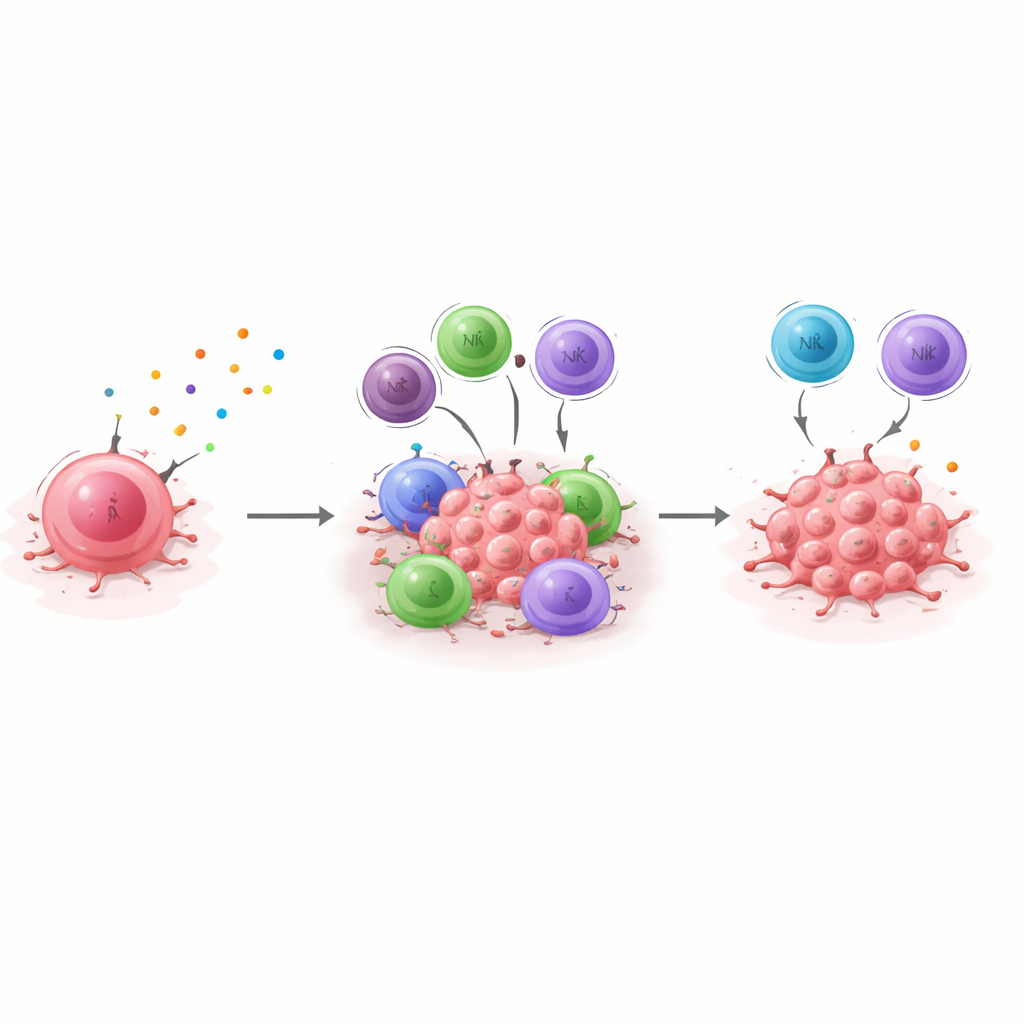
Среди многих молекул, активированных в дремлющих клетках, выделяется одна: CXCL10, небольшой белок, действующий как маячок для иммунных клеток, несущих его партнёрный рецептор CXCR3. Дремлющие раковые клетки продуцируют гораздо больше CXCL10, чем их агрессивные аналоги. Когда исследователи целенаправленно выключают CXCL10 в дремлющих клетках и имплантируют их мышам с интактной иммунной системой, ранее спокойные клетки быстро формируют опухоли. Блокирование рецептора CXCR3 с помощью антитела даёт похожий эффект. В обоих случаях клетки рака выходят из иммунного паритета и начинают расти, показывая, что ось CXCL10/CXCR3 не просто коррелирует с дремотой — она необходима для её поддержания.
Как изменение местной «окружения» меняет равновесие
Снижение уровня CXCL10 влияет не только на один путь; оно перестраивает весь локальный иммунный ландшафт. В опухолях, потерявших CXCL10, уменьшаются числа полезных CD4 и CD8 Т‑клеток, тогда как определённые миелоидные клетки, способные подавлять иммунные ответы, становятся более многочисленными. Также меняется количество естественных киллеров и дендритных клеток. Такая картина наблюдается как в первичных опухолях, так и в лёгких, куда раковые клетки могут метастазировать и затаиться. Даже когда лёгочные метастазы слишком малы, чтобы увидеть их под микроскопом, молекулярные маркёры показывают: в отсутствие CXCL10 больше клеток успешно оседает в лёгких, и в эти ткани проникает меньше Т‑клеток. При этом у мышей с полностью нарушенной иммунной системой удаление CXCL10 не даёт эффекта — дремлющие клетки растут вне зависимости от этого — что подчёркивает: этот сигнал действует через иммунный контроль, а не как прямой тормоз роста раковых клеток.
Почему усиление сигнала полезно, но не волшебная кнопка
Команда также проверяет противоположную гипотезу: может ли повышение уровня CXCL10 превратить агрессивную опухоль в дремлющую? Когда они инженерно заставляют быстрорастущие раковые клетки продуцировать дополнительный CXCL10, опухоли растут медленнее и появляются позже, а в крови увеличиваются некоторые типы иммунных клеток. Однако полной дремоты не наступает; в конце концов у всех мышей всё равно развиваются опухоли. Это указывает на то, что хотя CXCL10 необходим для поддержания дремоты при наличии остального иммунного аппарата, он сам по себе не может создать это сложное состояние «с нуля». Другие пути должны сотрудничать, чтобы установить длительный баланс между иммунной атакой и выживанием раковых клеток.
От экспериментов на мышах к прогнозу для пациентов
Чтобы связать результаты с человеческим заболеванием, исследователи выделяют «подпись дремоты» — набор генов, которые стабильно выше в дремлющих клетках и снижаются при подавлении CXCL10. Затем они анализируют большие наборы клинических данных по раку молочной железы и проверяют, как эта подпись соотносится с выживаемостью. При тройном негативном раке молочной железы пациенты, опухоли которых экспрессируют эту подпись дремоты в более высоких уровнях, живут дольше в целом и дольше остаются без рецидивов, что согласуется с идеей о том, что иммунологически контролируемая дремота отсрочивает возвращение болезни. Такого эффекта не наблюдается в той же мере для гормон‑положительных опухолей, что подчёркивает биологические различия между подтипами рака молочной железы. В совокупности результаты указывают, что ось CXCL10/CXCR3 является центральной опорой иммуномедиируемой дремоты при тройном негативном раке молочной железы, и что измерение этой подписи дремоты может помочь выявлять пациентов, которые с большей вероятностью выиграют от терапий, усиливающих иммунный контроль, — или, наоборот, тех, кто требует более тщательного долгосрочного наблюдения, потому что их рак хуже удерживается под контролем.
Цитирование: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
Ключевые слова: тройной негативный рак молочной железы, опухолевая дремота, иммунный надзор, хемокиновая сигнализация, ось CXCL10 CXCR3