Clear Sky Science · ru
Пространственный анализ экспрессии генов выявляет факторы крайне ранней метастазирования в лимфатические узлы при раке молочной железы
Почему имеют значение крошечные путешествующие раковые клетки
Когда рак молочной железы выходит за пределы груди, он часто первым останавливается в соседних лимфатических узлах — небольших фильтрах, помогающих бороться с инфекцией. Врачи знают, что обнаружение рака в этих узлах обычно указывает на более высокий риск рецидива. Но то, что происходит в самые первые моменты, когда в узле появляется всего несколько клеток, почти невозможно было увидеть у реальных пациентов. В этом исследовании использовали новый тип микроскопической «карты» активности генов, чтобы проследить эти первые этапы с беспрецедентной детализацией, выявив, какие клетки преуспевают, какие терпят неудачу и почему это важно для исхода у пациентов.
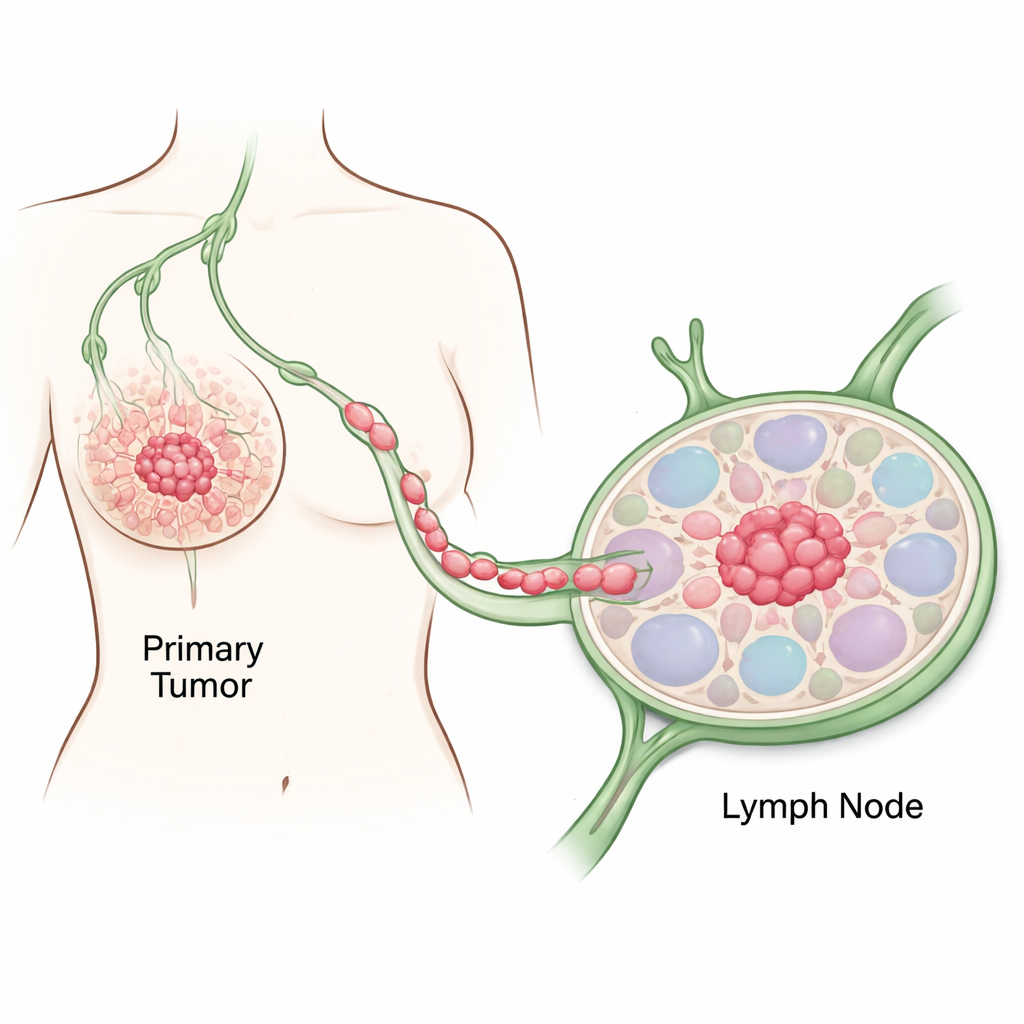
Следы первых шагов рака
Исследователи сосредоточились на ткани 80‑летней женщины с агрессивным HER2‑позитивным раком молочной железы. Они взяли образцы как внешне нормальных участков груди, так и близлежащих опухолевых зон, затем применили несколько ДНК‑ и РНК‑тестов, чтобы отследить, как обычные клетки превращались в раковые. По сравнению со здоровой тканью опухолевые регионы показали классические признаки рака: нарушение клеточной адгезии, чрезмерную пролиферацию, масштабные изменения метилирования ДНК и ключевые мутации в генах, контролирующих рост и стабильность генома. Эти молекулярные сдвиги соответствовали тому, что патологи наблюдали под микроскопом, подтверждая ступенчатый переход от нормальных клеток молочной железы к полностью злокачественным.
Клетки, меняющие форму, в движении
Чтобы понять, как опухолевые клетки начинают мигрировать, команда использовала высокоразрешающую методику, читающую активность генов в отдельных клетках при сохранении их точного положения в ткани. Это позволило реконструировать, как клетки рака изменяли свою идентичность по мере выхода из нормальных структур груди и движения к метастазированию. Они обнаружили, что опухоль, по‑видимому, возникала из одного особого типа зрелой клеткмолочной железы, которая затем постепенно приобретала черты процесса, называемого эпителиально‑мезенхимальным переходом — своего рода «смены формы», помогающей клеткам ослаблять сцепление, перемещаться и вторгаться в соседние ткани. Вместо простого включения‑выключения клетки занимали спектр смешанных состояний, сочетая «эпителиальные» признаки (упорядоченные, сцепленные) с «мезенхимальными» признаками (подвижные, инвазивные). Некоторые из этих гибридных клеток рассредотачивались по опухоли, в то время как другие образовывали кластеры более продвинутых опухолевых групп, подготовленных к распространению в лимфатические узлы.
Первый отдалённый плацдарм в лимфатическом узле
В лимфатическом узле, который стандартные клинические тесты сочли свободным от метастазов, учёные заметили нечто примечательное: всего около 30 отдельных опухолевых клеток, занимающих область шириной примерно 200 микрометров — примерно вдвое ширины человеческого волоса. Эти изолированные опухолевые клетки происходили из нескольких разных гибридных состояний, каждое со своим паттерном активности генов. Группируя родственные раковые клетки, команда выделила шесть подтипов с разными ролями. Один подтип, выраженно «мезенхимальный», выглядел особенно способным противостоять гибели клеток и уклоняться от иммунного атаки. Другой подтип, вернувший более эпителиальные черты, показал заметный сдвиг в использовании энергии, отдавая предпочтение обмену жирных кислот. Только эта метаболически перестроенная, более эпителиально‑подобная группа успешно образовывала небольшие колонии в лимфатических узлах, что указывает на то, что выбор топлива — а не только инвазивность — помогает определить, смогут ли ранние прибывшие закрепиться.
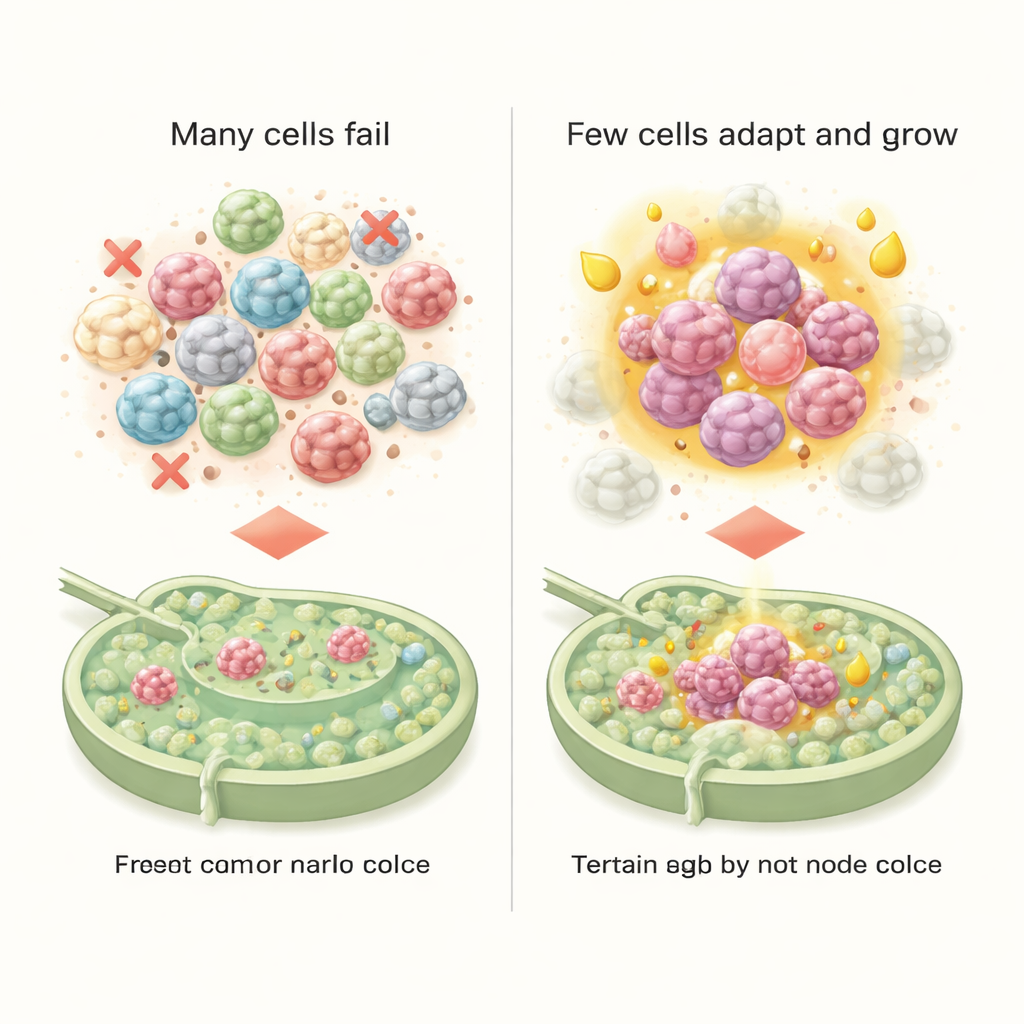
Лимфатический узел, который тихо помогает раку
Исследование также изучило, как среда лимфатического узла реагирует на этих захватчиков. Ещё до того, как сформировался заметный метастаз, иммунные клетки, клетки кровеносных сосудов и соединительной ткани уже посылали сигналы, которые ослабляли иммунные реакции и поддерживали выживание опухоли. Определённые пары рецептор‑лиганд между иммунными клетками указывали на раннюю иммунную толерантность, в то время как другие стимулировали рост новых сосудов и перестройку тканевого каркаса. В совокупности эти изменения создавали нишу, которая была удивительно благоприятна для метаболически адаптированных раковых клеток, помогая им выживать, расти и потенциально давать начало дальнейшему распространению.
Что это значит для пациентов
Сопоставив свои данные с большими имеющимися клиническими наборами, исследователи сделали контринтуитивное открытие. Клетки, лучшие в формировании ранних колоний в лимфатических узлах, и даже те, у которых были сильнейшие мезенхимальные черты, не соответствовали худшим клиническим исходам. Вместо этого наихудшие результаты наблюдались у пациентов, чьи опухоли содержали определённые агрессивные гибридные типы клеток, отмеченные высокой клеточно‑цикловой активностью и программами сжигания сахара (гликолиз), управляемыми такими генами, как MYC. Иными словами, разные состояния клеточной «смены формы» специализируются: одни хорошо осваивают тихое колонизирование новых участков, тогда как другие стимулируют быстрый рост и рецидив. Понимание и таргетирование этих различных состояний клеток и их метаболических предпочтений может привести к более точным терапиям — тем, которые не только надёжнее обнаруживают раннее распространение, но и отрезают типы опухолевых клеток, наиболее склонные вызывать смертельные рецидивы.
Цитирование: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
Ключевые слова: метастазирование рака молочной железы, лимфатический узел, эпителиально-мезенхимальный переход, пространственная транскриптомика, метаболизм рака