Clear Sky Science · ru
Сигнальная передача CD52 через сиглек-G макрофагов как терапевтическая мишень для иммунотерапии рака
Почему некоторые раки молочной железы скрываются от иммунной системы
Тройная‑негативная рак молочной железы — одна из самых опасных форм рака молочной железы, потому что он быстро распространяется и лишён многих распространённых терапевтических мишеней. В этом исследовании изучается недавно обнаруженный механизм, с помощью которого эти опухоли могут ускользать от защиты организма, и показано, как блокирование этого пути побега может сделать иммунную терапию более эффективной.
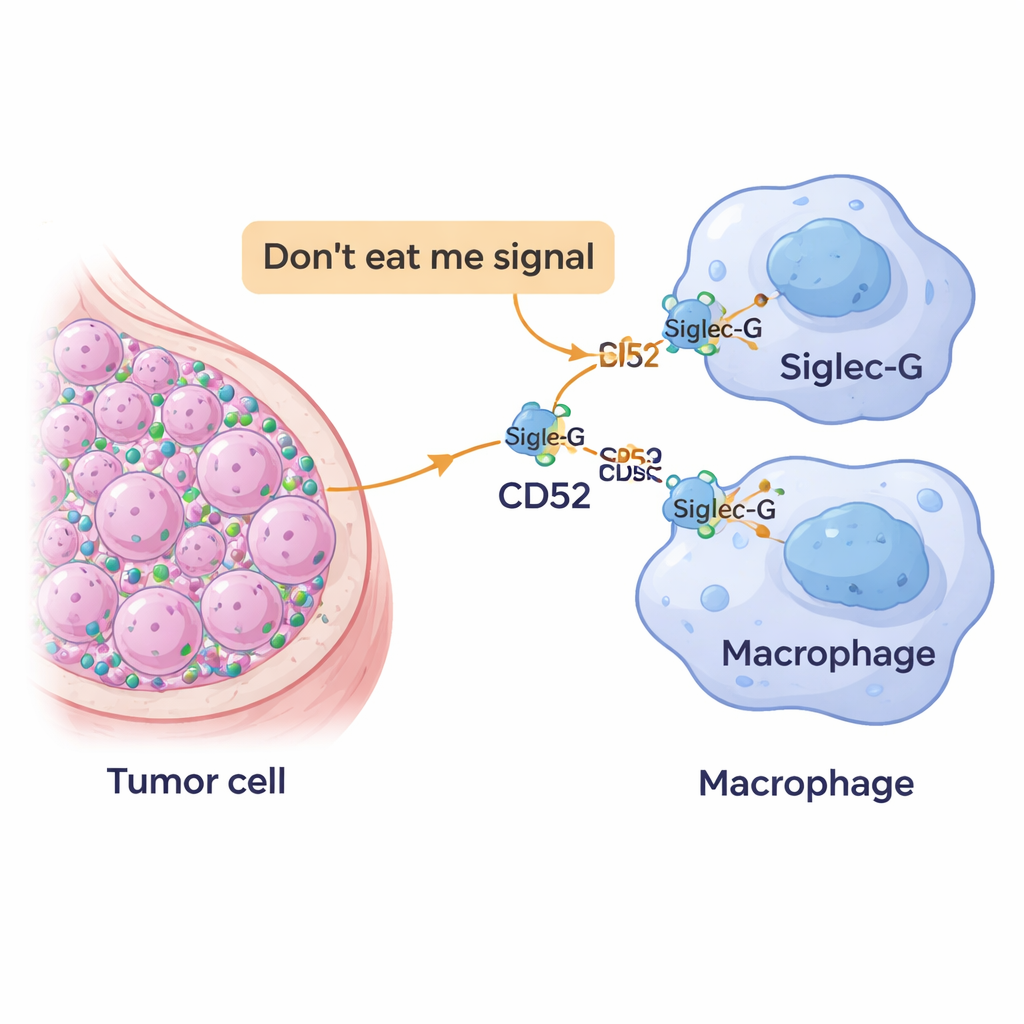
Новый «не ешь меня» флаг на раковых клетках
Наша иммунная система опирается на клетки‑«санитары» — макрофаги, которые патрулируют ткани и поглощают опасные или аномальные клетки. Чтобы избежать ошибочного уничтожения, здоровые клетки показывают поверхностные маркеры, которые по сути означают «я здесь свой». Раковые клетки часто перехватывают эту систему, чрезмерно экспрессируя такие защитные сигналы, превращая их в мощные «не ешь меня» флаги. Исследователи сосредоточились на молекуле CD52, уже известной по заболеваниям крови и аутоиммунным расстройствам, и выясняли, используют ли её раковые клетки молочной железы, чтобы убегать от атаки макрофагов.
Обнаружение CD52 в агрессивных опухолях молочной железы
Команда проанализировала крупные публичные базы данных по раку и образцы тканей пациентов. Они обнаружили, что опухоли молочной железы, особенно тройной‑негативный тип, вырабатывают больше CD52, чем нормальная ткань молочной железы. Более того, опухоли с повышенным уровнем CD52 чаще были менее дифференцированы — признаком, часто связанного с большей агрессивностью заболевания. Одновременно иммунные клетки в и вокруг опухолей несли высокий уровень взаимодействующего белка Siglec‑10 (и его мышиного аналога Siglec‑G), расположенного на макрофагах и способного посылать внутри этих клеток сигналы успокоения. В сумме эти данные указывали на то, что CD52 на опухолевых клетках может напрямую взаимодействовать с Siglec‑G на макрофагах, препятствуя их функции.
Отключение CD52, чтобы освободить макрофагов
Чтобы проверить эту гипотезу, учёные использовали инструменты редактирования генома, чтобы удалить CD52 из мышиных тройно‑негативных раковых клеток молочной железы. Когда изменённые клетки смешивали с макрофагами в лаборатории, макрофаги поглощали значительно больше опухолевых клеток по сравнению с незатронутыми раковыми клетками. Важно, что сами раковые клетки после потери CD52 не демонстрировали значительных изменений в росте или выживаемости, что указывает на то, что ключевой эффект связан с распознаванием иммунной системой, а не с собственной биологией опухолевых клеток. Когда те же клетки имплантировали мышам, опухоли без CD52 формировались меньше и были окружены макрофагами, указывающими на усиленное поглощение раковых клеток. Если же мышей лишали макрофагов, это преимущество в замедлении роста исчезало, подтверждая, что основная роль CD52 — защищать опухоли от поедания.
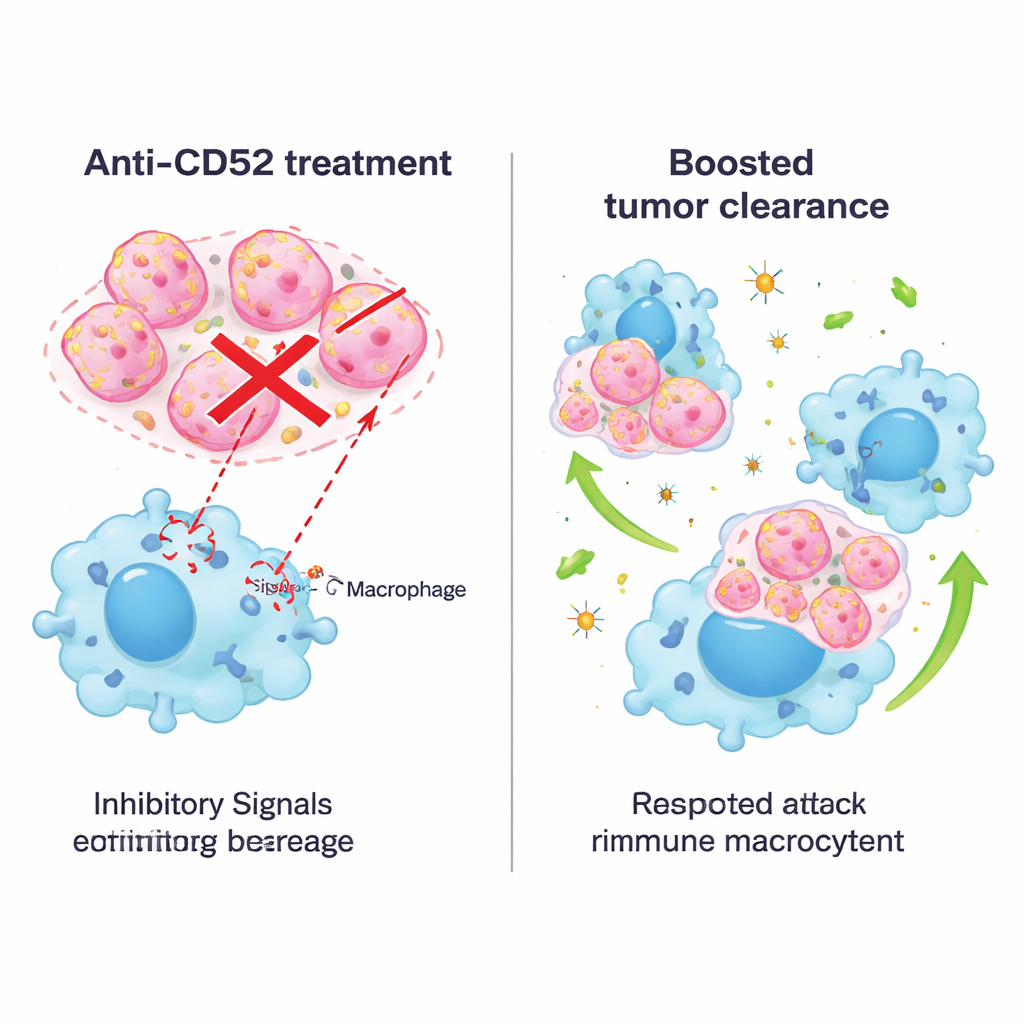
Блокирование сигнала антителами и комбинированные подходы
Поскольку препараты, нацеленные на CD52, уже применяются при других заболеваниях, исследователи далее испытали блокирующее антитело в мышиных моделях. Лечение мышей с опухолями анти‑CD52 антителом снизило рост опухолей, продлило выживаемость и не вызывало явного повреждения органов или потери веса. В культурах аналогичные антитела усиливали способность как мышиных, так и человеческих макрофагов захватывать раковые клетки молочной железы разных подтипов, а не только тройно‑негативные. Затем команда сочетала блокаду CD52 с анти‑PD‑1 терапией, широко применяемым препаратом, нацеленным на Т‑клетки. В спонтанной мышиной модели тройно‑негативного рака молочной железы комбинация сработала лучше, чем любая из стратегий по отдельности: опухоли уменьшались сильнее, макрофаги становились более провоспалительными и активными, в опухоль проникало больше эффективных Т‑клеток‑убийц, а число истощённых Т‑клеток снижалось.
Что это означает для будущего лечения рака молочной железы
Эта работа выявляет CD52 как ранее не признанный сигнал «не ешь меня», который тройно‑негативные раковые клетки молочной железы используют, чтобы отразить макрофагов. Прерывая «диалог» между CD52 на опухолевых клетках и Siglec‑G на макрофагах, исследователи смогли вновь активировать как врождённые иммунные клетки, так и, косвенно, Т‑клетки, особенно в сочетании с блокадой PD‑1. Хотя необходимы дополнительные исследования по безопасности и клинические испытания — поскольку CD52 также присутствует на многих нормальных иммунных клетках — эти результаты указывают на перспективную стратегию двойной блокировки контрольных точек, которая может превратить трудно‑лечимые, устойчивые к иммунитету опухоли молочной железы в такие, которые лучше реагируют на иммунотерапию.
Цитирование: Qin, X., Chang, Y., Qiu, Y. et al. CD52 signaling via macrophage Siglec-G represents a therapeutic target for cancer immunotherapy. npj Breast Cancer 12, 29 (2026). https://doi.org/10.1038/s41523-026-00895-3
Ключевые слова: тройная‑негативная рак молочной железы, макрофаги, иммунотерапия, CD52, блокада контрольных точек