Clear Sky Science · ru
Совместная доставка хемокина CXCL9 и ко-стимулирующего лиганда TNFSF9 мезенхимальными стволовыми клетками перенастраивает иммунную микросреду при тройном отрицательном раке молочной железы
Почему этот новый подход к раку молочной железы важен
Тройной отрицательный рак молочной железы — одна из самых опасных форм рака груди: он быстро растет, рано дает метастазы и лишен распространенных гормональных мишеней, на которые ориентированы многие лекарства. Иммунотерапия внушает надежду, но у многих пациентов защитные клетки организма просто не проникают в опухоль в достаточном количестве, чтобы изменить ход болезни. В этом исследовании изучается изобретательная стратегия: использование живых переносчиков в роли «автомобилей‑доставщиков», которые доставляют иммуномодулирующие сигналы прямо в трудноизлечимые опухоли, что потенциально может сделать больше пациентов доступными для мощных иммунных методов лечения.
Суровый рак с недостаточной иммунной поддержкой
Стандартные методы лечения тройного отрицательного рака молочной железы — операция, химиотерапия и лучевая терапия — часто не предотвращают рецидив, а средняя выживаемость при распространенном заболевании остается менее двух лет. Одна из ключевых причин в том, что многие из этих опухолей «холодные», то есть содержат мало противораковых иммунных клеток. Анализ крупных баз данных пациентов показал, что у людей, чьи опухоли естественно вырабатывают больше двух иммунных молекул — CXCL9 и TNFSF9, — как правило, дольше выживаемость и в опухолях больше Т‑клеток и естественных киллеров (NK). CXCL9 действует как химический сигнал, привлекающий иммунные клетки в ткани, тогда как TNFSF9 работает как дополнительный «газ», усиливающий их атаку. Такая картина навела на мысль, что повышение обоих сигналов непосредственно в опухоли может склонить чашу весов в пользу иммунной системы.
Превращение стволовых клеток в «умные» машины доставки
Исследователи сосредоточились на мезенхимальных стволовых клетках, полученных из донорских пуповинных канатиков человека. Эти клетки обладают полезным свойством: при введении в кровоток мышей с опухолями молочной железы они естественным образом направляются в очаги опухоли и задерживаются там в течение нескольких дней, при этом в значительной степени обходя нормальные органы. Команда генетически модифицировала эти стволовые клетки так, чтобы они выделяли CXCL9 и экспонировали TNFSF9 на своей поверхности, создав двухфункциональную клеточную терапию, которую назвали MSC‑T9C9. Лабораторные испытания показали, что модифицированные клетки выделяют высокие уровни CXCL9 и сильно активируют мышиные Т‑клетки и NK‑клетки, не меняя при этом собственного профиля роста и не вызывая появления опухолей. Это сделало их многообещающими кандидатами в целевые иммунные усилители.
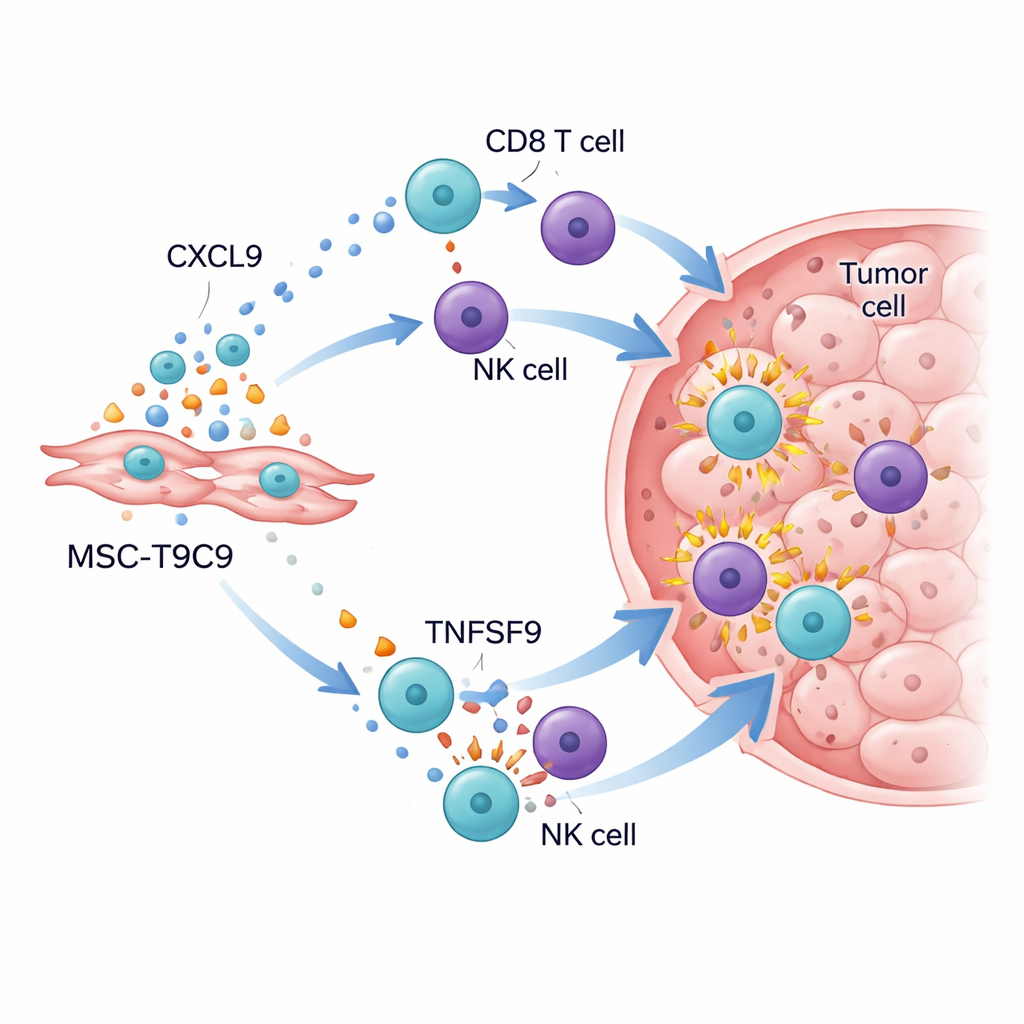
Пробуждение иммунного поля битвы в опухоли
Когда эти генетически модифицированные клетки вводили мышам с тройным отрицательным раком молочной железы, результаты были впечатляющими. У мышей с функционирующей иммунной системой многократные инъекции MSC‑T9C9 значительно замедляли рост опухолей и усиливали гибель раковых клеток, в то время как контрольные стволовые клетки давали мало эффекта. Детальный анализ опухолей показал драматический рост числа CD8 «киллерных» Т‑клеток и NK‑клеток, а также повышение уровней мощных молекул атаки, таких как гранзим B, интерферон‑γ, фактор некроза опухоли‑α и интерлейкин‑2. Одновременно микросреда опухоли сместилась от подавляющего состояния: увеличилось число провоспалительных макрофагов, и хотя регуляторные Т‑клетки по‑прежнему присутствовали, они оказались в меньшинстве по сравнению с новой волной бойцов. В иммундефицитных мышах, лишенных Т‑ и NK‑клеток, MSC‑T9C9 не замедляли рост опухолей, что подтверждает зависимость эффективности от мобилизации собственных защит организма.
Подготовка опухолей к терапии блокадами контрольных точек
Современные препараты иммунотерапии, такие как анти‑PD‑1‑антитела, снимают молекулярные «тормоза» с Т‑клеток, но они работают лучше, когда в самой опухоли уже присутствует достаточное число Т‑клеток. В исследовании показано, что MSC‑T9C9 не только привлекали больше CD8 Т‑клеток в опухоли, но и переводили их в высокоактивное, но чувствительное к «тормозам» состояние, отмеченное рецептором PD‑1. В модельных экспериментах у мышей сочетание MSC‑T9C9 с анти‑PD‑1‑препаратом давало наибольшее уменьшение опухолей и наибольшую выживаемость по сравнению с любым из методов по‑отдельности. Анализы человеческих онкологических наборов данных поддержали эту идею: у пациентов с более высокими совокупными уровнями TNFSF9 и CXCL9 вероятность пользы от терапии блокадами контрольных точек была выше, что указывает на то, что та же биология может действовать и у людей.
Безопасность и перспективы
Любое лечение, усиливающее иммунитет, вызывает опасения по поводу опасных побочных эффектов, таких как системное воспаление или повреждение органов. Обнадеживающе, у мышей, получавших MSC‑T9C9, наблюдались нормальная масса тела и поведение, не было очевидных повреждений главных органов, а анализы крови и показатели функций печени и почек оставались в пределах нормы. Важно, что всплеск иммунной активности в основном ограничивался самой опухолью, а уровни провоспалительных сигналов в кровотоке не повышались. Хотя перед клиническими испытаниями необходимо провести дополнительные работы — включая тесты в более реалистичных моделях и тщательное определение дозы, — это исследование показывает, что направленная доставка генетически модифицированных стволовых клеток в опухоли с целью привлечения и активации иммунных клеток может предложить целевой, потенциально более безопасный путь превращения «холодных» тройных отрицательных раков молочной железы в «горячие», лучше откликающиеся на иммунотерапию.
Цитирование: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Ключевые слова: тройной отрицательный рак молочной железы, иммунотерапия, мезенхимальные стволовые клетки, микросреда опухоли, блокада контрольных точек