Clear Sky Science · ru
Интерлейкин‑1α, происходящий от хозяина, вызывает иммуноподавление опухоли путем перепрограммирования ассоциированных с опухолью миелоидных клеток
Почему это исследование важно для пациентов с раком
Иммунотерапия преобразила лечение некоторых видов рака, но многие опухоли молочной железы по‑прежнему ускользают от иммунной системы. В этой работе исследуют менее известного виновника: сигнальную молекулу интерлейкин‑1α (IL‑1α), вырабатываемую не самими раковыми клетками, а нормальными клетками организма. Авторы показывают, что IL‑1α, происходящий от хозяина, может тихо перевести иммунные клетки в союзники опухоли, и что блокирование этого сигнала у мышей приводит к уменьшению или исчезновению опухолей молочной железы. Понимание этого переключателя может помочь врачам разработать лечения, делающие иммунотерапию более эффективной при раке молочной железы.
Скрытое влияние в «окрестностях» опухоли
Опухоли не растут в изоляции; они живут в оживленном «округе» иммунных клеток, кровеносных сосудов и соединительной ткани, известном как микроокружение опухоли. Одними из важнейших обитателей являются миелоидные клетки, особенно макрофаги, которые могут либо атаковать опухоль, либо защищать её. Классические учебники делят макрофаги на M1 (борющиеся с опухолью) и M2 (поддерживающие опухоль), но в реальных опухолях встречаются многие промежуточные состояния. Авторы сосредоточились на IL‑1α, молекуле, обычно производимой нераковыми тканями, чтобы выяснить, направляет ли этот сигнальный фактор поступающие миелоидные клетки к полезным или вредным ролям внутри опухолей молочной железы.
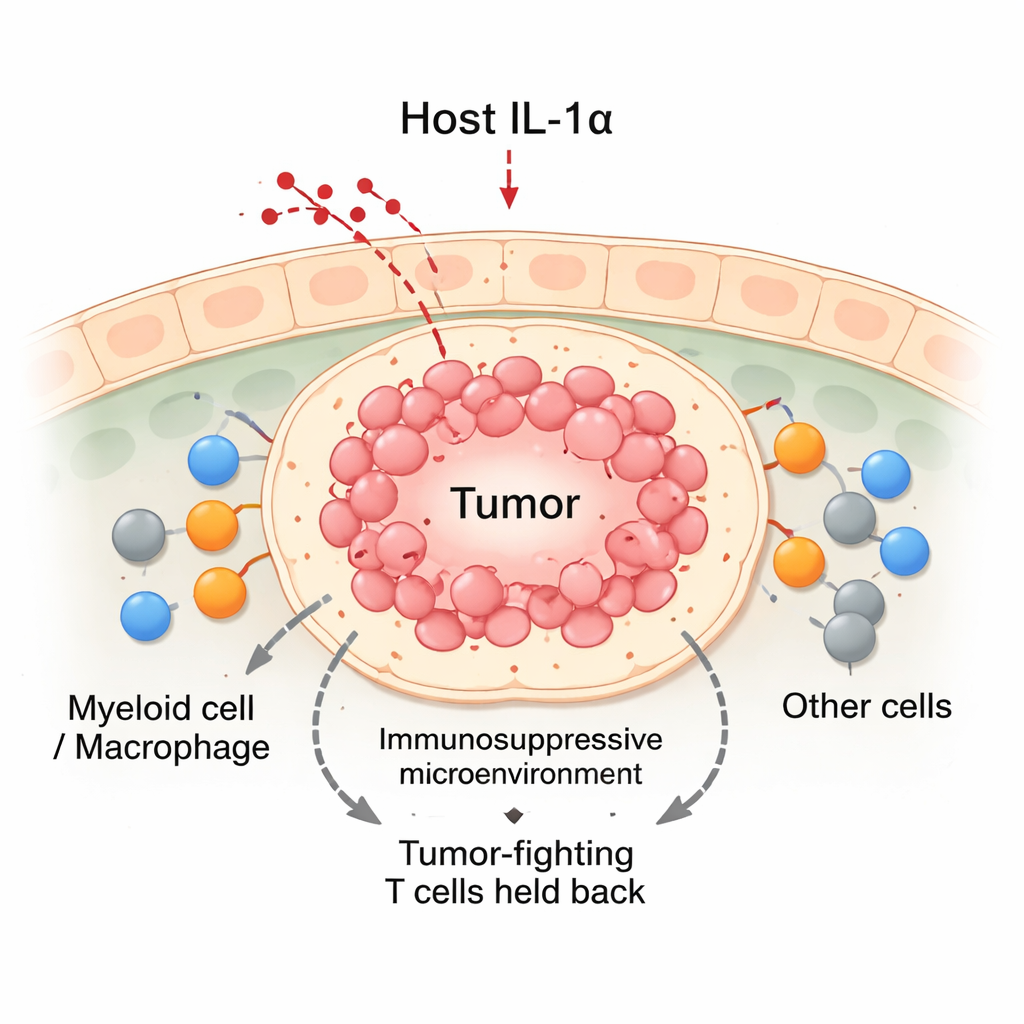
Отключение IL‑1α меняет баланс в пользу борьбы с опухолью
Используя модели рака молочной железы у мышей, команда сравнила нормальных животных с генетически модифицированными, лишёнными IL‑1α. Когда раковые клетки пересаживали в молочные железы, опухоли у нормальных мышей росли стабильно. Напротив, в мышей без IL‑1α опухоли сначала росли около двух недель, а затем часто регрессировали. В этих регрессирующих опухолях в целом было больше иммунных клеток, включая всплеск цитотоксических CD8‑Т‑клеток и миелоидных клеток. Хотя у мышей без IL‑1α в крови циркулировало меньше лейкоцитов, в ткани опухоли накапливалось значительно больше иммунных клеток. Детальные анализы показали, что инфильтрированные CD8‑Т‑клетки в опухолях без IL‑1α были более активны: они вырабатывали больше молекул, убивающих опухолевые клетки, и проявляли меньше признаков истощения.
Как IL‑1α перестраивает ассоциированные с опухолью миелоидные клетки
Чтобы понять, что делает IL‑1α на клеточном уровне, исследователи использовали секвенирование РНК отдельных клеток, чтобы изучить тысячи отдельных клеток из опухолей. Они обнаружили, что IL‑1α производит лишь небольшая подгруппа ассоциированных с опухолью макрофагов — те, которые отмечены рецептором CX3CR1. У нормальных мышей многие поступающие моноциты созревали в эти CX3CR1‑положительные макрофаги, связанные с иммуносупрессивным поведением. У мышей без IL‑1α этот путь созревания нарушался. Вместо этого миелоидные клетки с большей вероятностью становились iNOS‑положительными воспалительными макрофагами, профилем, ассоциированным с анти‑опухолевой активностью. Функционально миелоидные клетки из опухолей без IL‑1α в меньшей степени индуцировали тормозящие молекулы, такие как PD‑1 и CTLA‑4, на Т‑клетках и обладали более слабой способностью подавлять пролиферацию Т‑клеток.
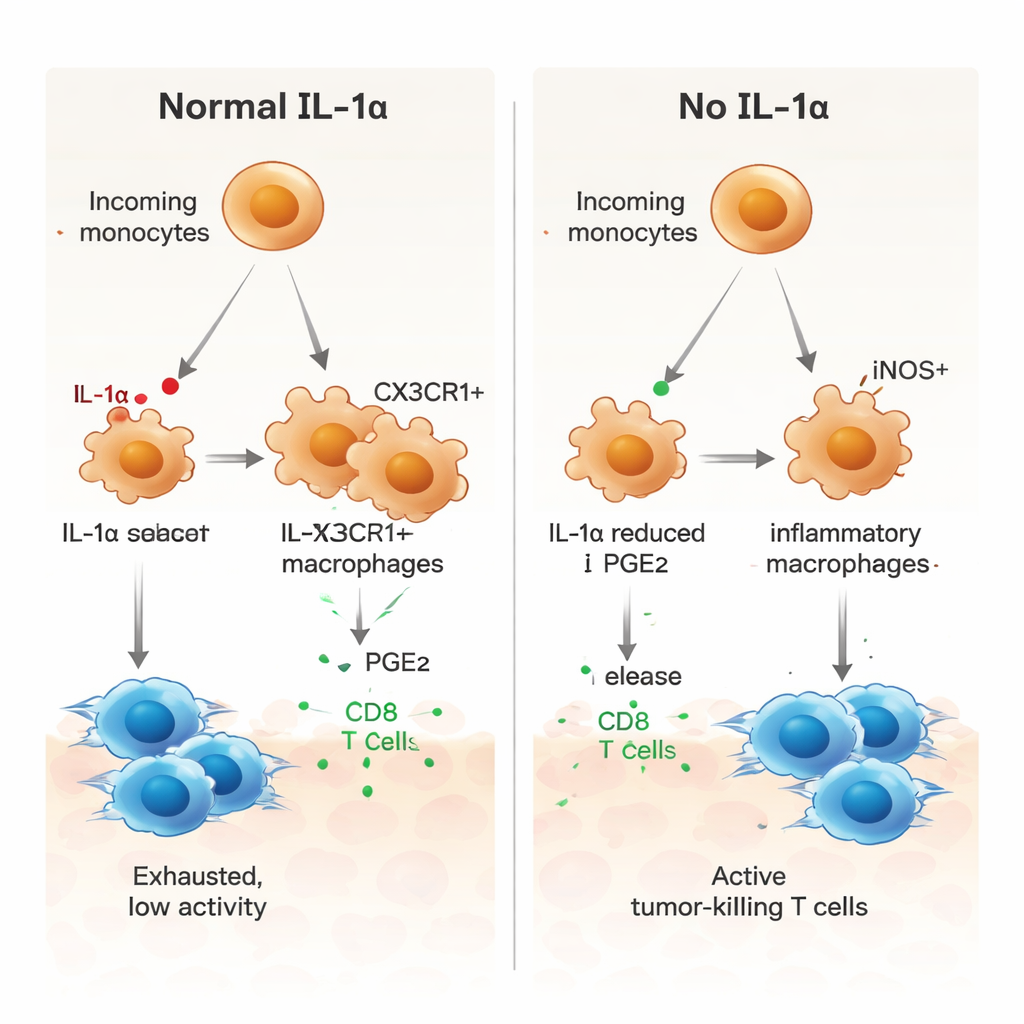
Ключевая роль липидного посредника PGE2
Затем авторы спросили, как IL‑1α направляет миелоидные клетки к поддерживающему опухоль состоянию. Анализ коммуникаций в данных одноклеточного секвенирования указал на несколько сигнальных путей, включая путь с участием простагландина E2 (PGE2), липидного медиатора, известного продвижением иммуносупрессии. В опухолях, лишённых IL‑1α, макрофаги экспрессировали более низкие уровни рецепторов фактора роста макрофагов (M‑CSF), рецепторов TGF‑β и рецептора PGE2, а ближайшие стромальные клетки вырабатывали меньше ферментов, формирующих PGE2. В культуре костного мозга макрофаги от мышей без IL‑1α проявляли более воспалительный профиль с повышенным iNOS и пониженным CX3CR1. Добавление PGE2 обращало этот сдвиг и восстанавливало более супрессивный профиль, тогда как блокирование PGE2 в нормальных макрофагах сдвигало их к провоспалительному состоянию. Макрофаги без IL‑1α также сильнее стимулировали пролиферацию опухолево‑специфичных CD8‑Т‑клеток — эффект, который ослаблялся при возвращении PGE2.
Связь находок у мышей с человеческим иммунитетом
Чтобы проверить, отражают ли их данные у мышей человеческую биологию, команда сравнила генетические подписи различных подмножеств макрофагов у мышей с большой панелью человеческих миелоидных клеток, индуцированных в лаборатории в разные состояния. Кластеры макрофагов из опухолей нормальных мышей напоминали человеческие клетки, сдвинутые в M2‑подобные, иммуноугнетающие состояния молекулами, такими как IL‑10, IL‑4 и глюкокортикоиды. Напротив, аналогичные кластеры из опухолей мышей без IL‑1α соответствовали человеческим клеткам в более воспалительных, менее супрессивных условиях. Примечательно, что генные паттерны, связанные с сигналингом PGE2, были обогащены в зависимости от IL‑1α макрофагах и отсутствовали при дефиците IL‑1α, что подкрепляет идею о совместной работе IL‑1α и PGE2 в создании иммуносупрессивной ниши.
Что это может значить для будущей терапии рака молочной железы
Проще говоря, это исследование указывает, что молекула хозяина IL‑1α может тихо приказывать определённым макрофагам защищать опухоль и сдерживать киллерные Т‑клетки, отчасти через сигналинг PGE2. Когда IL‑1α удаляют у мышей, макрофаги смещаются в более воспалительное, направленное против опухоли состояние, CD8‑Т‑клетки становятся более активными, и пересаженные опухоли молочной железы часто отторгаются. Поскольку существующие иммунотерапии уже направлены на оживление истощённых Т‑клеток, их сочетание с подходами, блокирующими IL‑1α или его путь через PGE2, могло бы ещё сильнее сместить микроокружение опухоли в пользу иммунитета пациента. Хотя необходимы дополнительные исследования для оценки безопасности и эффективности у людей, эти результаты выделяют IL‑1α как перспективную новую мишень для повышения уязвимости рака молочной железы к иммунной атаке.
Цитирование: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Ключевые слова: иммунотерапия рака молочной железы, микроокружение опухоли, макрофаги, интерлейкин‑1 альфа, простагландин E2