Clear Sky Science · ru
Микробная регуляция молекул сигнального стресса и её роль в здоровье и болезни
Как крошечные обитатели кишечника формируют нашу реакцию на стресс
Большинство из нас считает, что стресс — это то, что происходит у нас в голове, но в этой статье показано, что одни из ключевых участников ответной реакции на стресс живут в кишечнике. Микробы, населяющие наши кишечники, делают намного больше, чем просто помогают переваривать пищу: они могут синтезировать, разрушать и модифицировать те самые гормоны, которые управляют тем, как наше тело реагирует на давление, страх и боль. Понимание этого скрытого партнёрства может открыть новые пути для облегчения состояний, таких как воспалительные заболевания кишечника, депрессия и другие болезни, связанные со стрессом.
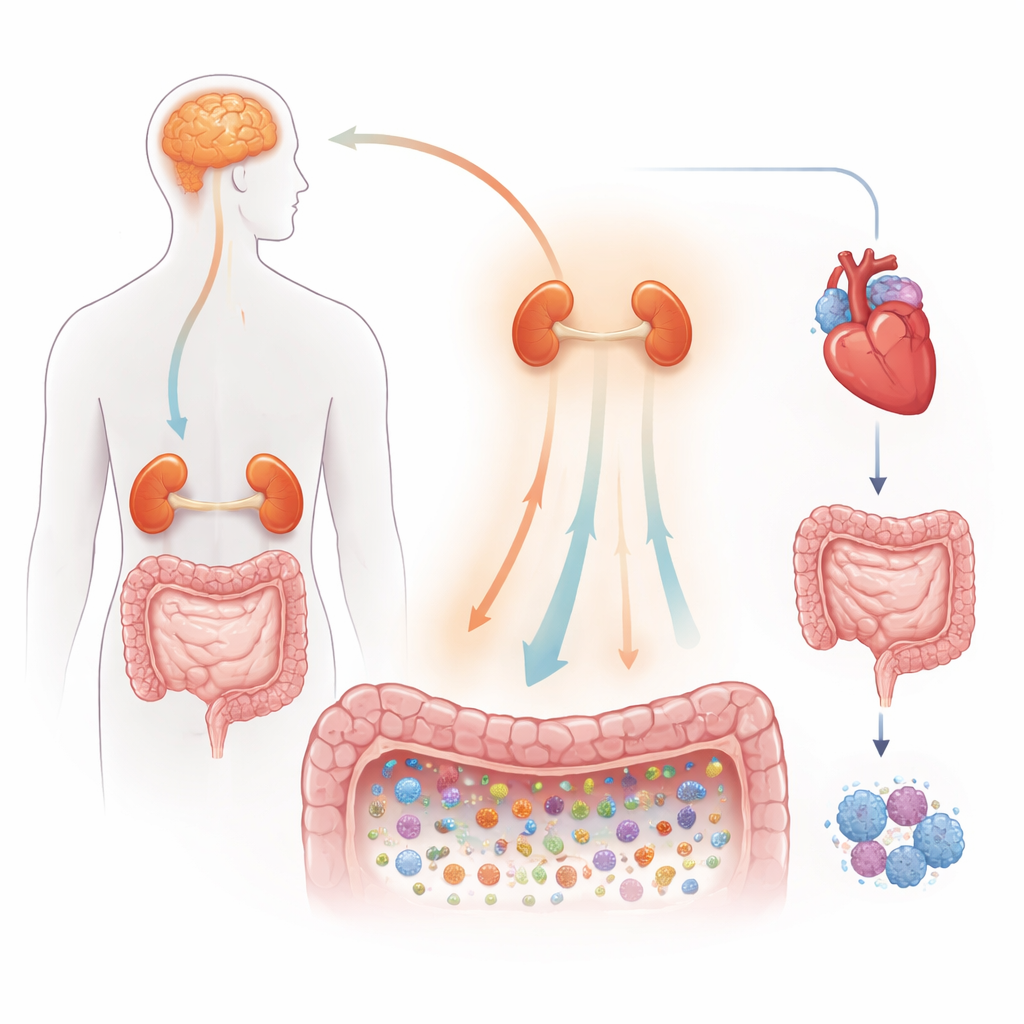
Встроенная система тревоги организма
Авторы начинают с описания того, как обычно работает реакция на стресс. Когда мы сталкиваемся с вызовом, мозг запускает цепь команд, проходящую через гипофиз и надпочечники, заливая организм химическими посредниками, такими как катехоламины, похожие на адреналин, и стероидные гормоны — глюкокортикоиды. Эти сигналы повышают частоту сердечных сокращений, перераспределяют кровоток, изменяют моторику кишечника и настраивают иммунную систему в режим «борьбы или бегства». Нервы, напрямую связанные с пищеварительным трактом, обеспечивают быструю передачу сигналов к кишечнику, сжимая или расслабляя барьер кишечника и меняя местную среду, в которой живут микробы. Это делает кишечник ключевым перекрёстком, где биология стресса и микробиом постоянно пересекаются.
Микробы, которые слушают и «разговаривают» со стрессовыми сигналами
Исследования, проведённые за несколько десятилетий, показывают, что многие бактерии могут распознавать и использовать наши стрессовые химические вещества. Ранние эксперименты продемонстрировали, что некоторые кишечные и патогенные бактерии растут быстрее и становятся более агрессивными при контакте с катехоламинами, такими как норадреналин и адреналин. Другие работы показали, что бактерии могут захватывать эти молекулы, преобразовывать их в новые формы или даже синтезировать похожие соединения из аминокислот, таких как тирозин. В то же время ферменты хозяина часто «выключают» катехоламины, присоединяя к ним небольшие химические группы; некоторые кишечные бактерии, имея соответствующие инструменты, могут отрезать эти группы, возвращая молекулам активную форму. У мышей без микробиоты большинство стрессовых медиаторов в кишечнике находятся в неактивной форме, но введение определённых бактерий восстанавливает пул активных молекул, показывая, что микробы непосредственно контролируют доступность этих сигналов.
Переработка стрессовых стероидов изнутри
Далее обзор переходит к глюкокортикоидам — стероидным гормонам, наиболее известным своей способностью усмирять воспаление и помогать организму справляться с хроническим стрессом. Небольшие количества этих гормонов поступают в кишечник из кровотока или синтезируются локально в слизистой, где они сталкиваются с густыми бактериальными сообществами. Многие кишечные микробы несут специализированные ферменты, способные отрезать, перестроить или восстановить эти стероидные молекулы. Некоторые удаляют боковые цепи, превращая их в андрогены, которые действуют ближе к половым гормонам и могут влиять на кровяное давление и даже на гормонозависимые раки. Другие убирают определённые химические группы, ослабляя способность гормона связываться с рецептором, или дополнительно восстанавливают структуру так, что она больше не может быть переработана в мощные формы. Есть и те, кто обращает ступени «инактивации» хозяина, удаляя присоединённые сульфаты или сахароподобные группы, возвращая стероиды в активный оборот. В совокупности эти действия превращают микробиом в подвижную ручку управления силой и балансом стероидов.
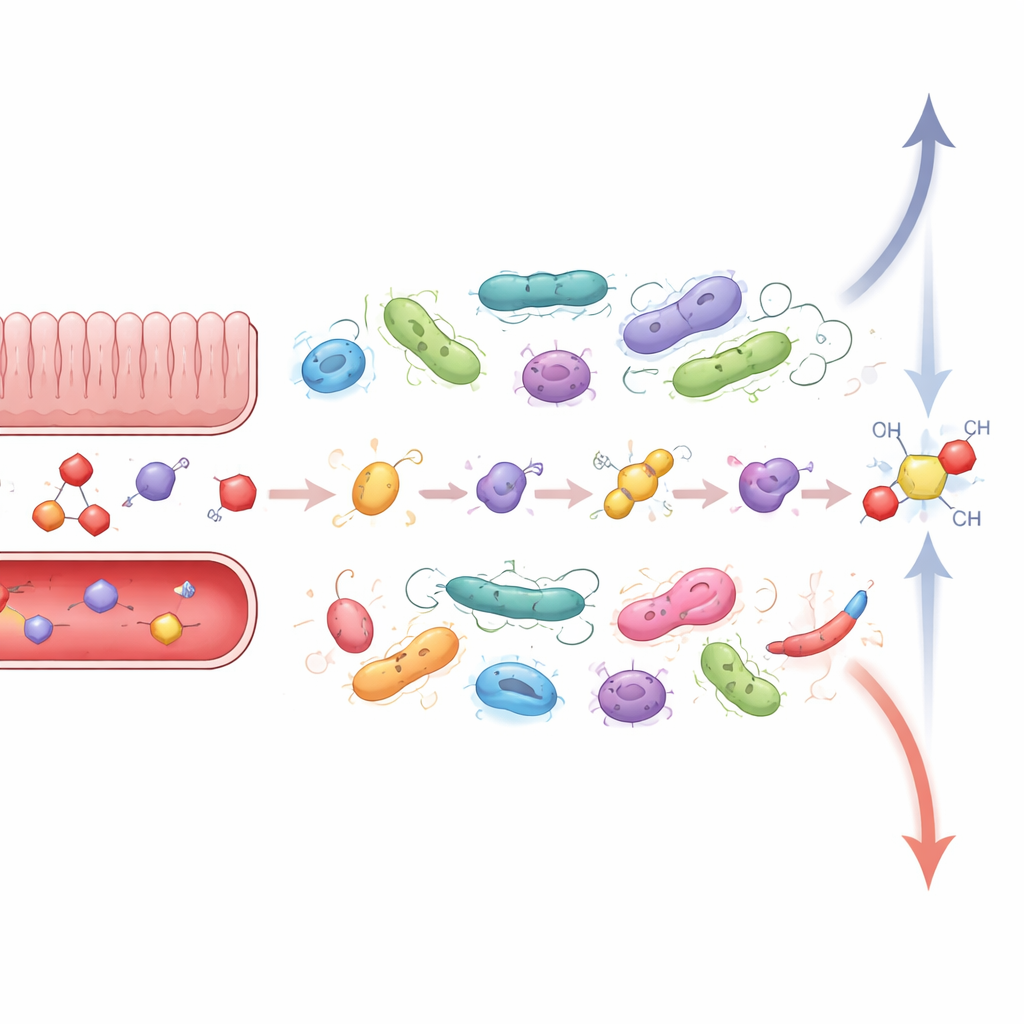
Когда стресс, воспаление и микробы подпитывают друг друга
Эти интимные химические обмены особенно важны при болезнях, где и стресс, и кишечная микробиота уже нарушены. Воспалительные заболевания кишечника (ВЗК) — яркий пример: у пациентов наблюдается хроническое воспаление кишечника, изменённый состав микробиоты и повышенная чувствительность к жизненным стрессам. Гормоны стресса могут ослаблять кишечный барьер, позволяя большему количеству микробов и их продуктам проникать через него и активировать иммунную систему. Одновременно с этим при ВЗК часто обнаруживают разрастание видов, способных перестраивать кортизол и связанные стероиды, а также потерю бактерий, производящих короткоцепочечные жирные кислоты — небольшие продукты ферментации, которые обычно помогают укреплять барьер и успокаивать воспаление. Исследования на животных указывают, что такие микробные сдвиги могут усиливать гормональные нарушения и иммунную активность, затягивая пациентов в порочный цикл, в котором стресс усугубляет болезнь кишечника, а болезнь кишечника повышает уровень стресса.
Новые способы успокоить петлю «кишечник–стресс»
Поскольку микробы находятся на стыке стрессовых сигналов и воспаления, они представляют собой привлекательную цель для новых терапий. В статье приводятся работы, показывающие, что диеты, богатые волокнами, такими как инулин, могут повышать уровень полезных продуктов ферментации, снижать воспаление кишечника и смягчать часть связанных со стрессом повреждений в моделях ВЗК. Пробиотические штаммы Lactobacillus обнаруживались как способные укреплять барьер кишечника, уменьшать всплески гормонов при стрессе и снижать чувствительность к боли у животных. Прямое введение короткоцепочечных жирных кислот в толстую кишку уменьшало поведение, похожее на тревогу, у мышей и ослабляло кортизоловые реакции на социальный стресс у людей. Эти ранние успехи предполагают, что тщательно подобранные пробиотики, пребиотики и микробные метаболиты могут помочь сбалансировать реакцию на стресс, изменяя то, как гормоны обрабатываются в кишечнике.
Что это значит для повседневного здоровья
В заключение авторы утверждают, что кишечную микробиоту следует рассматривать как активного партнёра в нашей биологии стресса, а не как пассивного наблюдателя. Синтезируя, модифицируя и рециклируя молекулы сигнальной системы стресса, микробиом может влиять на силу нашей реакции на вызовы, на скорость восстановления и на то, насколько вероятно, что стресс приведёт к хроническому заболеванию. Это не значит, что существует одна «волшебная» микробная форма, которая исцелит стресс, но это указывает на то, что защита и поддержка здоровой экосистемы кишечника может быть одним из самых мощных инструментов для выработки устойчивости. По мере того как исследователи более подробно картируют взаимодействия между микробами и гормонами и проверяют их на людях, повседневные стратегии поддержки здоровья кишечника могут стать центральной частью управления стрессом, настроением и воспалительными состояниями.
Цитирование: Sie, C., Tropini, C. Microbial regulation of stress-associated signaling molecules and its role in health and disease. npj Biofilms Microbiomes 12, 65 (2026). https://doi.org/10.1038/s41522-026-00932-w
Ключевые слова: микробиом кишечника, гормоны стресса, ось микробиота‑кишечник‑мозг, воспалительные заболевания кишечника, микробная эндокринология