Clear Sky Science · ru
Целенаправленное уничтожение маститов, вызванных Staphylococcus aureus, с помощью синтетических фагоподобных систем доставки CRISPR-Cas
Борьба с дорогостоящей инфекцией в молочном хозяйстве
Молоко коров и других сельскохозяйственных животных может быть испорчено болезненной инфекцией молочной железы — маститом, который часто вызывается бактерией Staphylococcus aureus. Лечение таких инфекций обычно требует длительного курса антибиотиков, что дорого, стрессово для животных и способствует росту устойчивости к антибиотикам. В этом исследовании рассматривается радикально иной подход: превращение естественного вирусоподобного паразита бактерий в точное оружие, способное избирательно разрезать ДНК бактерии и очищать инфекции без распространения генов резистентности.
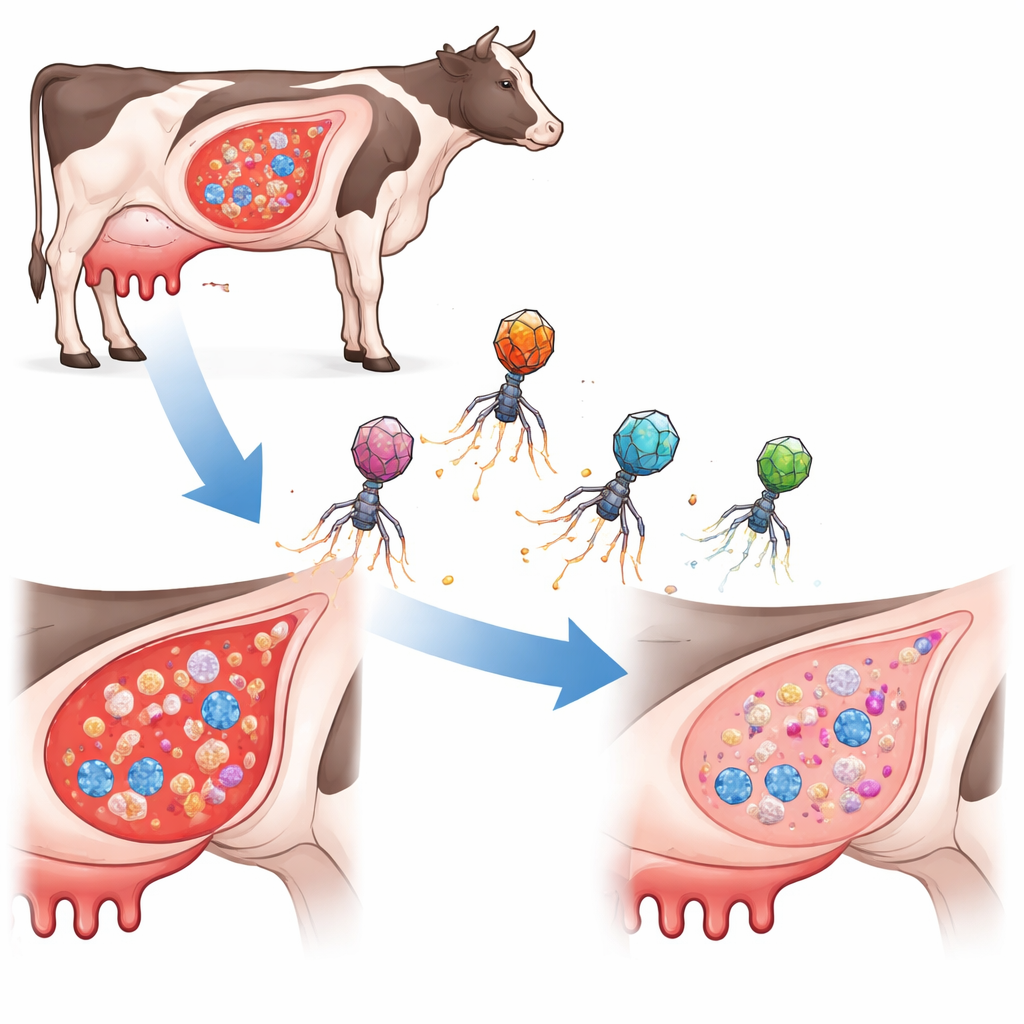
Новый тип целевого охотника на бактерии
Вместо использования традиционных антибиотиков или обычных бактериофагов (вирусов, поражающих бактерии) исследователи спроектировали крошечные элементы, несущие ДНК, известные как фаг‑индуцируемые хромосомные острова. В природе эти острова «путешествуют», запаковываясь в фаговые оболочки, чтобы переходить между бактериальными клетками. Здесь команда перестроила их как «ePICI», которые несут систему редактирования генов CRISPR‑Cas9 и короткие направляющие последовательности, нацеленные на три небольших, но важных регуляторных РНК в S. aureus. Когда ePICI попадает в целевую клетку, синтезируется Cas9, который разрезает хромосому бактерии в выбранном месте, убивая клетку изнутри. Важно, что эти инженерные частицы не реплицируются самостоятельно, что ограничивает их распространение и снижает риск случайной передачи вредных генов.
Как бактериальный щит меняет ход борьбы
S. aureus часто выживает при лечении, образуя биопленки — липкие сообщества, где клетки заключены в самосинтезируемую матрицу. Команда сравнила два распространённых типа матрикса: один, построенный преимущественно из белка Bap, и другой, состоящий из сахарного полимера, известного как PIA/PNAG. В лабораторных экспериментах биопленки, богатые Bap, сильно защищали бактерии от ePICI и от стандартного вспомогательного фага, действуя как плотная броня, блокирующая инфицирование. Напротив, биопленки на основе сахарного полимера делали бактерий более уязвимыми, вероятно потому, что ферменты на фаговых оболочках могут расщеплять эти сахара и помогать частицам добираться до целей.
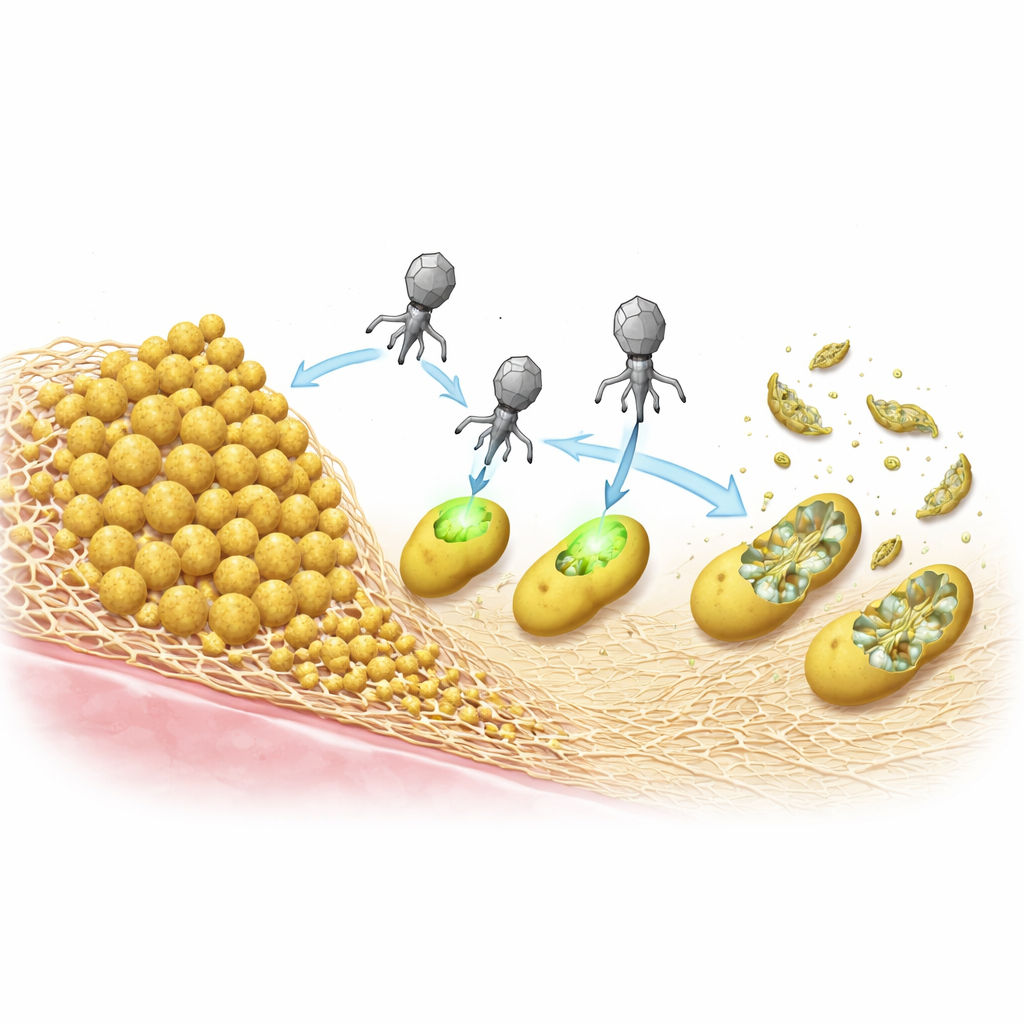
Уничтожение бактерий без встраивания их ДНК
Попав в клетку, ePICI могут интегрироваться в бактериальную хромосому, но исследователи выясняли, обязателен ли этот шаг для убийства. Они создали версию, лишённую способности интегрироваться, и показали, что при условии правильного производства частицы в исходном штамме она была столь же смертельна для S. aureus, как и оригинал. Это означает, что система CRISPR может экспрессироваться прямо с входящей кольцевой ДНК, выполнить свою задачу и затем исчезнуть по мере гибели клетки. Такое действие без интеграции ещё больше снижает шансы непреднамеренного переноса генов и отличает эти частицы от классической фаговой терапии, которая полагается на вирусную репликацию и лизис клеток для распространения.
От чашки Петри до инфицированных молочных желёз
Поскольку штаммы, продуцирующие Bap, распространены при мастите у коров, команда протестировала свой лучший конструкт, названный ePICIrsaE, на модели мыши, имитирующей инфекцию вымени. В молоке и в лабораторных культурах биопленки, богатые Bap, явно ослабляли активность ePICI. Тем не менее внутри молочной железы многократные дозы ePICIrsaE резко снижали число бактерий для всех протестированных штаммов, включая продуцирующие Bap. Его эффективность была сравнима с ванкомицином, мощным антибиотиком последней инстанции. Результаты предполагают, что условия в живой ткани — такие как снижение продукции Bap, наличие свободноплавающих бактерий или присутствие полезных компонентов в молоке — позволяют инженерным частицам работать значительно лучше, чем в статических лабораторных биопленках.
Что это может значить для ферм и не только
Исследование показывает, что нереплицирующиеся, упакованные в фаговые оболочки системы CRISPR могут избирательно уничтожать S. aureus при трудных, связанных с биопленкой инфекциях, не распространяясь и не вызывая одновременного лизиса огромного числа клеток. Хотя требуются высокие дозы частиц и перенос результатов с мышей на коров будет сложной задачей, эти частицы предлагают перспективную, контролируемую альтернативу антибиотикам для локализованных инфекций, таких как мастит. В более широком плане работа подчёркивает, что методы, кажущиеся неудачными в простых лабораторных тестах, могут всё же преуспеть в сложной среде животного, и открывает путь к библиотекам настраиваемых ePICI, ориентированных на разные бактерии, фаговые оболочки и направляющие последовательности.
Цитирование: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Ключевые слова: коровий мастит, Staphylococcus aureus, CRISPR-терапия, лечение на основе фагов, инфекции в биопленках