Clear Sky Science · ru
Микробиота кишечника опосредует депрессивоподобное поведение у мышей при хронической инфекции Echinococcus multilocularis
Когда скрытая инфекция влияет на разум
Большинство людей считают паразитов проблемой кишечника или печени, но не разума. Тем не менее многие пациенты с длительными инфекциями жалуются на плохое настроение, усталость и утрату способности получать удовольствие. В этом исследовании изучается неожиданный звеньевой механизм: как хроническая инфекция ленточным червём, локализующаяся в брюшной полости и печени, может через изменения в кишечной микробиоте и химии организма вызывать депрессивоподобное поведение у мышей. Понимание этой цепочки событий в перспективе может указать новые пути защиты психического здоровья у людей с упорными инфекциями.
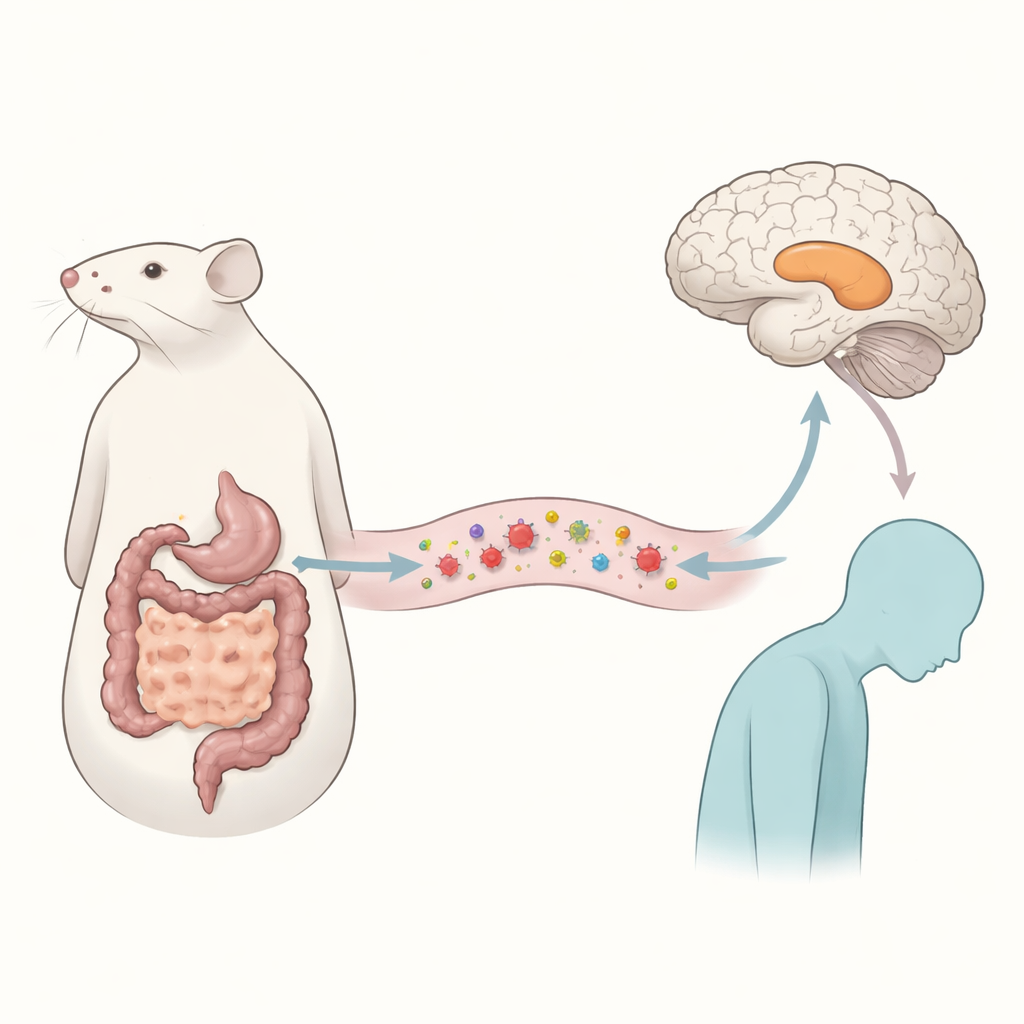
Паразит-попутчик и перемены в настроении
Исследователи сосредоточились на Echinococcus multilocularis — паразите, вызывающем альвеолярный эхинококкоз, тяжёлое заболевание, которое преимущественно поражает печень. Пациенты с этой патологией часто сообщают о плохом психическом самочувствии, но причины оставались неясными. Чтобы изучить это, команда инфицировала мышей паразитом и выжидала два месяца — достаточно, чтобы смоделировать хроническую инфекцию. Затем животные прошли набор поведенческих тестов, предназначенных для различения простой болезни и более специфических изменений настроения. Инфицированные мыши двигались столько же, сколько и здоровые, и нормально справлялись с обучением и запоминанием задач, однако демонстрировали явные признаки депрессивоподобного поведения: меньший интерес к сладким вознаграждениям и большее время неподвижности в стрессовых тестах, которые широко используются как индикаторы состояний, похожих на отчаяние у грызунов.
Тонкие изменения в мозге и иммунные сигналы
Изучая мозг, учёные сосредоточились на гиппокампе и миндалине — областях, глубоко вовлечённых в эмоции и стресс. Их общая структура осталась неизменной, но при микроскопическом осмотре некоторые нейроны выглядели уменьшенными или деформированными, а наружная мембрана их ядер казалась сморщенной. Микроглия — резидентные иммунные клетки мозга — была более многочисленна в отдельных регионах и имела более простое, менее ветвистое строение — признаки смещения от спокойного, «патрулирующего» состояния к активированному. В то же время в ткани кишечника и в крови инфицированных мышей выявили повышенные уровни провоспалительных молекул, особенно цитокинов IL‑6 и MCP‑1, а гены некоторых из этих сигнальных молекул были более активны в гиппокампе. В сумме эти данные указывают на медленно текущую воспалительную реакцию, которая простирается от кишечника к мозгу и сдвигает баланс его иммунных клеток.
Кишечные бактерии и утраченные химические посредники
Далее команда спросила, не причастна ли к происходящему сообщество микробов кишечника. С помощью секвенирования ДНК они обнаружили, что инфекция перестраивает кишечную микробиоту: полезные группы, такие как Lactobacillus и Bifidobacterium, заметно сократились, тогда как другие роды, включая Ruminococcus и Prevotella, увеличились. У мышей с меньшим количеством «дружественных» бактерий как правило отмечались более высокие уровни провоспалительных цитокинов в кишечнике и крови. Одновременно анализ крови и широкий метаболомный профиль показали истощение ключевых компонентов пути триптофан–серотонин. Уровни триптофана (пищевой аминокислоты), его промежуточного метаболита N‑ацетилсеротонина и нейромедиатора серотонина (5‑HT) снижались у инфицированных животных. Эти изменения напоминают сдвиги, описанные у людей с большим депрессивным расстройством, и были тесно связаны с численностью определённых кишечных микробов.
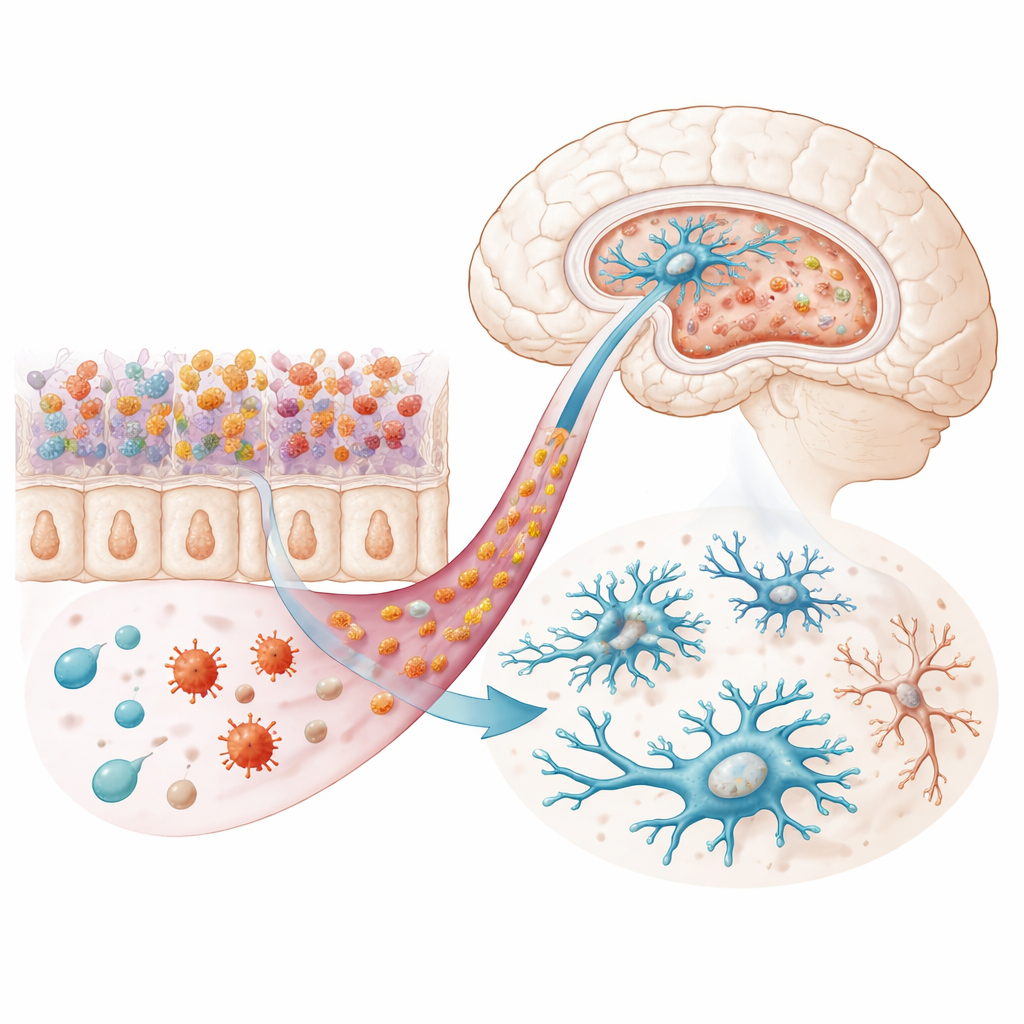
Перенос микробиоты — перенос настроения
Чтобы проверить, достаточно ли изменённой микробиоты, чтобы вызвать поведенческие изменения, исследователи провели трансплантацию фекальной микробиоты. Сначала они очистили кишечник здоровых мышей от бактерий с помощью антибиотиков, затем пересадили фекалии от донора либо инфицированного, либо неинфицированного. Поразительно, что реципиенты микробиоты от инфицированных доноров развивали депрессивоподобное поведение и избегали центра открытой арены, демонстрируя поведение, похожее на тревожное, хотя сами никогда не контактировали с паразитом. Эти мыши также проявляли усиленное воспаление, пониженные уровни триптофана и связанных с серотонином молекул в крови, а микроглия напоминала таковую у напрямую инфицированных животных — более многочисленная в отдельных регионах, менее ветвистая и заполненная лизосомоподобными структурами, что указывает на повышенный клеточный стресс или активность по утилизации материалов.
Что это значит для здоровья человека
Для непрофессионала главный вывод таков: хроническая инфекция в теле может нарушать кишечное микробное сообщество и химические посредники, которые оно помогает продуцировать, а это, в свою очередь, может влиять на иммунные клетки мозга и схемы, управляющие настроением. Исследование не утверждает, что этот ленточный червь вызывает клиническую депрессию у людей, но предлагает детальную карту того, как долгосрочный паразит, воспалённый кишечник, нарушенная микробиота и изменённый метаболизм триптофана–серотонина могут действовать совместно, порождая депрессивоподобные проявления. Возникающая картина даёт повод полагать, что в будущем лечение психических осложнений хронических инфекций может включать не только эрадикацию паразита, но и подавление воспаления и восстановление здоровой кишечной микробиоты.
Цитирование: Wen, R., Xin, Y., Bao, S. et al. The gut microbiota mediates depression-like behaviors in mice with chronic Echinococcus multilocularis infection. npj Biofilms Microbiomes 12, 63 (2026). https://doi.org/10.1038/s41522-026-00929-5
Ключевые слова: ось кишечник—мозг, микробиом, паразитарная инфекция, депрессия, метаболизм триптофана