Clear Sky Science · ru
Регуляторный путь ppGpp–HpaR1–gum модулирует продукцию экзополисахаридов у Xanthomonas campestris pv. campestris
Почему «липкие» бактерии важны для сельского хозяйства
Многие патогенные бактерии выживают и распространяются, окутываясь скользкими сахаристыми оболочками, известными как биоплёнки. В овощных культурах, таких как капуста и брокколи, эти оболочки могут закупоривать сосудистую систему растений, вызывая печально известное «чёрное гниение» и значительные потери урожая. В этом исследовании заглядывают внутрь одной из таких бактерий, Xanthomonas campestris, чтобы выяснить, как внутренняя химическая сигнализация контролирует производство её сахаристого щита. Понимание этой скрытой цепи управления может помочь учёным разработать лучшие способы защиты культур или даже использовать эти сахара для промышленных целей.
Микроб, поражающий растения, и его сахарная броня
Xanthomonas campestris проникает в сосуды крестоцветных — таких растений, как капуста, цветная капуста и горчица — и производит большие количества липкого вещества под названием ксантановая камедь. Этот материал состоит из длинных цепочек сахарных звеньев и составляет основную часть биоплёнки, которая помогает бактериям прикрепляться к тканям растения, противостоять его защитным механизмам и переживать неблагоприятные условия. В растении эти толстые сахарные слои могут перекрывать поток воды, приводя к омертвению тканей и характерным V-образным пятнам на листьях при чёрном гниении. Любопытно, что та же ксантановая камедь широко используется как загуститель в пищевой и других отраслях, делая этот бактериальный сахар одновременно аграрным злом и промышленным ресурсом.
Внутренний сигнал тревоги, формирующий поведение бактерии
Внутри многих бактерий небольшая сигнальная молекула ppGpp действует как аварийная тревога. Когда ресурсов не хватает или появляются другие стрессы, уровень ppGpp повышается и запускает широкий «строгий ответ», перестраивающий рост, метаболизм и стратегии выживания. Ранее было показано, что ppGpp может способствовать формированию биоплёнок у нескольких видов, и что его отсутствие у Xanthomonas ослабляет способность бактерии образовывать биоплёнки и вызывать заболевание. Оставалось неясным, как именно эта маленькая молекула связана с механизмами синтеза толстой экзополисахаридной (EPS) оболочки у данного фитопатогена.
Прослеживание пути от сигнала к сахару
Исследователи сравнили нормальные бактерии с мутантами, неспособными синтезировать ppGpp. На средах с избытком сахара мутанты без ppGpp образовывали меньшие, менее мукоидные колонии, а прямые измерения показали значительное снижение выработки EPS. Однако химическая хроматография с инфракрасной спектроскопией и изображения электронного микроскопа указали, что базовый состав и высшая структура EPS не изменились: мутанты просто синтезировали его в меньших количествах. Внимание переключилось на кластер генов «gum», группу генов, кодирующих ферменты, собирающие ксантановую камедь. По данным измерений экспрессии генов и РНК‑секвенирования, почти все гены gum были снижены в клетках, лишённых ppGpp, что помещает ppGpp выше в иерархии контроля над этим кластером.
Ключевой посредник: переключатель HpaR1
Между сигналом ppGpp и генами gum находится регуляторный белок HpaR1 — транскрипционный фактор, который связывается с ДНК и усиливает активность генов gum. Исследование показало, что ppGpp действует по двум направлениям. Во‑первых, в клетках без ppGpp активность гена hpaR1 снижалась, то есть доступного белка HpaR1 становилось меньше. Во‑вторых, в очищенных лабораторных тестах добавление ppGpp непосредственно усиливало связывание HpaR1 с участками ДНК, контролирующими гены gum, и даже с собственной регуляторной областью. При умеренных уровнях ppGpp это связывание явно усиливалось, хотя при чрезвычайно высоких уровнях эффект частично ослабевал, что указывает на тонко настроенный баланс. Когда учёные искусственно повышали количество HpaR1, синтез EPS снова возрастал — даже у бактерий, лишённых ppGpp — подтверждая, что HpaR1 является ключевым посредником между сигналом тревоги и ферментами синтеза сахара.
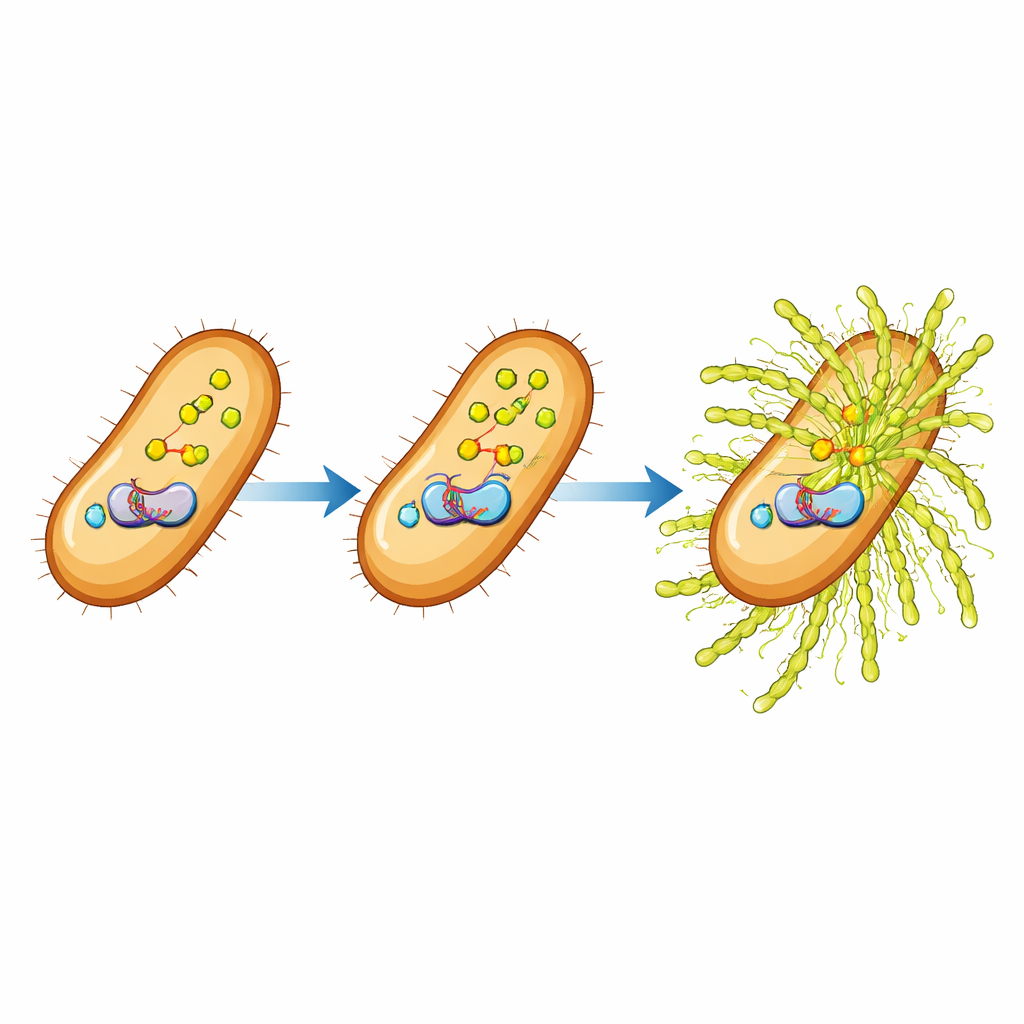
Что эта схема управления значит для сельского хозяйства и не только
Проще говоря, работа раскрывает трёхступенчатую цепочку внутри фитопатогена: внутренняя сигнальная молекула (ppGpp) повышает и укрепляет ДНК‑связывающий переключатель (HpaR1), который, в свою очередь, усиливает работу сахарного завода (гены gum), приводя к образованию более толстой защитной слизи вокруг бактерий. Детальная карта пути ppGpp–HpaR1–gum показывает, как экологические стресс‑сигналы преобразуются в изменения производства матрицы биоплёнки. Для фермеров и фитопатологов эти данные указывают новые цели для разрушения бактериальной брони и снижения ущерба от чёрного гниения. Для микробиологов в целом результаты добавляют важный фрагмент к пониманию того, как универсальные стресс‑сигналы контролируют формирование сложных микробных сообществ.
Цитирование: Bai, K., Xu, X., Yu, C. et al. The ppGpp-HpaR1-gum regulatory pathway modulates exopolysaccharides production in Xanthomonas campestris pv. campestris. npj Biofilms Microbiomes 12, 60 (2026). https://doi.org/10.1038/s41522-026-00926-8
Ключевые слова: бактериальные биоплёнки, фитопатогены, ксантановая камедь, сигналы стресса, экзополисахариды