Clear Sky Science · ru
Нанотела, переносимые Lactobacillus, повышают продуктивность бройлеров при субклиническом некротическом энтерите с сопутствующими изменениями микробиома и транскриптома
Почему здоровье кишечника куриных тушек важно для вашей тарелки
Современные птицефабрики балансируют на тонкой грани: им нужно эффективно выращивать миллиарды птиц и при этом сокращать использование антибиотиков, которые могут способствовать развитию лекарственной устойчивости у людей. Одна из крупнейших скрытых угроз бройлерам — кишечное заболевание, называемое субклиническим некротическим энтеритом. Птицы с этим состоянием часто выглядят нормально, но растут медленнее и съедают больше корма, чтобы набрать тот же вес, тихо повышая стоимость и экологический след производства курятины. В этом исследовании изучается новый, очень таргетный пробиотический подход: полезным бактериям придают крошечные фрагменты антител, чтобы нейтрализовать токсичные вещества прямо в кишечнике.
Дорогое, в основном незаметное заболевание кишечника
Некротический энтерит вызывается обычной кишечной бактерией Clostridium perfringens, когда она чрезмерно размножается и выделяет мощные токсины. В тяжелой форме болезнь убивает птиц и вызывает явные повреждения кишечника. Но гораздо более распространена субклиническая форма, при которой токсины, такие как NetB и альфа-токсин, тонко повреждают слизистую кишечника. Птицы хуже усваивают корм, набирают меньше веса и при этом демонстрируют мало внешних признаков болезни. В мировом масштабе этот незаметный удар по продуктивности оценивают в более чем 2 миллиарда долларов США в год. Исторически фермы контролировали проблему с помощью антибиотиков в корме, но растущая обеспокоенность устойчивостью к антимикробным препаратам и спрос потребителей на курицу «без антибиотиков» сделали такие препараты менее приемлемыми, создав острую потребность в точных, нелекарственных альтернативах.
Преобразование пробиотиков в таргетные блокировщики токсинов
Исследователи опирались на ранние работы, в которых они модифицировали два штамма пробиотической бактерии Limosilactobacillus reuteri, чтобы те секретировали «нанотела» — очень маленькие фрагменты антител, которые прикрепляются к NetB или альфа-токсину и нейтрализуют их. В новом исследовании они проверили, могут ли эти сконструированные пробиотики улучшить показатели бройлеров при мягкой, коммерчески реалистичной форме заболевания. В ходе 43-дневного эксперимента более 2000 птиц разделили на четыре группы: группа контроля с вызовом заболевания; группа, получавшая распространенный профилактический антибиотик (бакитрацин метилендизалицилат, BMD); группа, получавшая генетически модифицированные штаммы, продуцирующие нанотела (обозначенные NE01 и NE06); и группа, получавшая исходные, немодифицированные родительские штаммы пробиотика. Всем птицам делали вакцинацию против кокцидиоза, а затем подвергали воздействию C. perfringens для индукции субклинического заболевания.
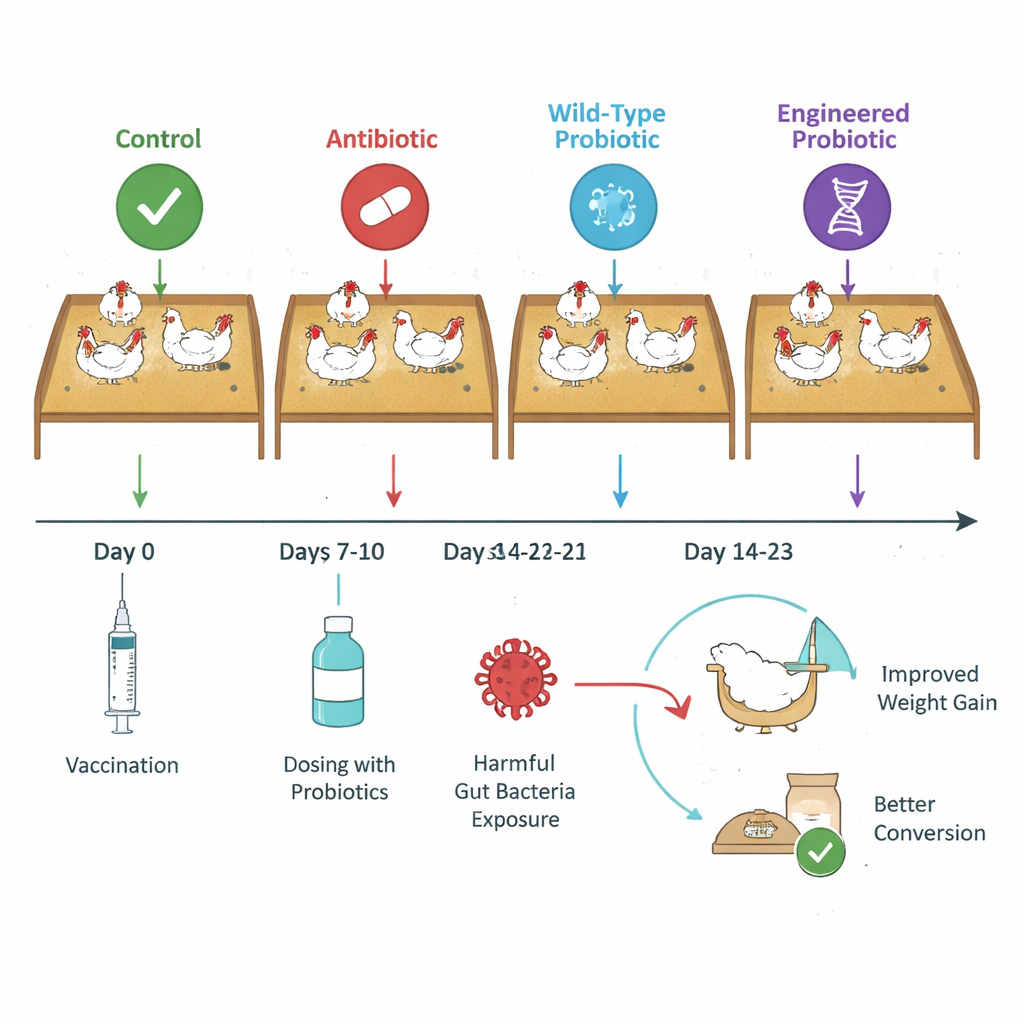
Лучший рост при меньших скрытых затратах
Птицы, получавшие штаммы, продуцирующие нанотела, постоянно эффективнее превращали корм в массу тела по сравнению с другими группами. Их коэффициент конверсии корма с поправкой на смертность улучшился на 4–7 «пунктов» (0,04–0,07 единицы) по отношению к нелеченым птицам в разные моменты времени, а к концу исследования они весили на 34–81 грамм больше по сравнению как с контрольной группой с вызовом, так и с группой антибиотика или птицами, получавшими обычные пробиотики. Интересно, что классические показатели болезни — такие как видимые поражения кишечника и подсчеты C. perfringens в фекалиях и содержимом слепой кишки — показали лишь незначительные различия между группами. Это означает, что все птицы испытывали похожий уровень низкоуровневого воздействия, но группа с нанотелами справлялась с ним гораздо эффективнее, превращая тот же корм в большее количество мяса.
Более спокойные микробиомы и менее активные иммунные ответы
Чтобы понять, почему улучшилась производительность, команда заглянула дальше общей патологии и исследовала микробиом и активность генов в кишечнике и печени. Метратранскриптомный анализ содержимого тонкой кишки (дуоденум/тощая кишка) показал, что у птиц, получавших модифицированные штаммы, было больше транскриптов L. reuteri и обнаруживалось экспрессирование генов нанотел, что подтверждает выживание пробиотиков в кишечнике и производство ими молекул, блокирующих токсины. Общий состав микробиоты менялся главным образом с возрастом птиц, а не в зависимости от лечения, но в группе нанотелов наблюдалась меньшая вариабельность между образцами, что указывает на более стабильное и устойчивое сообщество кишечных микробов. Функционально микробы в этой группе экспрессировали больше генов, связанных с ферментацией и синтезом белка, и меньше генов, связанных с дыханием и использованием нитратов — паттерны, ассоциированные с менее воспаленной средой. Исследователи также обнаружили повышенную экспрессию ферментов, синтезирующих соединение 2,3-бутандиол, которое в животных моделях проявляет противовоспалительный эффект.
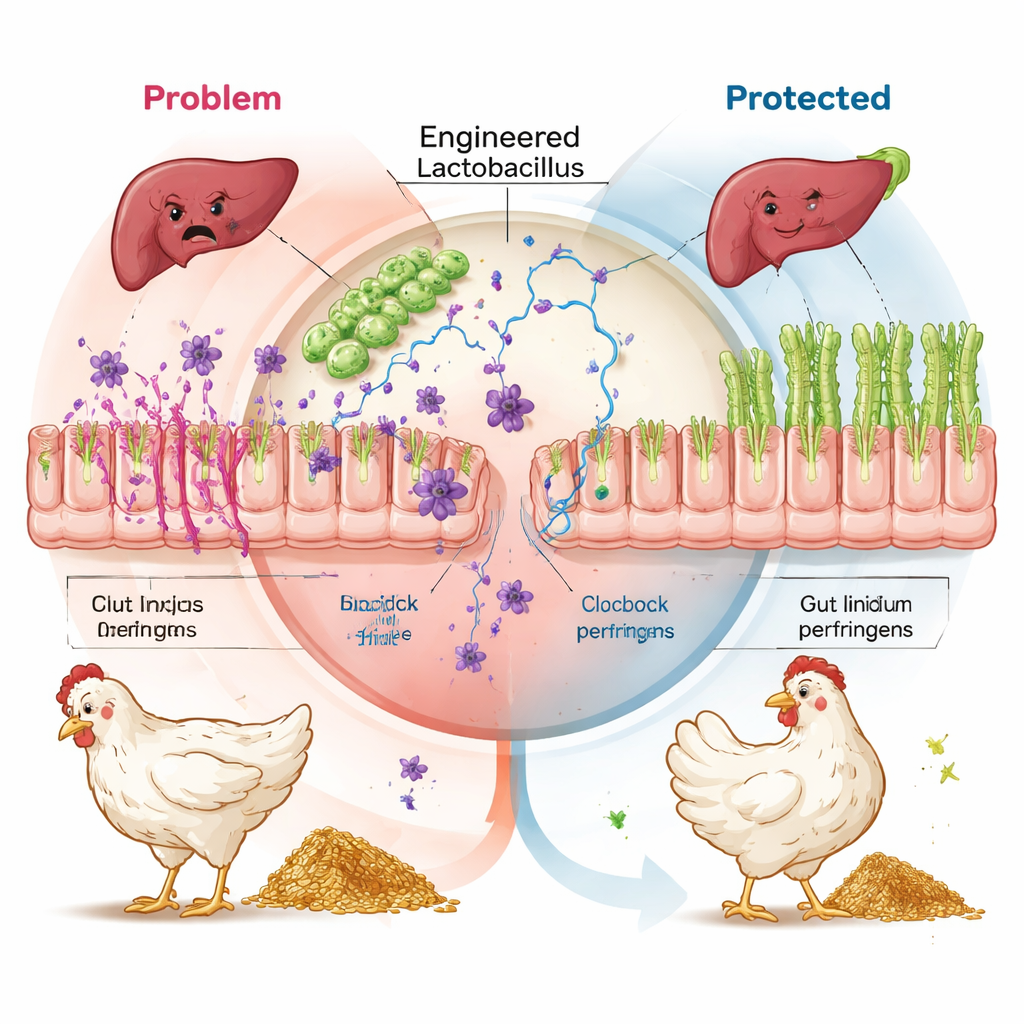
Защита отдаленных органов и повышение эффективности
История не ограничилась кишечником. Экспрессия генов в тощей кишке и печени показала, что у птиц, получавших инженерные пробиотики, значительно снижался уровень активации иммунных и окислительно-стрессовых путей по сравнению с группой с вызовом заболевания, а во многих случаях — и по сравнению с группами антибиотика и обычных пробиотиков. В печени — органе, который страдает вторично от бактериальных токсинов — у группы нанотелов наблюдалось снижение сигнализации по путям инсулина и mTOR, известных тем, что они активируются при повреждении, вызванном токсинами, при одновременном усилении антиоксидантных и энергообразующих путей. В совокупности эти выводы указывают на то, что нейтрализация NetB и альфа-токсина на поверхности кишечника предотвращает каскад воспаления и повреждения тканей, экономя птице метаболические ресурсы, которые в противном случае тратились бы на постоянную борьбу с скрытыми инфекциями.
Что это значит для будущего здоровья кур и людей
Для неспециалиста ключевая мысль такова: не все «пробиотики» одинаковы. Оснастив полезные бактерии точно нацеленными нанотелами, исследователи создали живую терапию, которая защищает кур от распространенного, в основном незаметного кишечного заболевания без использования традиционных антибиотиков — и при этом превзошла как антибиотик, так и стандартные пробиотики. Птицы съедали меньше корма, чтобы достичь товарного веса, с меньшими признаками внутреннего стресса. Если аналогичные стратегии можно будет применить к другим сельскохозяйственным животным, а в перспективе и к людям, инженерные пробиотики могут стать мощным способом обезвредить вредные кишечные токсины, сохраняя полезные микробы и замедляя распространение антибиотикорезистентности.
Цитирование: Hall, A.N., Manuja, S., Payling, L.M. et al. Lactobacillus-vectored nanobodies improve broiler productivity under sub-clinical necrotic enteritis with associated microbiome and transcriptome changes. npj Biofilms Microbiomes 12, 52 (2026). https://doi.org/10.1038/s41522-026-00916-w
Ключевые слова: инженерные пробиотики, некротический энтерит, здоровье кишечника птицы, нанотела, альтернативы антибиотикам